Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn B.
Trạng thái khí lúc đầu: p1 = 750 mmHg; T1 = 30 + 273 = 303 K; V1
Trạng thái khí lúc sau: p2; T2 = 200 + 273 = 473 K; V2 = 1,5.V1.
Từ phương trình trạng thái:
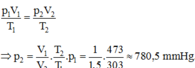

Phương trình trạng thái khí lí tưởng: \(\dfrac{P.V}{T}=\text{const}\)
Suy ra: \(\dfrac{P_1.V_1}{T_1}=\dfrac{P_2.V_2}{T_2}\)
\(\Rightarrow T_2=\dfrac{P_2.V_2}{P_1.V_1}.T_1=\dfrac{7.10^5}{0,8.10^5.5}.(273+50)=565.25K\)
\(\Rightarrow t_2=565,25-273=292,25^0C\)

Chọn D.
Áp dụng định luật Bôi-lơ – Ma-ri-ốt, ta có p1V1 = p2V2
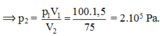

Chọn A.
Quá trình biến đổi là đẳng tích, ta có:
![]()
Với p1 = 40 atm; p2 = p1 + 10 = 50 atm; T1 = t1 + 273 = 27 + 273 = 300 K.
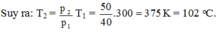

Chọn B.

p 2 = V 1 V 2 . T 2 T 1 . p 1 = 1 1,5 . 473 303 .750 = 780,5 m m H g

Đáp án: C
Ta có:
- Trạng thái 1: p 1 = p , T 1 = t + 273
- Trạng thái 2: p 2 = p 1 + 1 360 , T 2 = t + 1 + 273
Do thể tích không đổi, theo định luật Sáclơ, ta có:
p 1 T 1 = p 2 T 2 ↔ p t + 273 = p 1 + 1 360 t + 1 + 273 → t = 87 0 C
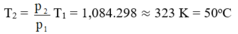
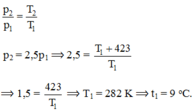
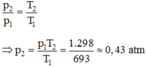
Chọn A.
Coi quá trình biến đổi là đẳng tích, ta có:
T2 = p 2 p 1 T1 = 1,084.298 ≈ 323 K = 50oC