
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Mik ra kết quả luôn nhé.
- Lần lượt:
N(V), N(IV), Al(III), Al(III), Fe(II)
- Gọi CTHH là: \(\overset{\left(II\right)}{Fe_x}\overset{\left(II\right)}{O_y}\)
Ta có: \(II.x=II.y\)
\(\Leftrightarrow\dfrac{x}{y}=\dfrac{II}{II}=\dfrac{1}{1}\Leftrightarrow\left\{{}\begin{matrix}x=1\\y=1\end{matrix}\right.\)
Vậy CTHH là: FeO

\(a) Zn + H_2SO_4 \to ZnSO_4 + H_2\\ b) n_{H_2} = n_{Zn} = \dfrac{97,5}{65} = 1,5(mol)\\ V_{H_2} = 1,5.22,4= 33,6(lít)\\ c) n_{Fe_2O_3} = \dfrac{120}{160} = 0,75(mol)\\ Fe_2O_3 + 3H_2 \xrightarrow{t^o} 2Fe + 3H_2O\\ \dfrac{n_{Fe_2O_3}}{1} = 0,75 > \dfrac{n_{H_2}}{3} = 0,5 \to Fe_2O_3\ dư\\ n_{Fe_2O_3\ pư} = \dfrac{n_{H_2}}{3} = 0,5(mol)\\ \Rightarrow m_{Fe_2O_3\ dư} = 120 - 0,5.160 = 40(gam)\)

-Thí nghiệm: Cho một ít KMnO4 hoặc KClO3 vào ống nghiệm có cắm ống dẫn khí,đầu ống nghiệm được nút lại.
Câu hỏi là: cách điều chế oxi trong phòng thí nghiệm á
Giúp mình đi mọi ngừi ơiii 😥🥺

1.
\(Ca+2H_2O\rightarrow Ca\left(OH\right)_2+H_2\)
\(2Na+2H_2O\rightarrow2NaOH+H_2\)
\(P_2O_5+3H_2O\rightarrow2H_3PO_4\)
\(K_2O+H_2O\rightarrow2KOH\)
\(SO_2+H_2O\rightarrow H_2SO_3\)
\(SO_3+H_2O\rightarrow H_2SO_4\)
2.
(1)\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
(2)\(2Cu+O_2\rightarrow\left(t^o\right)2CuO\)
(3)\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\)
(4)\(4Na+O_2\rightarrow\left(t^o\right)2Na_2O\)
(5)\(Na_2O+H_2O\rightarrow2NaOH\)
(6)\(S+O_2\rightarrow\left(t^o\right)SO_2\)
(7)\(SO_2+H_2O\rightarrow H_2SO_3\)
(1) 2KMnO4 --to--> K2MnO4 + MnO2 + O2
(2) 2Cu + O2 --to--> 2CuO
(3) CuO + CO --to--> Cu + CO2
(4) 4Na + O2 --to--> 2Na2O
(5) Na2O + H2O ---> 2NaOH
(6) S + O2 --to--> SO2
(7) SO2 + H2O ---> H2SO3

Bài 4 :
a)
\(Mg + H_2SO_4 \to MgSO_4 + H_2\\ b) n_{H_2} = n_{Mg} = \dfrac{4,8}{24} = 0,2(mol)\\ V_{H_2} = 0,2.22,4 = 4,48(lít)\\ c) n_{MgSO_4} =n_{Mg} = 0,2(mol)\\ m_{MgSO_4} = 0,2.120 = 24(gam)\)
Bài 5 :
a)
\(Zn + 2HCl \to ZnCl_2 + H_2\\ b) n_{H_2} = n_{Zn} = \dfrac{97,5}{65} =1,5(mol)\\ V_{H_2} = 1,5.22,4 = 33,6(lít)\\ c) n_{Fe_2O_3} = \dfrac{120}{160} = 0,75(mol)\\ Fe_2O_3 + 3H_2 \xrightarrow{t^o} 2Fe + 3H_2O\\ n_{H_2} = 1,5 < 3n_{Fe_2O_3} = 2,25 \to Fe_2O_3\ dư\\ n_{Fe_2O_3\ pư} = \dfrac{1}{3}n_{H_2} = 0,5(mol)\\ \Rightarrow m_{Fe_2O_3\ dư} = 120 - 0,5.160 = 40(gam)\)

\(n_{O_2}=\dfrac{3.36}{22.4}=0.15\left(mol\right)\)
\(3Fe+2O_2\underrightarrow{t^0}Fe_3O_4\)
\(.......0.13....0.075\)
\(V_{O_2}=3.36\left(l\right)\)
\(m_{Fe_3O_4}=0.075\cdot232=17.4\left(g\right)\)
a) pt: 3Fe + 2O2 \(\rightarrow\) Fe3O4
b) Thể tích khí oxi cho ở đề bài rồi mà
c) Theo pt: nFe3O4 = \(\dfrac{1}{2}n_{O_2}=\dfrac{1}{2}.0,15=0,075mol\)
\(\Rightarrow mFe_3O_4=0,075.232=17,4g\)
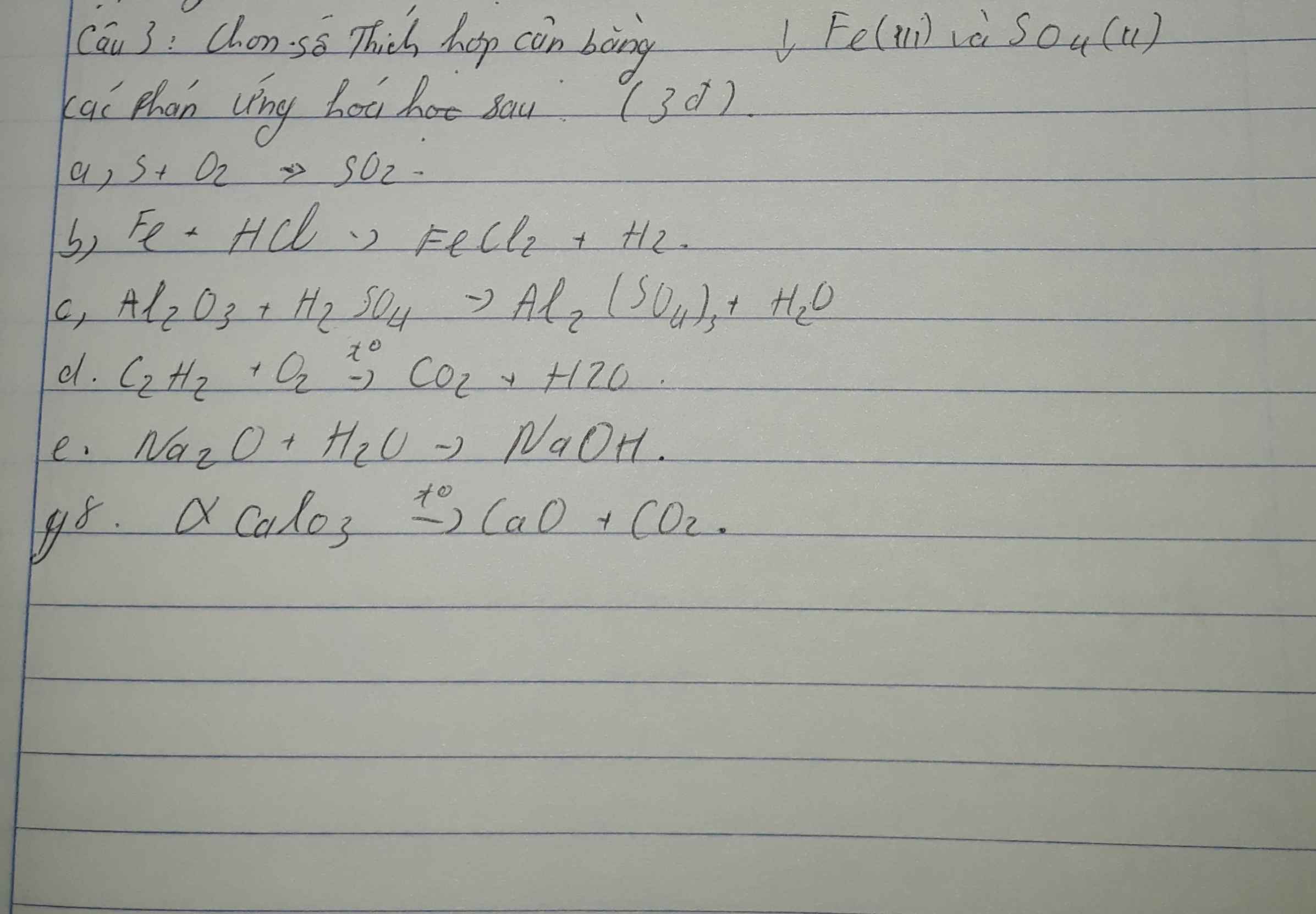
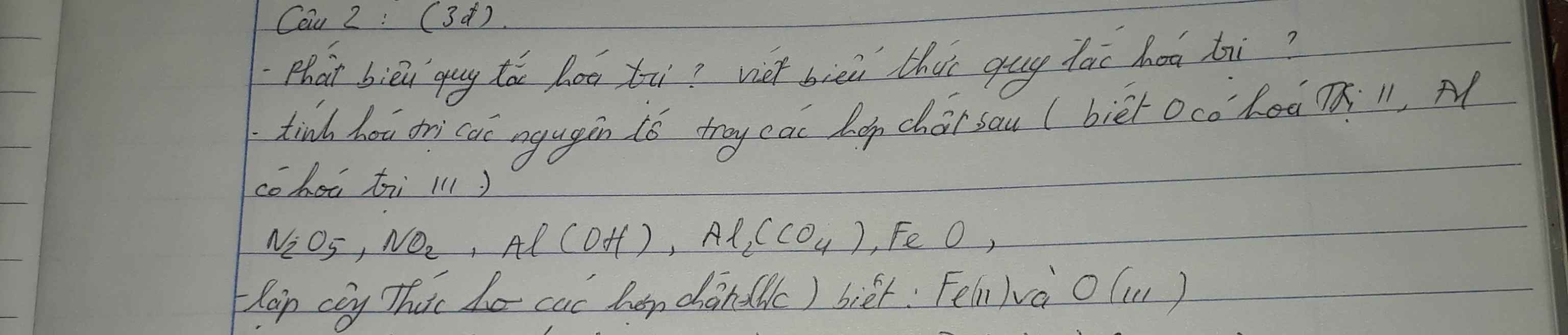
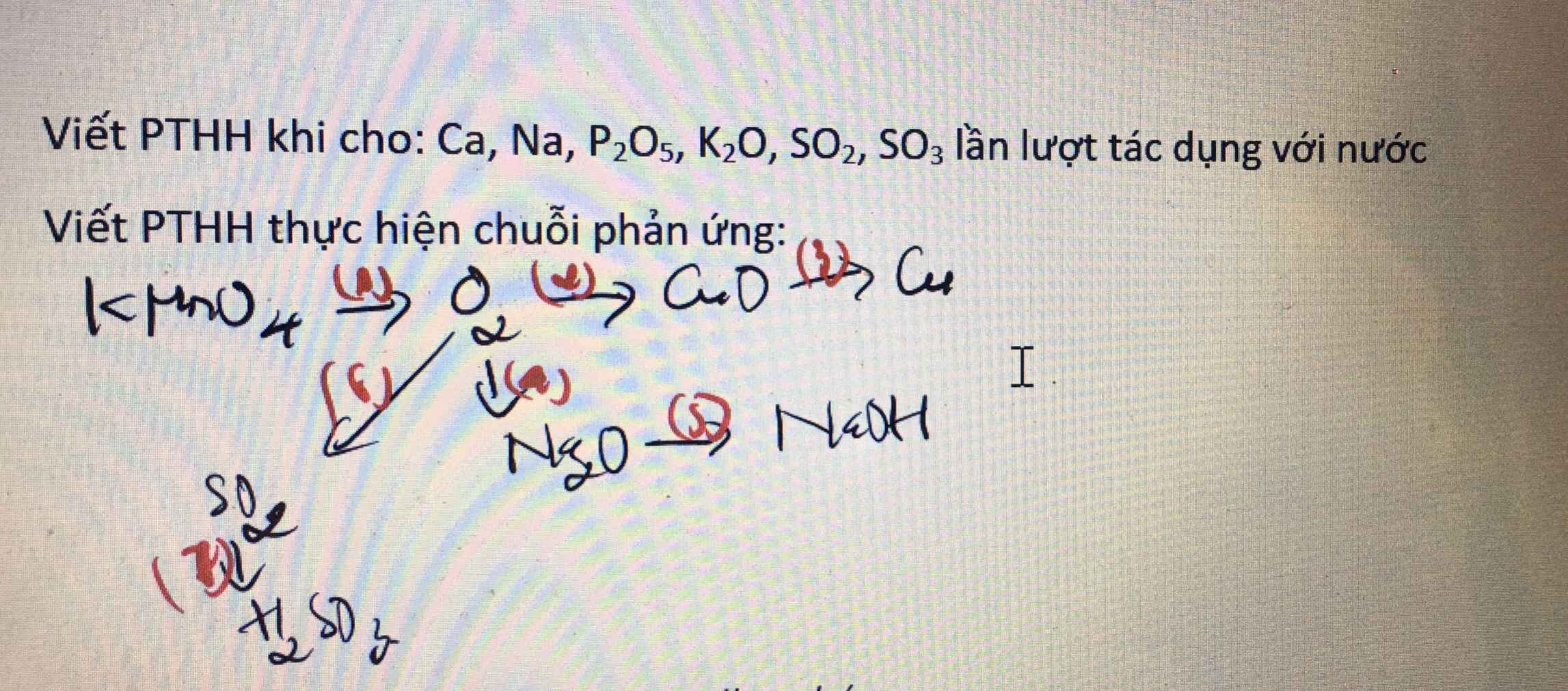



\(a.S+O_2\overset{t^o}{--->}SO_2\)
\(b.Fe+2HCl--->FeCl_2+H_2\)
\(c.Al_2O_3+3H_2SO_4--->Al_2\left(SO_4\right)_3+3H_2O\)
\(d.2C_2H_2+5O_2\overset{t^o}{--->}4CO_2\uparrow+2H_2O\)
\(e.Na_2O+H_2O--->2NaOH\)
\(g.CaCO_3\overset{t^o}{--->}CaO+CO_2\uparrow\)