Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Bài 4 :
100ml = 0,1l
300ml = 0,3l
\(n_{Na2SO4}=0,2.0,1=0,02\left(mol\right)\)
\(n_{BaCl2}=0,1.0,3=0,03\left(mol\right)\)
Pt : \(Na_2SO_4+BaCl_2\rightarrow2NaCl+BaSO_4|\)
1 1 2 1
0,02 0,03 0,04 0,02
a) Lập tỉ số so sánh : \(\dfrac{0,02}{1}< \dfrac{0,03}{1}\)
⇒ Na2SO4 phản ứng hết , BaCl2 dư
⇒ Tính toán dựa vào số mol của Na2SO4
\(n_{BaSO4}=\dfrac{0,02.1}{1}=0,02\left(mol\right)\)
⇒ \(m_{BaSO4}=0,02.233=4,66\left(g\right)\)
b) \(n_{NaCl}=\dfrac{0,02.2}{1}=0,04\left(mol\right)\)
\(n_{BaCl2\left(dư\right)}=0,03-0,02=0,01\left(mol\right)\)
\(V_{ddspu}=0,1+0,3=0,4\left(l\right)\)
\(C_{M_{NaCl}}=\dfrac{0,04}{0,4}=0,1\left(M\right)\)
\(C_{M_{BaCl2\left(dư\right)}}=\dfrac{0,01}{0,4}=0,025\left(M\right)\)
Chúc bạn học tốt


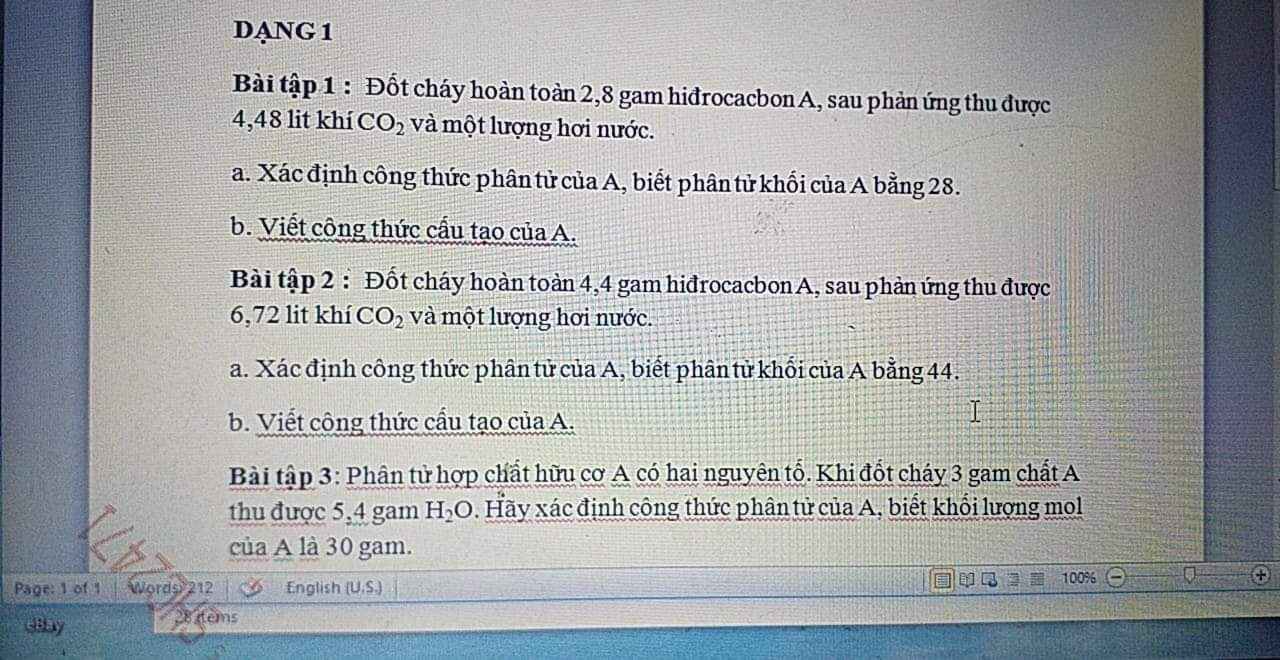
Bài 1: A là hiđrocacbon, nên trong A chỉ chứa hai nguyên tố là C và H
nCO2 = 0,2 mol → số mol của C trong A là nC = 0,2 mol → mC = 0,2.12 = 2,4 gam
mC + mH = mA → mH = 2,8 - 2,4 = 0,4 gam → nH = 0,4 mol
Đặt CTPT của A là CxHy
Có tỉ lệ x : y = nC : nH = 0,2 : 0,4 = 1 : 2
→ Công thức phân tử đơn giản nhất của A là CH2
→ Công thức phân tử của A có dạng (CH2)n
Phân tử khối của A bằng 28 → (12 + 2).n = 28 → n = 2
CTPT của A là C2H4
Công thức cấu tạo của A là CH2=CH2
Bài 2 và bài 3 tương tự bài 1, em tự làm theo cách trên.
Với bài 3, từ số mol H2O, em có thể suy ra số mol H trong A bằng cách nH = 2.nH2O

Ta có:
\(n_C=n_{CO2}=\frac{6,72}{22,4}=0,3\left(mol\right)\)
\(\Rightarrow m_C=0,3.12=3,6\left(g\right)\)
\(n_H=2n_{H2O}=\frac{2.7,2}{18}=0,8\left(mol\right)\)
\(\Rightarrow m_H=0,8.1=0,8\left(g\right)\)
\(m_O=6-3,6-0,8=1,6\left(g\right)\Rightarrow n_O=0,1\left(mol\right)\)
CTĐGN :(C3H8O)n
A có 3C nên n=1
Vậy CTPT của A là C3H8O
Các CTCT bạn tự vẽ nhé

Gọi \(\left\{{}\begin{matrix}n_{CH3OH}:a\left(mol\right)\\n_{C2H5OH}:b\left(mol\right)\end{matrix}\right.\)
\(CH_3OH+\frac{5}{2}O_2\rightarrow CO_2+2H_2O\)
a__________2,5a___a_______2a
\(C_2H_5OH+3O_2\rightarrow2CO_2+3H_2O\)
b_________3b______2b________3b
\(\Rightarrow n_{CO2}=\frac{8,96}{22,4}=0,4\left(mol\right)\)
Giải hệ PT:
\(\left\{{}\begin{matrix}32a+46b=11\\a+2b=0,4\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=0,2\\b=0,1\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{CH3OH}=\frac{0,2.32}{11}.100\%=58,18\%\\\%m_{C2H6OH}=100\%-58,18\%=41,82\%\end{matrix}\right.\)
Ta có:
\(n_{O2}=0,2.2,5+0,1.3=0,8\left(mol\right)\)
\(\Rightarrow V_{O2}=0,8.22,4=17,92\left(l\right)\)
\(n_{H2O}=0,2.2+0,1.3=0,7\left(mol\right)\)
\(\Rightarrow m_{H2O}=0,7.18=12,6\left(g\right)\)

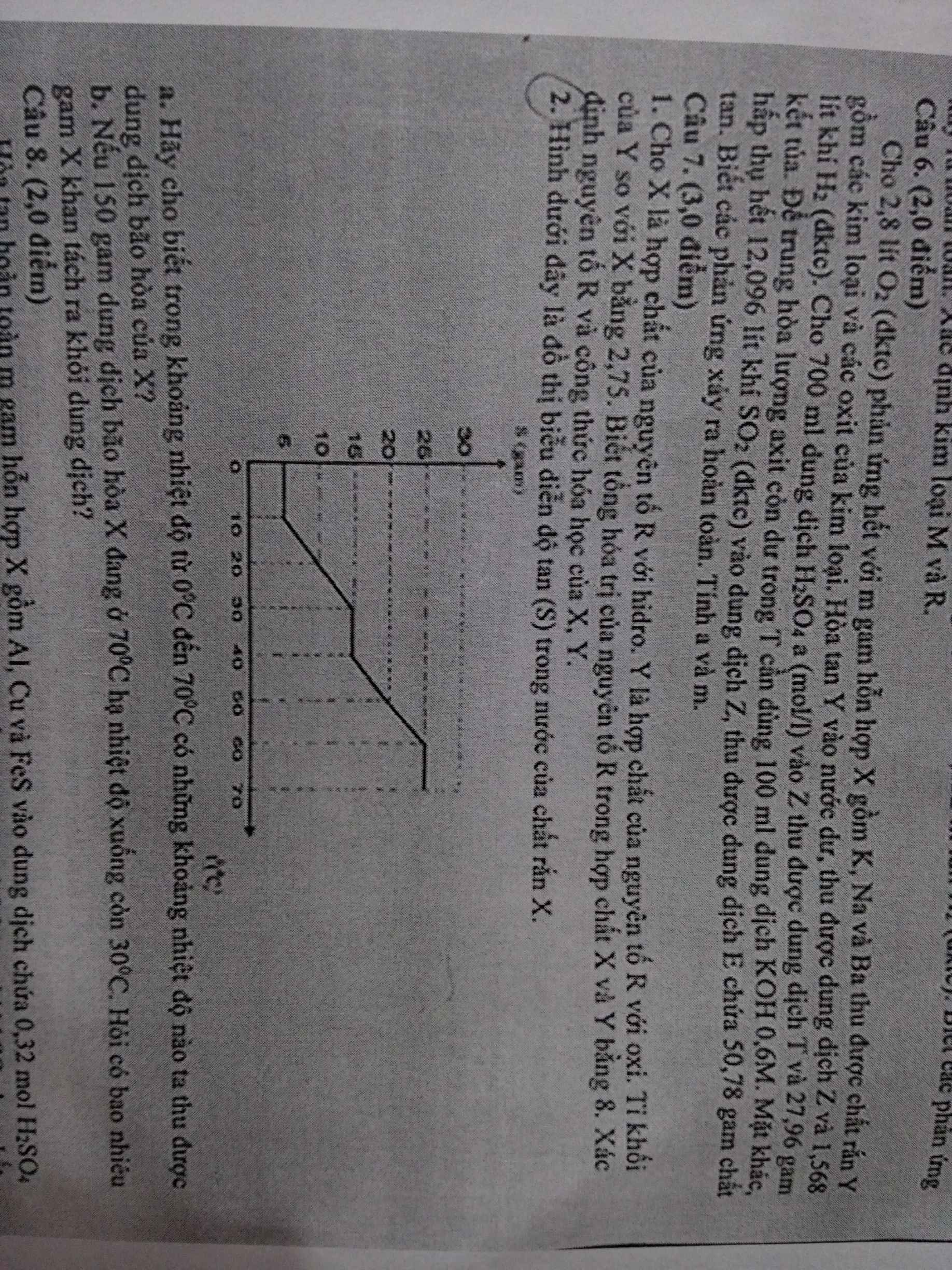
a) Những khoảng nhiệt độ mà dd X bão hòa:
+ 0-10oC
+ 30-40oC
+ 60-70oC
b)
- Xét khoảng 60-70oC:
Gọi khối lượng NaCl trong dd bão hòa tại khoảng nhiệt độ này là a (g)
\(S_{70^oC}=\dfrac{a}{150-a}.100=25\left(g\right)\)
=> a = 30 (g)
=> \(m_{H_2O}=150-30=120\left(g\right)\)
- Xét khoảng 30-40oC:
Gọi khối lượng NaCl trong dd bão hòa tại nhiệt độ này là b (g)
\(S_{30^oC}=\dfrac{b}{120}.100=15\)
=> b = 18 (g)
=> mNaCl(tách ra) = 30 - 18 = 12 (g)


Câu 25: (NH4)2HPO4 chứa N (đạm) và P (lân)
=> Chọn B
Câu 26: Chọn A
Tạo kết tủa xanh lơ là Cu(NO3)2
Cu(NO3)2 + 2NaOH ---> Cu(OH)2 + 2NaNO3
Tạo kết tủa nâu đỏ là Fe(NO3)3
Fe(NO3)3 + 3NaOH ---> Fe(OH)3 + 3NaNO3
Không hiện tượng là KNO3
Câu 27: \(n_{CO_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PTHH: Na2CO3 + 2HCl ---> 2NaCl + CO2 + H2O
0,15<----------------------------0,15
=> \(a=m_{Na_2CO_3}=0,15.106=15,9\left(g\right)\)
=> Chọn A
Câu 28: Chọn C (Fe bị thụ động trong H2SO4 đặc, nguội)