
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



Câu 18.
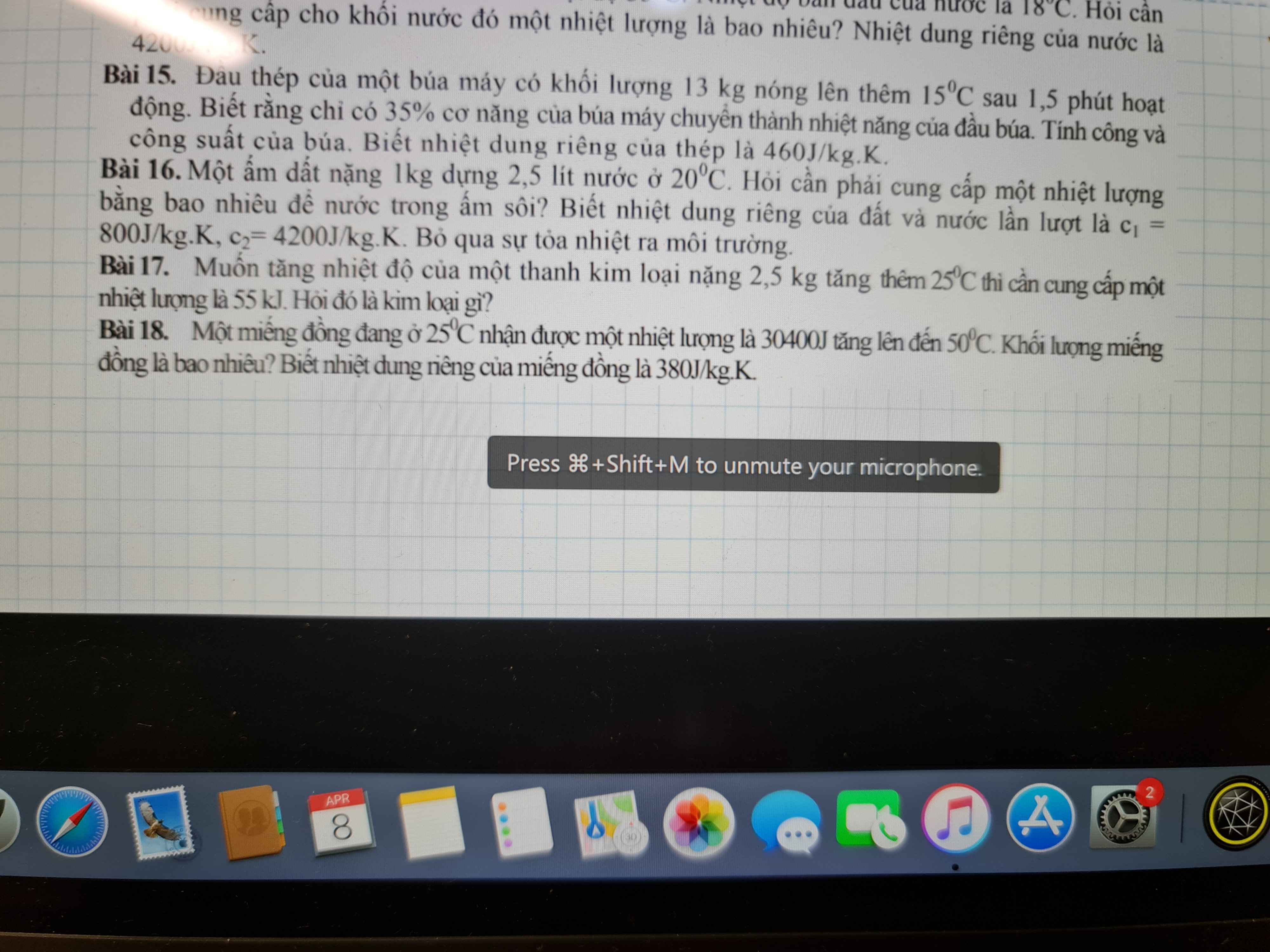
Nhiệt lượng miếng đồng thu vào:
\(Q=mc\left(t_2-t_1\right)\)
\(\Rightarrow30400=m\cdot380\cdot\left(50-20\right)\)
\(\Rightarrow m=2,67kg\)


\(m_{NaCl}=\dfrac{150.10}{100}=15\left(g\right)\\ m_{H_2O}=150-15=135\left(g\right)\)
Đong 15 gam NaCl khan, 135 gam nước cho sẵn vào cốc nước. Sau đó hóa tan 15 gam NaCl vào nước, dùng đũa thủy tinh khuấy đều thu được dd như theo yêu cầu của đề bài

Câu 4 :
Khí A : HCl
Khí B : $CO_2$
Khí C : $H_2$
Khí D : $O_2$
Câu 5 :
$n_{Fe} = a(mol) ; n_{Zn} = b(mol)$
Ta có : $56a + 65b = 31,15(1)$
$Fe + H_2SO_4 \to FeSO_4 + H_2$
$Zn + H_2SO_4 \to ZnSO_4 + H_2$
$n_{H_2} = a + b = \dfrac{11,2}{22,4} = 0,5(2)$
Từ (1)(2) suy ra a = 0,15 ; b = 0,35
$\%m_{Fe} = \dfrac{0,15.56}{31,15}.100\% = 26,97\%$
$\%m_{Zn} = 100\% -26,97\% = 73,03\%$

a) CM = \(\dfrac{n}{V}\Rightarrow n=C_M.V=0,9.2,5=2,25\left(mol\right)\)
b) 250 ml = 0,25 lit
CM = \(\dfrac{n}{V}\Rightarrow n=C_M.V=0,1.0,25=0,025\left(mol\right)\)
c) C0/0 = \(\dfrac{m_{ct}.100}{m_{dd}}\Rightarrow m_{ct}=\dfrac{C.m_{dd}}{100}=\dfrac{4.50}{100}=2\left(g\right)\)
nMgCl2 = \(\dfrac{m_{MgCl2}}{M_{MgCl2}}=\dfrac{2}{95}=0,02\left(mol\right)\)
d) C0/0 = \(\dfrac{m_{ct}.100}{m_{dd}}\Rightarrow m_{ct}=\dfrac{C.m_{dd}}{100}=\dfrac{15.200}{100}=30\left(g\right)\)
nKCl = \(\dfrac{m_{KCl}}{M_{KCl}}=\dfrac{30}{74,5}=0,4\left(mol\right)\)
Chúc bạn học tốt
Mình xin lỗi bạn nhé , mình đọc bị lộn đề , bạn sửa lại giúp mình :
a) Bổ sung :
mNaCl = nNaCl . MNaCl = 2,25 . 58,5 = 131,65 (g)
b) Bổ sung :
mMgSO4 = nMgSO4 . MMgSO4 = 0,025 . 120 = 3 (g)
Câu c và câu d bạn bỏ bước tính số mol giúp minh nhé

Câu 6 :
$a) C_xH_y + (x + \dfrac{y}{4} ) O_2 \xrightarrow{t^o} xCO_2 + \dfrac{y}{2}H_2O$
$b) 2xFe + yO_2 \xrightarrow{t^o} 2Fe_xO_y$
$c) Fe_xO_y + yCO \xrightarrow{t^o} xFe + yCO_2$
$d) Fe_xO_y + yH_2 \xrightarrow{t^o} xFe + yH_2O$
$e) 2Al + 2NaOH + 2H_2O \to 2NaAlO_2 + 3H_2$
$g) Cu+ 2H_2SO_{4_{đặc}} \xrightarrow{t^o} CuSO_4 +S O_2 + 2H_2O$
$h) 2Fe + 6H_2SO_{4_{đặc}} \xrightarrow{t^o} Fe_2(SO_4)_3 + 3SO_2 + 6H_2O$
Câu 7 :
a)
$Ba +2 H_2O \to Ba(OH)_2 + H_2$
$BaO + H_2O \to Ba(OH)_2$
b)
$n_{Ba} = n_{H_2} = \dfrac{4,48}{22,4} = 0,2(mol)$
$\Rightarrow n_{BaO} = \dfrac{58 - 0,2.137}{153} = 0,2(mol)$
$m_{dd} = 58 + 200 - 0,2.2 = 257,6(gam)$
$C\%_{Ba(OH)_2} = \dfrac{(0,2 + 0,2).171}{257,6}.100\% = 26,55\%$




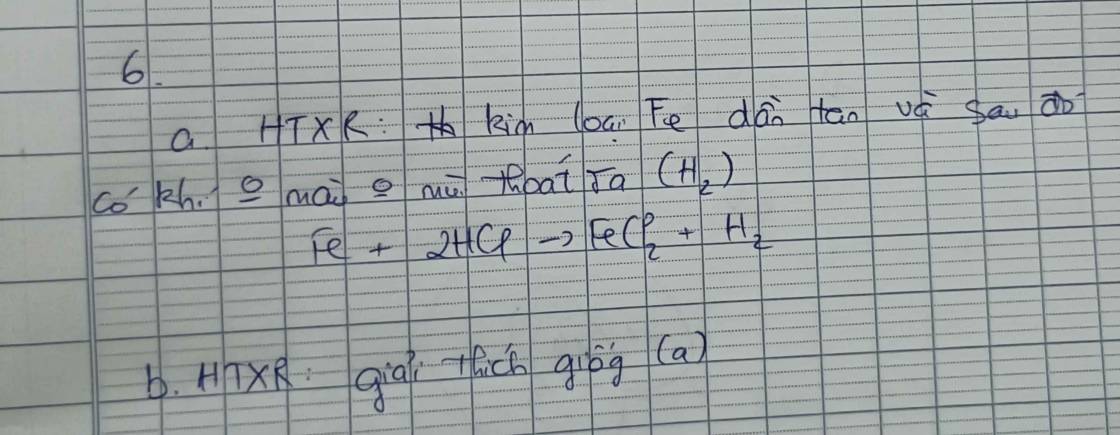











Câu 18:
PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
\(n_{HCl}=0,15.2=0,3\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,1}{1}< \dfrac{0,3}{2}\), ta được HCl dư.
Theo PT: \(n_{ZnCl_2}=n_{H_2}=n_{Zn}=0,1\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,1.22,4=2,24\left(l\right)\)
\(C_{M_{ZnCl_2}}=\dfrac{0,1}{0,15}=\dfrac{2}{3}\left(M\right)\)