Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

- Ba thí dụ phản ứng hóa hợp thuộc loại phản ứng oxi hóa – khử :
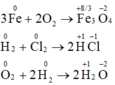
- Ba thí dụ phản ứng hóa hợp không thuộc loại phản ứng oxi hóa – khử :
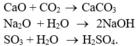

Ba thí dụ phản ứng phân hủy là phản ứng oxi hoá – khử :
CaCO3 -tº\(\rightarrow\) CaO + CO2\(\uparrow\)
NH4Cl -tº\(\rightarrow\) NH3 + HCl
Cu(OH)2 -tº\(\rightarrow\) CuO + H2O
Ba thí dụ phản ứng phân hủy không là phản ứng oxi hoá – khử
Cu(OH)2 -tº\(\rightarrow\)CuO + H2O
СаСОз -tº\(\rightarrow\) CaO + CO2
H2CO3 -tº\(\rightarrow\) CO2 + H2O.

- Ba thí dụ phản ứng phân hủy là phản ứng oxi hóa – khử:
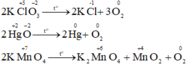
- Ba thí dụ phản ứng phân hủy không phải là phản ứng oxi hóa – khử:
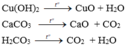

Đáp án D
Phản ứng oxi hóa khử nội phân tử là phản ứng mà sự thay đổi số oxi hóa xảy ra tại các nguyên tố trong cùng 1 phân tử. Các phản ứng oxi hóa – khử nội phân tử là: 2, 5, 7, 8, 9

Đáp án A
Ta có dãy chuyển đổi số OXH của S như sau:
![]()
Phản ứng thuộc loại phản ứng oxi hoá-khử khi S thay đổi số ôxi hóa.
Nhưng H2SO4 → SO2 có thể là phản ứng:
![]()
là phản ứng trao đổi

Chọn C
Phản ứng thế luôn là phản ứng oxi hóa – khử.
Một số ví dụ phản ứng không là phản ứng oxi hóa - khử:
C a O + C O 2 → C a C O 3 là phản ứng hóa hợp nhưng không là phản ứng oxi hóa – khử.
C a C O 3 → C a O + C O 2 là phản ứng phân hủy nhưng không là phản ứng oxi hóa – khử.
H C l + N a O H → N a C l + H 2 O là phản ứng trung hòa nhưng không là phản ứng oxi hóa - khử.

Ba thí dụ phản ứng hoá hợp thuộc loại phản ứng oxi hoá – khử :
.jpg)
Ba thí dụ phản ứng hoá hợp không thuộc loại phản ứng oxi hoá – khử :
CaO + CO2 \(\rightarrow\) СаСОз
Na2O + H2O \(\rightarrow\)2NaOH
SO3 + H2O \(\rightarrow\) H2SO4.