Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
M → Mn+ + ne
1,25 → 1,25nx
Zn → Zn2+ + 2e
x → 2x
Cl2 + 2e → 2Cl-
0,2 → 0,4
2H+ + 2e → H2
0,5 ← 0,25
BT e ⇒1,25nx + 2x = 0,4 + 0,5 = 0,9 (1)
Mặt khác: 1,25M + 65M = 19 (2)
(1)(2) ⇒ (1,25M +65)/(1,25n + 2) = 19/0,9 ⇒ n = 2; M = 24(Mg)

Đáp án A
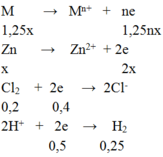
Bảo toàn e ⇒1,25nx + 2x = 0,4 + 0,5 = 0,9 (1)
Mặt khác: 1,25M + 65M = 19 (2)
Từ (1) và (2) ⇒ (1,25M +65M)/(1,25n + 2) = 19/0,9 ⇒ n = 2; M = 24(Mg)

Đáp án B
- Khi cho hỗn hợp tác dụng với H2SO4 loãng dư chỉ có Mg phản ứng sinh ra khí H2 => nMg=nH2=0,15 mol
- Khi cho hỗn hợp tác dụng với HNO3 dư => Chỉ có Cu và Mg (kim loại thay đổi số oxi hóa)
BT e: nCu=(3nNO-2nMg)/2=0,15 mol
=>mCu=0,15.64=9,6 gam

Gọi công thức oxit ban đầu là MxOy.
Có phản ứng khử hoàn toàn oxit MxOy thành kim loại:
![]()
Dẫn khí CO2 sinh ra hấp thụ vào dung dịch Ca(OH)2 dư:
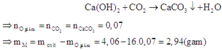
Cần lưu ý: Hóa trị của kim loại M trong oxit ban đầu và hóa trị của M trong sản phẩm của phản ứng giữa M với axit HCl có thể khác nhau.
Do đó ta gọi n là hóa trị của M thể hiện khi phản ứng với axit HCl.
![]()
Áp dụng định luật bào toàn mol electron, ta có:
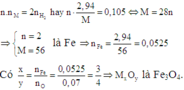
Đáp án D.


Gọi x là số mol của kim loại R:
PTHH: R + 2HCl -----> RCl2 +H2
x mol
=>MR= 4/x đvC (*)
Khi cho hỗn hợp Zn và R vào dd H2SO4:
nH2= 13.44/22.4=0.6 mol
PTHH: R + H2SO4 ---> RSO4+ H2
x x
Zn +H2SO4 ----> ZnSO4 + H2
y y
Kết hwpj với (*) ,ta có hệ pt: \(\left\{{}\begin{matrix}\dfrac{4}{x}+65y=22.2\\x+y=0.6\end{matrix}\right.\)
giải ra : x =0.489432167 ; y = 0.1910567833
mZn=0.1910567833*65= 12.41g
=>mR=22.2-12.41=9.79g
=>MR=9.79/0.489432167 \(\approx\) 24 đvC (Mg)
Vậy kim loại R cần tìm là Mg.
(Số mol tính ra giữ nguyên, chỉ làm tròn ở kết quả cưới cùng để tránh sai số).