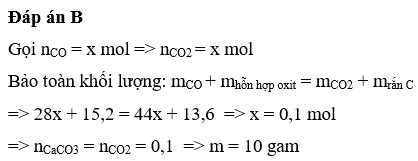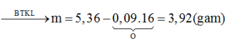Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Bảo toàn KL ; 24 +mCOp/ư +mCOdu =mY+ mco2 +mCodu Suy ra:: 24+mco(pư) =mY +mCO2 ,,,,,mÀ mol CO(pư)=mol CO2 .ta cần tính mol CO2 là ok.
pt: CO2 + 2OH-→ CO32- ( mol BaCO3: 0,15 ,đặt mol(NaCo3)= amol )\(\Rightarrow\)ΣCo32-=015 +a
(0,15+a) \(\leftarrow\) 0,15+a
CO2+ OH-→ HCO32- (mol Ba(hco3)2=0,05 (bảo toàn Ba2+ ) và mol NaHCO3 =0,2-a → ΣHco32-=0,3-a
0,3-a \(\leftarrow\) 0,3-a
ΣCO2= 0,45mol Lắp vào biểu thức trên tính đk : mY=16,8g

Sau khi hỗn hợp X bị CO lấy đi 1 phần oxi ⇒ Chất rắn Y.
+ Đặt nFe/Y = a và nO/Y = b ta có:
PT bảo toàn electron: 3a – 2b = 2nSO2 = 0,09 mol (1)
PT theo muối Fe2(SO4)3: 200a = 18 (2)
+ Giải hệ (1) và (2) ta có: a = b = 0,09 mol
⇒ mY = 0,09×(56+16) = 6,48 gam.
+ Mà nO bị lấy đi bởi CO = nCaCO3 = 0,04 mol
⇒ nX = mY + mO bị lấy đi = 6,48 + 0,04×16 = 7,12 gam
Đáp án B

Đáp án D
Vì CO dư nên hỗn hợp sau phản ứng chỉ gồm kim loại:
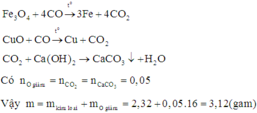

Đáp án C
X + CO tạo thành chất rắn Y gồm các kim loại Mg, Fe, Cu và hỗn hợp khí z gồm CO2 và CO dư
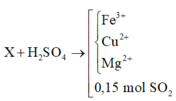
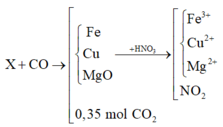
Áp dụng định luật bảo toàn mol electron
Trong thí nghiệm 1: ne nhường = ne nhận = 0,3(mol)
ne nhường trong thí nghiệm = ne nhường (1) + 2.nCO2 =1(mol) = ne nhận (2) = nNO2
Chú ý: Với các bài toán của phản ứng oxi hoá khử gồm nhiều quá trình ta thường sử dụng bảo toàn electron cho toàn bộ các quá trình, bỏ qua giai đoạn trung gian.