Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đặt \(\left\{{}\begin{matrix}n_{Fe}=a\left(mol\right)\\n_{Na}=b\left(mol\right)\end{matrix}\right.\)
PTHH:
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
a--------------------------->a
\(2Na+2HCl\rightarrow2NaCl+H_2\)
b---------------------------->0,5b
Ta có: \(m_M=\dfrac{1}{2}.\left(m_{Fe}+m_{Na}\right)=\dfrac{1}{2}.\left(56a+23b\right)=28a+11,5b\left(g\right)\)
PTHH: \(M+2HCl\rightarrow MCl_2+H_2\)
(a+0,5b)<----------------(a+0,5b)
\(\Rightarrow M_M=\dfrac{28a+11,5b}{a+0,5b}\\ \Rightarrow\dfrac{28a}{a}>M_M>\dfrac{11,5a}{0,5a}\\ \Leftrightarrow28>M_M>23\)
Vậy M là Magie (Mg)

bn check xem khối lượng mol M' bằng 1,793 hay 1,739 khối lượng mol M ?

X gồm \(\left\{{}\begin{matrix}M:a\left(mol\right)\\M_2O_n:b\left(mol\right)\end{matrix}\right.\)
=> a.MM + 2b.MM + 16bn = 8,1 (1)
nHCl = 0,3.1 = 0,3 (mol)
PTHH: 2M + 2nH2O --> 2M(OH)n + nH2
a---------------->a
M2On + nH2O --> 2M(OH)n
b---------------->2b
M(OH)n + nHCl --> MCln + nH2O
\(\dfrac{0,3}{n}\)<---0,3
=> \(a+2b=\dfrac{0,3}{n}\) => an + 2bn = 0,3
(1) => \(\dfrac{0,3}{n}.M_M+16bn=8,1\)
Mà bn < 0,15 => MM > 19n (g/mol)
bn < 0 => MM < 27n (g/mol)
=> 19n < MM < 27n
- Với n = 1 => 19 < MM < 27
Mà M và oxit của nó tan trong nước tạo thành dd kiềm
=> M là Na
- Với n = 2 => 38 < MM < 54
Mà M và oxit của nó tan trong nước tạo thành dd kiềm
=> M là Ca
- Với n = 3 => 57 < MM < 81
Mà M và oxit của nó tan trong nước tạo thành dd kiềm
=> Không có TH thỏa mãn
Vậy \(M\left[{}\begin{matrix}Na\\Ca\end{matrix}\right.\)
TH1: M là Na
Có: \(\left\{{}\begin{matrix}23a+62b=8,1\\a+2b=0,3\end{matrix}\right.\)
=> a = 0,15 (mol); b = 0,075 (mol)
=> \(\left\{{}\begin{matrix}m_{Na}=0,15.23=3,45\left(g\right)\\m_{Na_2O}=0,075.62=4,65\left(g\right)\end{matrix}\right.\)
TH2: M là Ca
Có: \(40a+56b=8,1\) (*)
PTHH: Ca + 2H2O --> Ca(OH)2 + H2
a-------------->a
CaO + H2O --> Ca(OH)2
b--------------->b
Ca(OH)2 + 2HCl --> CaCl2 + 2H2O
0,15<-----0,3
=> a + b = 0,15 (**)
(*)(**) => a = 0,01875 (mol); b = 0,13125 (mol)
=> \(\left\{{}\begin{matrix}m_{Ca}=0,01875.40=0,75\left(g\right)\\m_{CaO}=0,13125.56=7,35\left(g\right)\end{matrix}\right.\)
Mà bn < 0,15 => MM > 19n (g/mol)
bn < 0 => MM < 27n (g/mol)
chỗ này là sao vậy ạ

\(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\\ PTHH:2K+2H_2O\rightarrow2KOH+H_2\uparrow\\ Theo.pt:n_{KOH}=2n_{H_2}=2.0,15=0,3\left(mol\right)\)
\(PTHH:2KOH+H_2SO_4\rightarrow K_2SO_4+2H_2O \\ Mol:0,3\rightarrow0,15\\ V_{ddH_2SO_4}=\dfrac{0,15}{2}=0,075\left(l\right)\)

X + nH2O → X(OH)n + n/2 H2.
Ta có: n(H2) = 0,15 mol
→ n(OH-) = 2n (H2) = 0,3 mol
→ n(H+) = 0,3 mol → 2. 2V = 0,3 → V = 0,075 (lít)

Tham khảo:
a)
M+2HCl→MCl2+H2M+2HCl→MCl2+H2
2N+6HCl→2NCl3+3H22N+6HCl→2NCl3+3H2
nH2=11,222,4=0,5(mol)nH2=11,222,4=0,5(mol)
nHCl=2nH2=1(mol)nHCl=2nH2=1(mol)
Bảo toàn khối lượng :
18,4+1.36,5=m+0,5.2⇒m=53,9(gam)18,4+1.36,5=m+0,5.2⇒m=53,9(gam)
b)
Gọi nN=nM=a(mol)nN=nM=a(mol)
Theo PTHH :
nH2=1,5a+a=0,5⇒a=0,2nH2=1,5a+a=0,5⇒a=0,2
Suy ra :
0,2N + 0,2M = 18,4
⇒N+M=92⇒N+M=92
⇒M=92−N⇒M=92−N
Mà : 2N < M < 3N
⇔2N<92−N<3N⇔2N<92−N<3N
⇔23<N<30,6⇔23<N<30,6
Với N = 27(Al) thì thỏa mãn . Suy ra M = 92 - 27 = 65(Zn)
Vậy 2 kim loại là Al và Zn
Bạn tự thay thành A và B nhé

gọi kim loại hóa trị II là Mpt pứ:M+2HCl−−−>MgCl2+H2Fe+2HCl−−−>FeCl2+H2dd X: MgCl2,FeCl2,HCldưThêm NaOH dư vào X và biết nó không tạo kết tủa với hidroxit nên ta có pt pứFeCL2+2NaOH−−−>Fe(0H)2+2NaCl4Fe(OH)2+02−−−>2Fe203+4H20n Fe203 = 0, 075 moltừ các pt pu --->n H2= n Fe= n FeCl
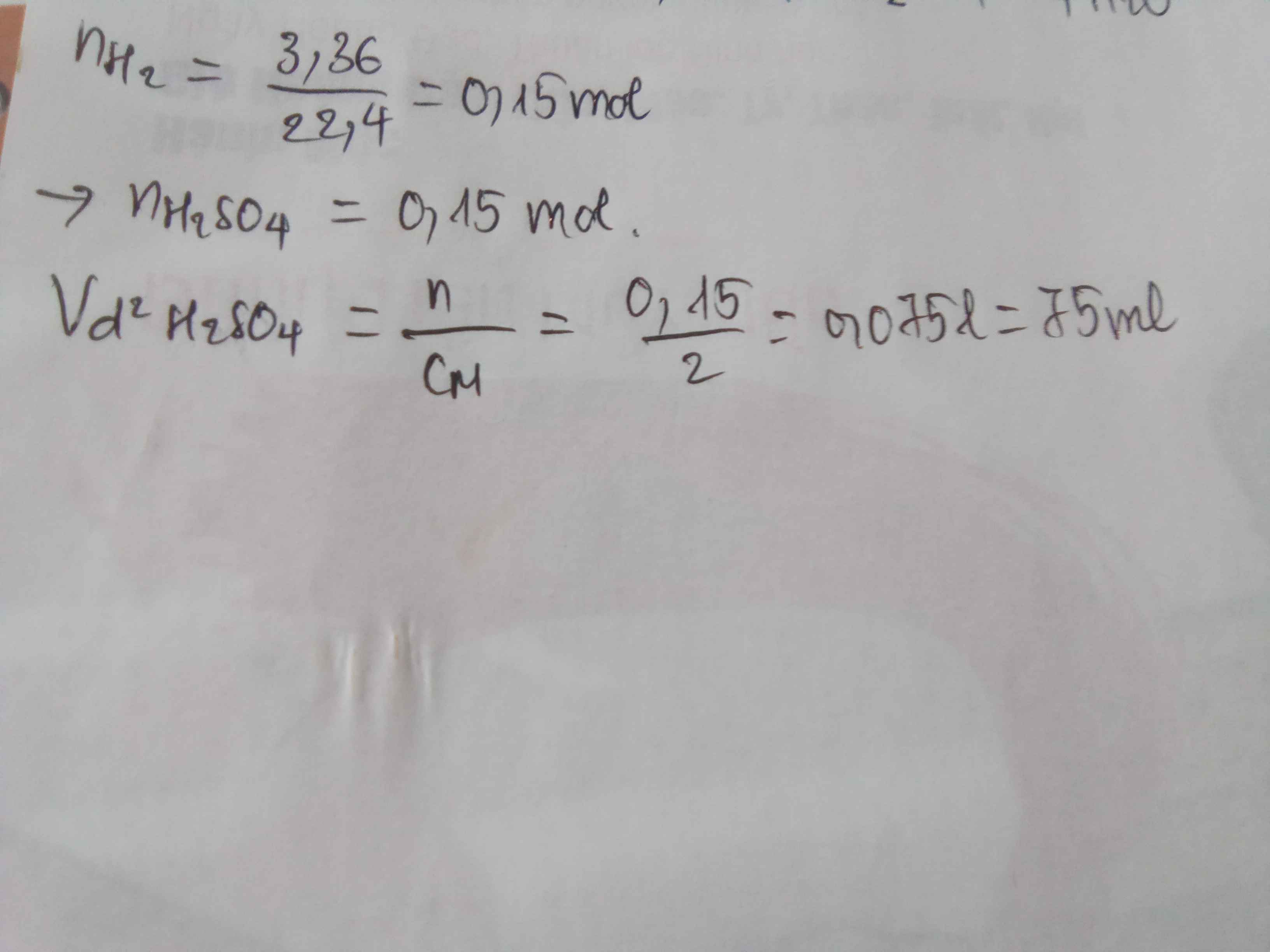
n HCl = 0,8 x 2 = 1,6 mol.
n NaOH trung hòa HCL dư = n HCl dư = 0,6 x 1 = 0,6 mol
--> n HCl phản ứng hết với hỗn hợp X = 1,6 - 0.6 = 1 mol.
n H2 = 4,48/22,4 = 0,2 mol
--> n H2O = n[O] có trong X = 0,3 mol nặng 4,8 gam.
--> m kim loại M = 27,2 - 4,8 = 22,4 gam
Vì kim loại có hai hóa trị là 2 và 3 nên khi phản ứng với HCl, kim loại chỉ có thể tạo muối clorua II và n M = n H2 = 0,2 mol.
Trường hợp 1. kim loại có hóa trị 2 trong oxit.
--> n M = n [O] = 0,3 mol --> tổng mol nguyên tố M trong X = 0,3 + 0,2 = 0,5 và NTK của kim loại = 22,4/0,5 = 44.8 (loại)
Trường hợp 2. Kim loại có hóa trị 3 trong oxit.
--> n M = 2/3 n [O] = 0,2 mol --> tổng mol nguyên tố M trong X = 0,2 + 0,2 = 0,4 và NTK của kim loại = 22,4/0,7 = 56.
--> M là Fe và oxit là Fe2O3 với khối lượng Fe = 0,2 x 56 = 11,2 gam và m Fe2O3 = 0,1 x 160 = 16 gam