Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Do X + Cu => sinh khí NO => X chứa ![]()
Quy H về Fe, S, O, C O 2 => Ta có sơ đồ phản ứng sau:
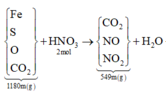
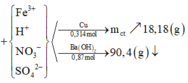
Đặt![]()
![]()
mchất tan giảm = ![]()
=> 18,18 = 10,16 - 30.0,25x - 18.0,5x => x = 0,12 mol
![]()
Bảo toàn e: ![]()
![]()
![]()
![]()
Bảo toàng điện tích trong X: ![]()
Bảo toàn nguyên tố Hidro: ![]()
Bảo toàn khối lượng ![]() => x = 0,04
=> x = 0,04
Đặt ![]()
![]()
nnguyên tố Oxi = ![]() = a + 2b
= a + 2b
giải hệ có a=0,56mol; b=0,08mol
bảo toàn nguyên tố Oxi: ![]()
bảo toàn nguyên tố Nito: ![]()
![]()
![]()
![]()

Do Y tác dụng AgNO3 sinh ra NO ⇒ trong Y có chứa H+ và NO3– hết.
4H+ + NO3– + 3e → NO + 2H2O ⇒ ở phản ứng đầu, nH+ = 0,4 – 0,02 × 4 = 0,32 mol.
⇒ nNO3– = 0,32 ÷ 4 = 0,08 mol ⇒ nFe(NO3)2 = 0,04 mol.
Đặt nFeCl2 = x mol; nCu = y mol. mX = 127x + 64y + 0,04 × 180 = 23,76 gam.
Bảo toàn nguyên tố Clo : nAgCl = 2x + 0,4 mol.
Bảo toàn nguyên tố Ag : nAg = 0,58 – (2x + 0,4) = 0,18 – 2x mol.
Bảo toàn electron cả quá trình : nFeCl2 + 2nCu + nFe(NO3)2 = nAg + 3/4nH+.
⇒ x + 2y + 0,04 = 0,18 – 2x + 3/4 × 0,4 ⇒ giải: x = 0,08 mol; y = 0,1 mol.
⇒ nAg = 0,02 mol; nAgCl = 0,56 mol ⇒ m = 0,02 × 108 + 0,56 × 143,5 = 82,52
Đáp án A

Đáp án A
Do X + Cu sinh ra khí NO=> chứa H + , N O - 3 chỉ chứa F e +
Quy H về Fe,S,O,C O 2 => Ta có sơ đồ phản ứng sau:
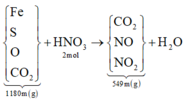
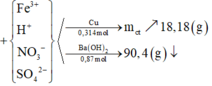
Đặt ![]()
![]()
=> mchất tan giảm ![]()
![]()
![]()
Bảo toàn e:
![]()
![]()
![]()
Bảo toàng điện tích trong X:
![]()
Bảo toàn nguyên tố Hidro:
![]()
Bảo toàn khối lượng
![]()
Đặt ![]()
![]()
nnguyên tố Oxi
![]()
giải hệ có a=0,56mol; b=0,08mol
bảo toàn nguyên tố Oxi:
![]()
bảo toàn nguyên tố Nito:
![]()
![]()
![]() x 100 = 29,33%
x 100 = 29,33%

Đáp án D
Đặt số mol của FeO, Fe3O4 và Cu lần lượt là a, b, c
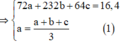
Dung dịch Y chỉ chứa các muối clorua => NO 3 - phản ứng hết.
X + HCl → 3 muối: CuCl2, FeCl2, FeCl3.
Có m muối = 135 c + 127 . ( a + b + 2 x ) + 162 , 5 . ( 2 b - 2 c ) = 29 , 6 ( 2 )

Gần nhất với giá trị 180,15

Đáp án D
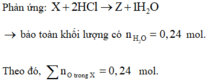
Lại thêm m x = 16 , 4 gam và số mol FeO bằng 1/3 tổng số mol của X nên ta có đủ giả thiết để giải ra hệ số mol FeO là 0,04 mol; Fe3O4 là 0,05 mol và Cu là 0,03 mol.
« Dạng bài tập Ag, Cl, Fe đặc trưng || → gộp sơ đồ và xem xét cả quá trình:
« Giải thích:
1. Gộp Y + Z nên lượng Fe, Cu, O dùng là gấp đôi.
2. NaNO3 bỏ ra khỏi sơ đồ vì lượng tham gia và cuối cùng thu được như nhau.
Ta có: n H 2 O = n O trong oxit + 2 n NO (theo ghép cụm) rồi suy ra số mol HCl.
Hay nhanh hơn ta dùng bảo toàn electron:

Tiếp tục, bảo toàn điện tích tính ∑ n NO 3 - rồi cộng với số mol NO → theo bảo toàn N có 1,3 mol AgNO3.
Vậy, yêu cầu khối lượng kết tủa:
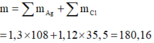

Đáp án D
♦ phản ứng X + 2HCl → Z + 1H2O ||→ BTKL có nH2O = 0,24 mol.
||→ nO trong X = 0,24 mol. Lại thêm mX = 16,4 gam và nFeO = 1/3nX
||→ đủ giả thiết để giải ra: nFeO = 0,04 mol; nFe3O4 = 0,05 mol và nCu = 0,03 mol.
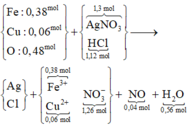
Dạng Ag, Cl, Fe đặc trưng ||→ gộp sơ đồ + xem xét cả quá trình:
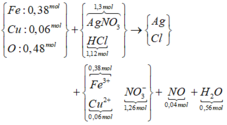
Giải thích: gộp Y + Z nên lượng Fe, Cu, O dùng là gấp đôi. NaNO3 bỏ ra khỏi sơ đồ vì đầu cuối như nhau.
nH2O = nO trong oxit + 2nNO (theo ghép cụm). hoặc nhanh hơn dùng bảo toàn electron mở rộng:
có ∑nH+ = 2nO trong oxit + 4nNO = 1,12 mol → ∑nCl = 1,12 mol.
bảo toàn điện tích tính ∑nNO3– rồi cộng NO theo bảo toàn N có 1,3 mol Ag
||→ yêu cầu mkết tủa = mAg + mCl = 180,16 gam


Đáp án A