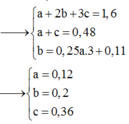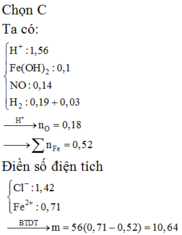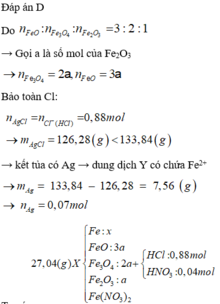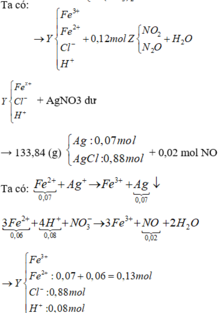Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Quy đổi hỗn hợp tương đương với hỗn hợp gồm a mol Fe, b mol OH và c mol O.
Khí Z gồm H2 và NO.
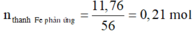
Dung dịch cuối cùng chứa Fe2+, Na+, S O 2 - 4
![]()
=> a = 0,27
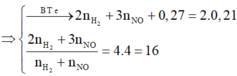

Đáp án C
Phân tích kết tủa:
0,88 mol Cl → 0,88 mol AgCl → 133,84 gam kết tủa còn 0,07 mol Ag nữa.
AgNO3 + dung dịch Y → 0,02 mol NO chứng tỏ trong Y chứa 0,08 mol H+.
Thêm nữa, kết tủa có Ag → chứng tỏ trong Y có Fe2+ → Y không chứa NO 3 - .
Rõ hơn quan sát sơ đồ:
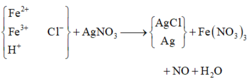
Theo đó, bảo toàn Ag có 0,95 mol AgNO3 → có 0,31 mol Fe(NO3)3.
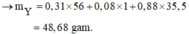
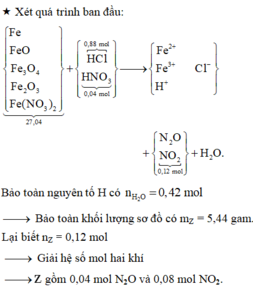
→ Bảo toàn nguyên tố N có số mol Fe(NO3)2 trong X là 0,06 mol.
Nhìn 27,04 gam X gồm 0,31 mol Fe + 0,12 mol NO3 + ? mol O → ? = 0,14 mol.
Lại có tỉ lệ FeO : Fe3O4 : Fe2O3 = 3:2:1
→ viết gộp cụm: 3FeO.2Fe3O4.1Fe2O3 = Fe11O14.
→ từ 0,14 mol O suy ra có 0,01 mol Fe11O14.
→ đọc ra có 0,03 mol FeO + 0,02 mol Fe3O4 + 0,01 mol Fe2O3.
→ nFe có trong X ban đầu = 0,31 - 0,11 - 0,06 = 0,14 mol
→ yêu cầu %nFe có trong hỗn hợp X
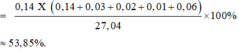

Dung dịch Y chứa Fe3+ (a); Fe2+ (b), Cl- (0,88) và nH+ dư = 4nNO = 0,88 (mol)
Bảo toàn điện tích: 3a + 2b + 0,08 = 0,88 (1)
nAgCl = 0,88 => nAg = 0,07 (mol)
Bảo toàn electron: b = 0,03.2 + 0,07 (2)
Từ (1) và (2) => a = 0,18 và b = 0,13 (mol)
Quy đổi hỗn hợp thành Fe ( 0,31 mol) ; O ( u mol) và NO3- ( v mol). Trong Z, đặt nN2O = x => nNO2 = 0,2 – x (mol)
=> 0,31.56 + 16u + 62v = 27,04 (3)
Bảo toàn nguyên tố N:
v + 0,04 = 2x + (0,12 –x) (4)
nH+ pư = 0,88 + 0,04 – 0,08 = 0,84
=> 10x + 2( 0,12 –x) + 2u = 0,84 (5)
Từ (3), (4), (5) => u = 0,14 ; v = 0,12 ; x = 0,04
nFe(NO3)2 = v/2 = 0,06 (mol)
Đặt k, 3h, 2h, h lần lượt là số mol Fe, FeO, Fe3O4, Fe2O3
Bảo toàn Fe: => 0,06 + k + 11h = 0,31 (6)
Bảo toàn O : => 14h = u = 0,14 (7)
Từ (6) và (7) => k = 0,14 (mol); h = 0,01 (mol)
Số mol hỗn hợp = 0,06 + k + 6h = 0,26
=> %nFe = 0,14/0,26 = 53,85%
Gần nhất với 54%
Đáp án A

Đáp án C
![]()
![]()
Ta có sơ đồ phản ứng:
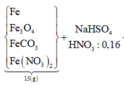
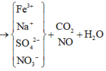
![]()
Bảo toàn e: ![]()
Xét ![]()
![]()
Bảo toàn gốc ![]()
![]()
Bảo toàn điện tích: ![]()
Bảo toàn nguyên tố Hidro: ![]()
Bảo toàn khối lượng: m Z = 4 , 92 ( g ) => dễ giả ra được 0,03 mol C O 2 ; 0,12 mol NO
Bảo toàn nguyên tố Nito:
![]() = 0,03 mol
= 0,03 mol
![]()
![]()
Bảo toàn nguyên tố Fe: ![]()
![]()

Đáp án C
Phân tích: dung dịch Y + Cu → sản phẩm có NO nên Y chứa H+ và NO 3 - → muối sắt chỉ có Fe3+.
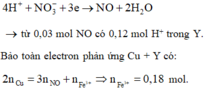
Xử lí Ba(OH)2 + Y: 154,4 gam kết tủa gồm 0,18 mol Fe(OH)3 và ? mol BaSO4 → ? = 0,58 mol.
« Sơ đồ phản ứng chính:

Bảo toàn electron hoặc bảo toàn nguyên tố O (nhớ ghép bỏ cụm) → có 0,01 mol Fe3O4.
Theo đó, bảo toàn nguyên tố Fe có 0,1 mol Fe đơn chất trong X
![]()

Chọn đáp án C
- Dung dịch Y gồm Fe3+, H+, Na+, N O 3 - v à S O 4 2 - (dung dịch Y không chứa Fe2+, vì không tồn tại dung dịch cùng chứa Fe2+, H+ và N O 3 - ).
- Khi cho dung dịch Y tác dụng với 0,135 mol Cu thì:
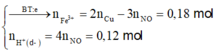
- Khi cho dung dịch Y tác dụng với Ba(OH)2 ta có:

- Xét dung dịch Y, có: ![]()
= 0,08 mol
![]()
![]()
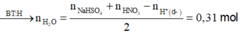
- Xét hỗn hợp khí Z, có n C O 2 = x m o l và n N O = 4x mol. Mặt khác:
![]()
![]()
=> 44x + 3x.30 = 4,92 (g) => x = 0,3 mol
- Quay trở lại hỗn hợp rắn X, ta có:
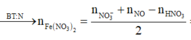
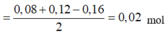
![]()
mà 
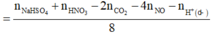
= 0,01 mol
![]()
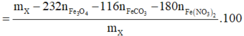
= 37,33%