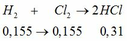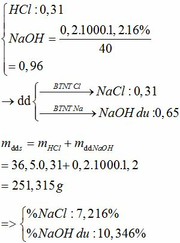Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Gọi số mol Ca, CaCO3 là a, b (mol)
=> 40a + 100b = 2,8 (1)
\(n_{khí}=\dfrac{0,896}{22,4}=0,04\left(mol\right)\)
PTHH: Ca + 2HCl --> CaCl2 + H2
a-------------->a------>a
CaCO3 + 2HCl --> CaCl2 + CO2 + H2O
b------------------>b------->b
=> a + b = 0,04 (2)
(1)(2) => a = 0,02 (mol); b = 0,02 (mol)
\(n_{CaCl_2}=a+b=0,04\left(mol\right)\)
=> m = 0,04.111 = 4,44 (g)
\(\left\{{}\begin{matrix}m_{Ca}=0,02.40=0,8\left(g\right)\\m_{CaCO_3}=0,02.100=2\left(g\right)\end{matrix}\right.\)
b)
\(\overline{M}_X=\dfrac{0,02.2+0,02.44}{0,02+0,02}=23\left(g/mol\right)\)
=> \(d_{X/H_2}=\dfrac{23}{2}=11,5\)
c)
nNaOH = 0,1.0,2 = 0,02 (mol)
Xét tỉ lệ: \(\dfrac{n_{NaOH}}{n_{CO_2}}=\dfrac{0,02}{0,02}=1\) => Tạo muối NaHCO3
PTHH: NaOH + CO2 --> NaHCO3
0,02------------>0,02
=> mNaHCO3 = 0,02.84 = 1,68 (g)

a)
Gọi số mol MgSO3, MgCO3 là a, b (mol)
=> 104a + 84b = 1,88 (1)
\(n_{khí}=\dfrac{0,448}{22,4}=0,02\left(mol\right)\)
PTHH: MgSO3 + 2HCl --> MgCl2 + SO2 + H2O
a----------------->a-------->a
MgCO3 + 2HCl --> MgCl2 + CO2 + H2O
b------------------>b-------->b
=> a + b = 0,02 (2)
(1)(2) => a = 0,01 (mol); b = 0,01 (mol)
=> \(\left\{{}\begin{matrix}m_{MgSO_3}=0,01.104=1,04\left(g\right)\\m_{MgCO_3}=0,01.84=0,84\left(g\right)\end{matrix}\right.\)
nMgCl2 = 0,02 (mol)
=> m = 0,02.95 = 1,9 (g)
b)
\(\left\{{}\begin{matrix}n_{SO_2}=0,01\left(mol\right)\\n_{CO_2}=0,01\left(mol\right)\end{matrix}\right.\)
nKOH = 0,25.0,3 = 0,075 (mol)
Xét tỉ lệ: \(\dfrac{n_{KOH}}{n_{CO_2}+n_{SO_2}}=\dfrac{0,075}{0,01+0,01}=3,75\) => Tạo ra muối K2CO3 và K2SO3
PTHH: 2KOH + CO2 --> K2CO3 + H2O
0,01---->0,01
2KOH + SO2 --> K2SO3 + H2O
0,01---->0,01
=> \(\left\{{}\begin{matrix}m_{K_2CO_3}=0,01.138=1,38\left(g\right)\\m_{K_2SO_3}=0,01.158=1,58\left(g\right)\end{matrix}\right.\)

448cm3 = 0,448 l
(1) CaO + 2HCl \(\rightarrow\) CaCl2 + H2O
(2) CaCO3 + 2HCl \(\rightarrow\) CaCl2 + H2O + CO2
a) Theo (2) \(\rightarrow\) n\(CaCO_3\) = n\(CO_2\) = \(\dfrac{0,448}{22,4}\) = 0,02 (mol)
\(\rightarrow\) m\(CaCO_3\) = 0,02 . 100 = 20 (g)
m\(CaCl_2\) (2)= 0,02 . 111 = 2,22 (g)
\(\rightarrow\) m\(CaCl_2\) (1) = 3,33 - 2,22 = 1,11 (g)
Theo (1) \(\rightarrow\) nCaO = n\(CaCl_2\) (1) = \(\dfrac{1,11}{111}\) = 0,01 (mol)
\(\rightarrow\) mCaO = 0,01 . 56 = 0,56 (g)
b)
(3) 2NaOH + CO2 \(\rightarrow\) Na2CO3 + H2O
(4) NaOH + CO2 \(\rightarrow\) NaHCO3
Ta có : \(\dfrac{n_NaOH}{n_CO_2}\) = \(\dfrac{0,025}{0,02}\) = 1,25
1< 1,25 < 2 \(\rightarrow\) tạo hỗn hợp 2 muối
Gọi số mol NaOH p1,p2 là x, y mol
Lập hệ theo số mol NaOH và số mol CO2
x + y = 0,025 (mol)
x/2 + y =0,02 (mol)
Giải hệ tìm được x= 0,01 mol, y= 0,015 mol
mmuối = 0,01 . 106 + 0,015 . 84 = 2,32 (g)
Ciao_

Gọi\(\left\{{}\begin{matrix}n_{Fe}=a\left(mol\right)\\n_{FeS}=b\left(mol\right)\end{matrix}\right.\)
mH2SO4 = 150.9,8% = 14,7 (g)
-> nH2SO4 = \(\dfrac{14,7}{98}=0,15\left(mol\right)\)
\(n_{hhkhí\left(H_2,H_2S\right)}=\dfrac{\dfrac{224}{1000}}{22,4}=0,01\left(mol\right)\)
PTHH:
Fe + H2SO4 ---> FeSO4 + H2
a a a a
FeS + H2SO4 ---> FeSO4 + H2S
b b b b
Hệ phương trình\(\left\{{}\begin{matrix}56a+88b=0,72\\a+b=0,01\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,005\left(mol\right)\\b=0,005\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}m_{Fe}=0,005.56=0,28\left(g\right)\\m_{FeS}=0,005.88=0,44\left(g\right)\end{matrix}\right.\)
\(n_{H_2SO_4\left(pư\right)}=0,005+0,005=0,01\left(mol\right)\\ \Rightarrow n_{H_2SO_4\left(dư\right)}=0,15-0,01=0,14\left(mol\right)\\ m_{ddY}=0,72+150-0,005.2+0,005.34=150,88\left(g\right)\)
=> \(\left\{{}\begin{matrix}C\%_{FeSO_4}=\dfrac{152.\left(0,005+0,005\right)}{150,88}=1\%\\C\%_{H_2SO_4}=\dfrac{98.0,14}{150,88}=9,1\%\end{matrix}\right.\)

a)
\(n_{HCl\left(bđ\right)}=\dfrac{250.7,3\%}{36,5}=0,5\left(mol\right)\)
\(n_{khí}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: Zn + 2HCl --> ZnCl2 + H2
ZnS + 2HCl --> ZnCl2 + H2S
Do nHCl(bđ) > 2.nkhí => HCl dư
Gọi số mol Zn, ZnS là a, b (mol)
=> 65a + 97b = 8,1 (1)
\(n_{khí}=n_{H_2}+n_{H_2S}=a+b=0,1\) (2)
(1)(2) => a = 0,05 (mol); b = 0,05 (mol)
\(\left\{{}\begin{matrix}m_{Zn}=0,05.65=3,25\left(g\right)\\m_{ZnS}=0,05.97=4,85\left(g\right)\end{matrix}\right.\)
nZnCl2 = 0,1 (mol) => mZnCl2 = 0,1.136 = 13,6 (g)
nHCl(dư) = 0,5 - 0,2 = 0,3 (mol) => mHCl = 0,3.36,5 = 10,95 (g)
mdd sau pư = 8,1 + 250 - 0,05.2 - 0,05.34 = 256,3 (g)
\(\left\{{}\begin{matrix}C\%_{ZnCl_2}=\dfrac{13,6}{256,3}.100\%=5,3\%\\C\%_{HCl\left(dư\right)}=\dfrac{10,95}{256,3}.100\%=4,3\%\end{matrix}\right.\)
b) \(\overline{M}_X=\dfrac{0,05.2+0,05.34}{0,05+0,05}=18\left(g/mol\right)\)
=> \(d_{X/H_2}=\dfrac{18}{2}=9\)

a)
\(n_{HCl}=\dfrac{300.7,3\%}{36,5}=0,6\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
FeCO3 + 2HCl --> FeCl2 + CO2 + H2O
\(n_{khí}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Theo PTHH, nHCl(pư) = 2.nkhí = 0,2 (mol) < 0,6 (mol)
=> HCl dư
Gọi số mol Fe, FeCO3 là a, b (mol)
=> \(\left\{{}\begin{matrix}56a+116b=8,6\\a+b=0,1\end{matrix}\right.\)
=> a = 0,05 (mol); b = 0,05 (mol)
=> \(\left\{{}\begin{matrix}m_{Fe}=0,05.56=2,8\left(g\right)\\m_{FeCO_3}=0,05.116=5,8\left(g\right)\end{matrix}\right.\)
nFeCl2 = 0,1 (mol) => mFeCl2 = 0,1.127 = 12,7 (g)
nHCl(dư) = 0,6 - 0,2 = 0,4 (mol) => mHCl(dư) = 0,4.36,5 = 14,6 (g)
mdd sau pư = 8,6 + 300 - 0,05.2 - 0,05.44 = 306,3 (g)
\(\left\{{}\begin{matrix}C\%_{FeCl_2}=\dfrac{12,7}{306,3}.100\%=4,146\%\\C\%_{HCl\left(dư\right)}=\dfrac{14,6}{306,3}.100\%=4,767\%\end{matrix}\right.\)
b)
\(\overline{M}_X=\dfrac{0,05.2+0,05.44}{0,05+0,05}=23\left(g/mol\right)\)
=> \(d_{X/H_2}=\dfrac{23}{2}=11,5\)

n HCl = 360 x 18,25/(100x36,5) = 1,8 mol
H 2 + CuO → t ° Cu + H 2 O
n CuO = x
Theo đề bài
m CuO (dư) + m Cu = m CuO (dư) + m Cu p / u - 3,2
m Cu = m Cu p / u - 3,2 => 64x = 80x - 3,2
=> x= 0,2 mol → m H 2 = 0,4g
Fe + 2HCl → FeCl 2 + H 2
Số mol HCl tác dụng với Fe 3 O 4 , Fe 2 O 3 , FeO là 1,8 - 0,4 = 1,4 mol
Phương trình hóa học của phản ứng:
Fe 3 O 4 + 8HCl → 2 FeCl 3 + FeCl 2 + 4 H 2 O (1)
Fe 2 O 3 + 6HCl → 2 FeCl 3 + 3 H 2 O (2)
FeO + 2HCl → FeCl 2 + H 2 O (3)
Qua các phản ứng (1), (2), (3) ta nhận thấy n H 2 O = 1/2 n HCl = 1,4:2 = 0,7 mol
Áp dụng định luật bảo toàn khối lượng, ta có:
m hỗn hợp + m HCl = m muối + m H 2 O + m H 2
57,6 + 1,8 x 36,5 = m muối + 0,7 x 18 +0,4
m muối = 57,6 + 65,7 - 12,6 - 0,4 = 110,3 (gam)

\(n_{HCl}=0,8.0,5=0,4\left(mol\right);n_{H_2SO_4}=0,8.0,75=0,6\left(mol\right)\)
=> \(n_{Cl^-}=0,4\left(mol\right);n_{SO_4^{2-}}=0,6\left(mol\right)\)
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Bảo toàn nguyên tố H:
\(n_{HCl}.1+n_{H_2SO_4}.2=n_{H_2}.2+n_{H_2O}.2\)
\(\Leftrightarrow0,4.1+0,6.2=0,2.2+n_{H_2O}.2\)
=>\(n_{H_2O}=0,6\left(mol\right)\)
=> \(n_O=0,6\left(mol\right)\)
\(m_{muối}=m_{kimloai}+m_{Cl^-}+m_{SO_4^{2-}}\)
=>\(m_{kimloai}=88,7-35,5.0,4-0,6.96=16,9\left(g\right)\)
=> \(m=m_{kimloai}+m_O=16,9+0,6.16=26,5\left(g\right)\)

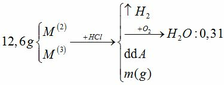
Đồng nhất dữ kiện để thuận lợi cho tính toán, bằng cách nhân đôi khối lượng H2O.
a.
BTNT H: nH2 = nH2O = 0,31 mol
=> nHCl = 0,62mol
BTKL: m kim loại + mHCl = mA + mB => 12,6 + 36,5 . 0,62 = m + 2 . 0,31 => m = 34,61g
b.