Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(CaCO_3+ HCl → CaCl_2+H_2O +CO_2\)
\(n_{CaCO_3}=\dfrac{10}{40+12+16.3}=0,1(mol)\)
\(n_{HCl}=\dfrac{146}{1+35,5}=4(mol)\)
\(\Rightarrow n_{HCl_{dư}}=4-0,1=3,9(mol) ; n_{CaCl_2}=0,1(mol)\\\Rightarrow m_{\text{chất tan}} = m_{HCl_{dư}}+m_{CaCl_2}\\=0,39.(35,5+1)+0,1(40+35,5.2)=25,335(g)\)
Vậy...

a) PTHH :\(Mg+2HCl-->MgCl_2+H_2\) (1)
\(Fe+2HCl-->FeCl_2+H_2\) (2)
b) \(n_{HCl}=\dfrac{600\cdot3,65}{100\cdot36,5}=0,6\left(mol\right)\)
Đặt \(\left\{{}\begin{matrix}n_{Mg}=x\left(mol\right)\\n_{Fe}=y\left(mol\right)\end{matrix}\right.\) => 24x + 56y = 13,6 (*)
Theo PTHH (1) và (2) : \(\Sigma n_{HCl}=2n_{Mg}+2n_{Fe}\)
=> \(0,6=2x+2y\) (**)
Từ (*) và (**) suy ra : \(\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
=> \(\Rightarrow\left\{{}\begin{matrix}\%m_{Mg}=\dfrac{0,1\cdot24}{0,1\cdot24+0,2\cdot56}\cdot100\%\approx17,65\%\\\%m_{Fe}=100\%-17,65\%=82,35\%\end{matrix}\right.\)
c) Theo PTHH (1) và (2) :
\(n_{MgCl_2}=n_{Mg}=0,1\left(mol\right)\)
\(n_{FeCl_2}=n_{Fe}=0,2\left(mol\right)\)
Theo ĐLBTKL :
\(m_A+m_{ddHCl}=m_{dd.spu}\)
=> 13,6 + 600 = m(dd.spu)
=> m(dd.spu) = 613,6 (g)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{MgCl_2}=\dfrac{0,1\cdot95}{613,6}\cdot100\%\approx1,55\%\\C\%_{FeCl_2}=\dfrac{0,2\cdot127}{613,6}\cdot100\%\approx4,14\%\end{matrix}\right.\)

\(n_{HCl}=\dfrac{44,8}{22,4}=2\)
\(\Rightarrow m_{HCl}=2.36,5=73g\)
=> \(C\%_{HCl}=\dfrac{73}{73+327}\times100\%=18,25\%\)
b.
\(n_{HCl}=\dfrac{250.18,25\%}{36,5}=1,25mol\)
\(n_{CaCO_3}=\dfrac{50}{100}=0,5mol\)
\(CaCO_3+2HCl\rightarrow CaCl_2+CO_2+H_2O\)
\(n_{CaCl_2}=n_{CO_2}=0,5mol\)
\(n_{HClpu}=0,5.2=1mol\)
\(\Rightarrow n_{HCldu}=1,25-1=0,25\)
\(\Rightarrow m_{ddpu}=50+250-0,5.44=278g\)
\(C\%_{HCl}=\dfrac{0,25.36,5}{278}.100\%=3,28\%\)
\(C\%_{CaCl_2}=\dfrac{0,5.111}{278}.100\%=19,96\%\)

Bài 4 :
\(n_{MgO}=\dfrac{4}{40}=0,1\left(mol\right)\)
300ml = 0,3l
\(n_{HCl}=1.0,3=0,3\left(mol\right)\)
1) Pt : \(MgO+2HCl\rightarrow MgCl_2+H_2O|\)
1 2 1 1
0,1 0,3 0,1
2) Lập tỉ số so sánh : \(\dfrac{0,1}{1}< \dfrac{0,3}{2}\)
⇒ MgO phản ứng hết , HCl dư
⇒ Tính toán dựa vào số mol của MgO
\(n_{MgCl2}=\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
⇒ \(m_{MgCl2}=0,1.95=9,5\left(g\right)\)
\(n_{HCl\left(dư\right)}=0,3-\left(0,1.2\right)=0,1\left(mol\right)\)
⇒ \(m_{HCl\left(dư\right)}=0,1.36,5=3,65\left(g\right)\)
\(m_{ddHCl}=1,14.300=342\left(g\right)\)
\(m_{ddspu}=4+342=346\left(g\right)\)
\(C_{MgCl2}=\dfrac{9,5.100}{346}=2,75\)0/0
\(C_{HCl\left(dư\right)}=\dfrac{3,65.100}{346}=1,05\)0/0
Chúc bạn học tốt

nCuO=2,4/80=0,03(mol)
m(H2SO4)=29,4%.100=29,4(g) -> nH2SO4=29,4/98=0,3(mol)
a) PTHH: CuO + H2SO4 -> CuSO4 + H2O
Ta có: 0,03/1 < 0,3/1
b)=> CuO hết, H2SO4 dư => Tính theo nCuO
nH2SO4(p.ứ)=nCuSO4=nCuO=0,03(mol)
=>nH2SO4(dư)=0,3-0,03=0,27(mol)
=>mH2SO4(dư)=0,27. 98= 26,46(g)
b) mCuSO4=0,03.160= 4,8(g)
mddsau= 2,4+ 100=102,4(g)
C%ddCuSO4= (4,8/102,4).100=4,6875%
C%ddH2SO4(dư)= (26,46/102,4).100= 25,84%
Số mol của đồng (II) oxit
nCuO = \(\dfrac{m_{CuO}}{M_{CuO}}=\dfrac{2,4}{80}=0,03\left(mol\right)\)
Khối lượng của axit sunfuric
C0/0H2SO4 = \(\dfrac{m_{ct}.100}{m_{dd}}\Rightarrow m_{ct}=\dfrac{C.m_{dd}}{100}=\dfrac{29,4.100}{100}=29,4\left(g\right)\)
Số mol của axit sunfuric
nH2SO4 = \(\dfrac{m_{H2SO4}}{M_{H2SO4}}=\dfrac{29,4}{98}=0,3\left(mol\right)\)
a) Pt : CuO + H2SO4 → CuSO4 + H2O\(|\)
1 1 1 1
0,03 0,3 0,03
b) Lập tỉ số so sánh : \(\dfrac{0,03}{1}< \dfrac{0,3}{1}\)
⇒ CuO phản ứng hết , H2SO4 dư
⇒ Tính toán dựa vào số mol của CuO
Số mol dư của axit sunfuric
ndư = nban đầu - nmol
= 0,3 - (0,03 . 1)
= 0,27 (mol)
Khối lượng dư của axit sunfuric
mdư = ndư . MH2SO4
= 0,27 . 98
= 26,46 (g)
c) Số mol của đồng (II) sunfat
nCuSO4 = \(\dfrac{0,03.1}{1}=0,03\left(mol\right)\)
Khối lượng của đồng (II) sunfat
mCuSO4 = nCuSO4 . MCuSO4
= 0,03 . 160
= 4,8 (g)
Khối lượng của dung dịch sau phản ứng
mdung dịch sau phản ứng = mCuO + mH2SO4
= 2,4 + 100
= 102,4 (g)
Nồng độ phần trăm của đồng (II) sunfat
C0/0CuSO4= \(\dfrac{m_{ct}.100}{m_{dd}}=\dfrac{4,8.100}{102,4}=4,6875\)0/0
Nồng độ phần trăm của axit sunfuric
C0/0H2SO4 = \(\dfrac{m_{ct}.100}{m_{dd}}=\dfrac{26,46.100}{102,4}=25,84\)0/0
Chúc bạn học tốt

\(n_{FeO}=\dfrac{14,4}{72}=0,2\left(mol\right)\)
\(m_{ct}=\dfrac{10,95.200}{100}=21,9\left(g\right)\)
\(n_{HCl}=\dfrac{21,9}{36,5}=0,6\left(mol\right)\)
Pt : \(FeO+2HCl\rightarrow FeCl_2+H_2O|\)
1 2 1 1
0,2 0,6 0,2
a) Lập tỉ số so sánh : \(\dfrac{0,2}{1}< \dfrac{0,6}{2}\)
⇒ FeO phản ứng hết , HCl dư
⇒ Tính toán dựa vào số mol của FeO
\(n_{HCl\left(dư\right)}=0,6-\left(0,2.2\right)=0,2\left(mol\right)\)
⇒ \(m_{HCl\left(dư\right)}=0,2.36,5=7,3\left(g\right)\)
b) \(n_{FeCl2}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
⇒ \(m_{FeCl2}=0,2.127=25,4\left(g\right)\)
\(m_{ddspu}=14,4+200=214,4\left(g\right)\)
\(C_{FeCl2}=\dfrac{25,4.100}{214,4}=11,85\)0/0
\(C_{HCl\left(dư\right)}=\dfrac{7,3.100}{214,4}=3,4\)0/0
Chúc bạn học tốt

Bài 4 :
\(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
a) Pt : \(Zn+2HCl\rightarrow ZnCl_2+H_2|\)
1 2 1 1
0,2 0,4 0,2 0,2
b) \(n_{H2}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
\(V_{H2\left(dktc\right)}=0,2.22,4=4,48\left(l\right)\)
c) \(n_{HCl}=\dfrac{0,2.2}{1}=0,4\left(mol\right)\)
⇒ \(m_{HCl}=0,4.36,5=14,6\left(g\right)\)
\(C_{ddHCl}=\dfrac{14,6.100}{100}=14,6\)0/0
d) \(n_{ZnCl2}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
⇒ \(m_{ZnCl2}=0,2.136=27,2\left(g\right)\)
\(m_{ddspu}=13+100-\left(0,2.2\right)=112,6\left(g\right)\)
\(C_{ZnCl2}=\dfrac{27,2.100}{112,6}=24,16\)0/0
Chúc bạn học tốt
Bài 3 :
\(n_{Mg}=\dfrac{12}{24}=0,5\left(mol\right)\)
a) Pt : \(Mg+H_2SO_4\rightarrow MgSO_4+H_2|\)
1 1 1 1
0,5 0,5 0,5 0,5
b) \(n_{H2}=\dfrac{0,5.1}{1}=0,5\left(mol\right)\)
\(V_{H2\left(dktc\right)}=0,5.22,4=11,2\left(l\right)\)
c) \(n_{H2SO4}=\dfrac{0,5.1}{1}=0,5\left(mol\right)\)
⇒ \(m_{H2SO4}=0,5.98=49\left(g\right)\)
\(C_{ddH2SO4}=\dfrac{49.100}{200}=24,5\)0/0
d) \(n_{MgSO4}=\dfrac{0,5.1}{1}=0,5\left(mol\right)\)
⇒ \(m_{MgSO4}=0,5.120=60\left(g\right)\)
\(m_{ddspu}=12+200-\left(0,5.2\right)=211\left(g\right)\)
\(C_{MgSO4}=\dfrac{60.100}{211}=28,44\)0/0
Chúc bạn học tốt
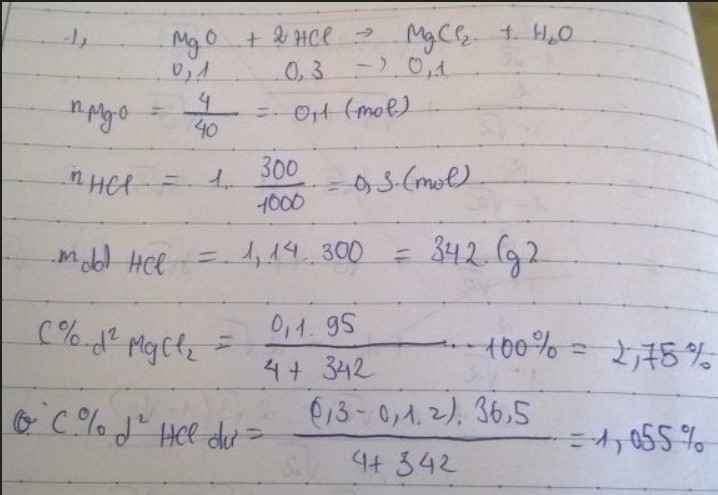
CaCO3 + 2HCl ----------> CaCl2 + H2O + CO2 (1)
0,1 0,2 0,1 (mol)
nCaCO3 = 10 /100 =0,1 (mol)
mHCl = 114,1 . 8% : 100% = 9,128 (g)
=> n HCl =9,128 /26,5 = 0,25 (mol)
nHCl = 10/100 = 0,1 (mol)
nCaCO3 /1 = 0,1/1 = 0,1 < nHCl /2 = 0,25/2 =0,125
=> HCl dư
=> sau pư thu được dd CaCl2 , dd HCl dư
C% dd ZnCl2 = \(\frac{0,1.136}{10+114,1}.100\%\) = 10,96%
C% dd HCl dư = \(\frac{\left(025-0,2\right).36,5}{10+114,1}.100\%\)= 1,47%