
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a) Hợp chất của X với Cl : XCl3
Vì Cl hóa trị I
Gọi hóa trị của X là n
Áp dụng quy tắc hóa trị : n.1=1.3 => n=3
=> Hóa trị của X là III
b)Hóa trị của X là III, hóa trị của nhóm SO4 là II
=> Hợp chất của X với SO4 là : X2(SO4)3

\(\dfrac{m_S}{m_O}=\dfrac{1}{1}\)
=> \(\dfrac{32.n_S}{16.n_O}=\dfrac{1}{1}\)
=> \(\dfrac{n_S}{n_O}=\dfrac{1}{2}\)
=> CTHH: SO2

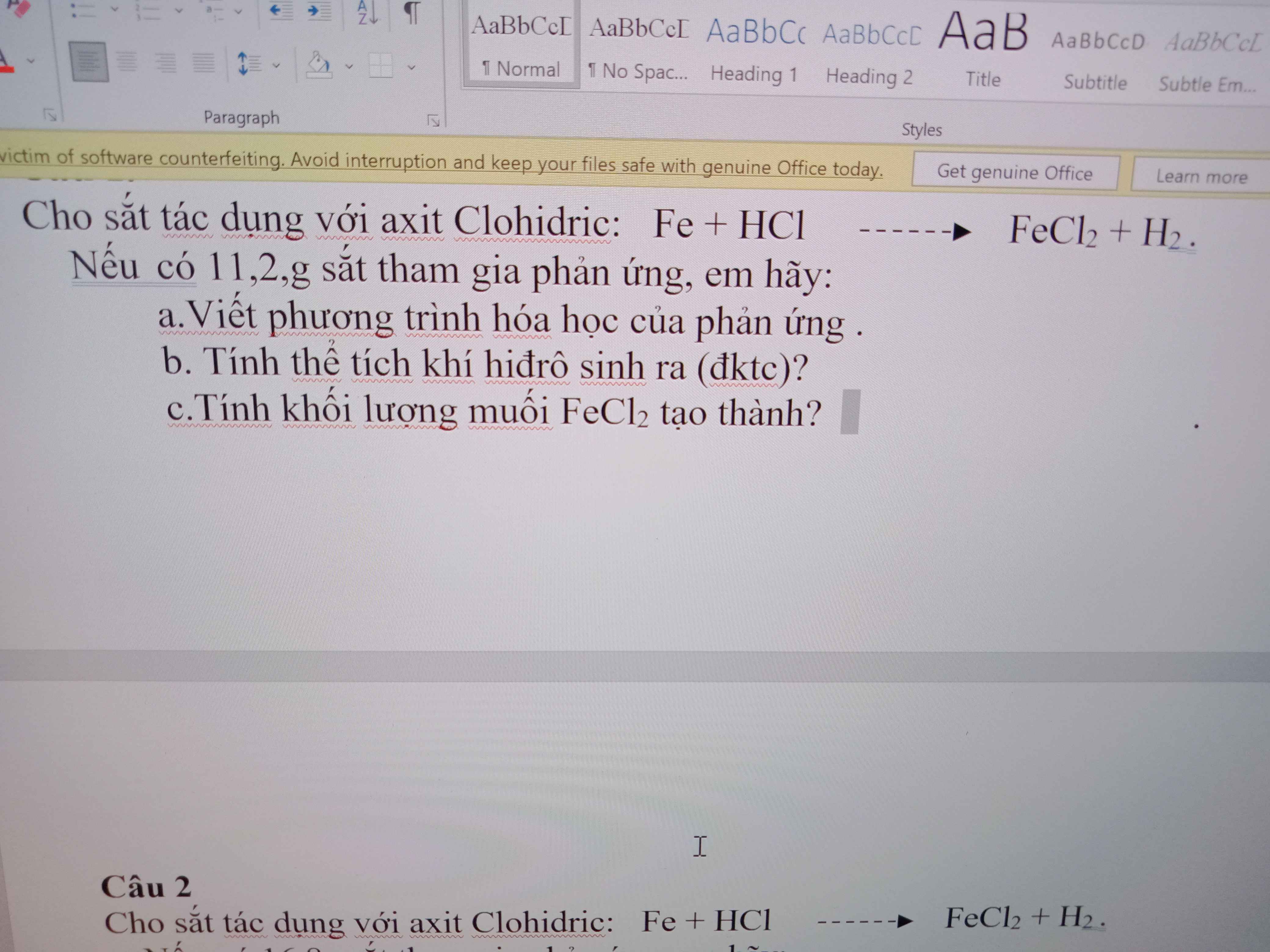
a, Fe + 2HCl \(\rightarrow\) FeCl2 + H2
b, \(n_{Fe}=\dfrac{11,2}{56}=0,2mol\\ n_{H_2}=0,2mol\\ V_{H_2}=0,2.22,4=4,48l\)
\(c,n_{FeCl_2}=0,2mol\\ m_{FeCl_2}=0,2.\left(56+35,5.2\right)=25,4g\)
a. PTHH: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
b. \(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
1 mol Fe tạo ra 1 mol H2
=> 0,2 mol Fe tạo ra 0,2 mol H2
\(V_{H_2}=0,2.22,4=4,48\left(l\right)\)
c.
1 mol Fe tạo ra 1 mol FeCl2.
=> 0,2 mol Fe tạo ra 0,2 mol FeCl2
\(m_{FeCl_2}=0,2.\left(56+35,5.2\right)=25,4\left(g\right)\)



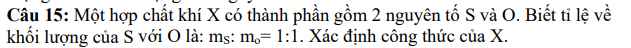

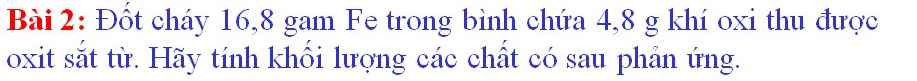
a, Fe + 2HCl \(\rightarrow\) FeCl2 + H2
b, \(n_{Fe}=\dfrac{16,8}{56}=0,3mol\\ n_{H_2}=0,3mol\\ V_{H_2}=0,3.22,4=6,72l\)
c, \(m_{FeCl_2}=0,3.\left(56+35,5.2\right)=38,1g\)