Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Bảo toàn khối lượng ta có: $m_{R}=2,4(g)$$R+X_2\rightarrow RX_2$
Ta có: $\frac{2,4}{R}=\frac{4,26}{2X}$
Lập bảng biện luận thông qua halogen tìm được X và R lần lượt là Cl và Ca

4) \(m_{Cl_2}=43,25-18,4=24,85g\)
\(n_{Cl_2}=\frac{24,85}{71}=0,35mol\)
\(V_{Cl_2}=0,35.22,4=7,84l\)
5) \(m_{F_2}=53,6-30,8=22,8g\)
\(n_{F_2}=\frac{22,8}{39}=0,6mol\)
\(V_{F_2}=0,6.22,4=13,44l\)

1.
Gọi hóa trị của kim loại M là n, ta có:
\(2M+nCl_2\underrightarrow{^{to}}2MCl_n\)
Dựa vào pt, ta thấy:
nM=nMCln
⇔ 3,2/M=6,75/M+35,5n
⇔ M=32n
Vì M là kim loại nên hóa trị có thể là I, II và III:
- Nếu n=1 ==> M=32 (Loại)
- Nếu n=2 ==> M=64 (Chọn - Cu)
- Nếu n=3 ==> M=96 (Loại)
Vậy kim loại M là Cu.
2.
\(Cu+X_2\underrightarrow{^{to}}CuX_2\)
nX2=2,24/22,4=0,1 (mol)
nCuX2=nX2=0,1 (mol)
==> mCuX2= 0,1.(64 + 2X)=22,4
==> X= 80 (Br)
Vậy halogen X là Br.

\(\text{a)2M+2H2O}\rightarrow\text{2MOH+H2}\)
Ta có :
\(n_{H2}=\frac{1,334}{22,4}=\text{0,06(mol)}\)
\(\rightarrow\text{nM=0,06.2=0,12(mol)}\)
\(M_M=\frac{2,76}{0,12}=23\)
\(\rightarrow\)M là Natri
\(\text{b) 2Na+X2}\rightarrow\text{2NaX}\)
Ta có
mNa=mNaX-mX2=11,7-7,1=4,6(g)
\(n_{Na}=\frac{4,6}{23}\text{=0,2(mol)}\)
\(\rightarrow n_{X2}=\frac{0,2}{2}=\text{0,1(mol)}\)
\(\rightarrow M_{X2}=\frac{7,1}{0,1}=\text{71}\)
\(\rightarrow\text{MX=35,5}\)
Vậy X là Clo
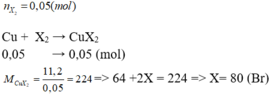
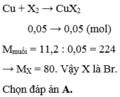

Bài 2 :
- Gọi hóa trị của kim loại M là x ( x > 0 )
PTHH : \(2M+xCl_2\rightarrow2MCl_x\)
\(n_M=\frac{m_M}{M_M}=\frac{10,8}{M_M}\left(mol\right)\)
\(n_{MCl_x}=\frac{m_{MCl_x}}{M_{MCl_x}}=\frac{53,4}{M_M+35,5x}\left(mol\right)\)
- Theo PTHH : \(n_M=n_{MCl_x}\left(mol\right)\)
=> \(\frac{10,8}{M_M}=\frac{53,4}{M_M+35,5x}\)
=> \(10,8M_M+383,4x=53,4M_M\)
=> \(383,4x=42,6M_M\)
=> \(M_M=9x\)
- Lập bảng giá trị :
-> MM = 27 ( đvc ) khi x = 3 .
Vậy M là kim loại nhôm ( Al ) .
1/n(X2) = 0,05 (mol)
=> n(Cu) = 0,05 (mol)
=> m(Cu) = 3,2 (g)
=> m(X2) = m(CuX2) - m(Cu) = 8 (g)
=> M(X2) = 8/0,05 = 160 => Br2
Vậy X là Brom