
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Câu 8:
a) Bảo toàn khối lượng: \(m_{O_2}=m_{KClO_3}-m_{rắn}=9,6\left(g\right)\)
\(\Rightarrow n_{O_2}=\dfrac{9,6}{32}=0,3\left(mol\right)\) \(\Rightarrow V_{O_2}=0,3\cdot22,4=6,72\left(l\right)\)
b) Bảo toàn khối lượng: \(m_{rắn}=m_{O_2}+m_P=9,6+9,3=18,9\left(g\right)\)

Mỗi một câu trong mỗi phần mình đánh số (1),(2),... nhé
a)
(1) : Biến đổi vật lí
(2) : Biến đổi hóa học
b)
(1) : Biến đổi vật lí
(2) : Biến đổi hóa học
a) Giũa một đinh sắt thành mạt sắt => Biến đổi vật lý
Ngâm mạt sắt trong ống nghiệm đựng axit clohidric, thu được sắt clorua và khí hidro => Biến đồi hóa học
Fe + 2HCl --------> FeCl2 + H2
b) Cho một ít đường vào ống nghiệm đựng nước, khuấy cho đường tan hết ta thu được nước đường =>Biến đổi vật lý
Đun sôi nước đường trên ngọn lửa đèn cồn, nước bay hơi hết => Biến đổi vật lý
Tiếp tục đun ta được chất rắn màu đen và khí thoát ra, khí này làm đục nước vôi trong => Biến đồi hóa học
C12H22O11 + 12O2 ------> 12CO2 + 11H2O
CO2 + Ca(OH)2 ------> CaCO3 + H2O



C12:
\(nK=\dfrac{19,5}{39}=0,5\left(mol\right)\)
\(2K+2H_2O\rightarrow2KOH+H_2\)
0,5 0,5 0,5 0,25 (mol)
mKOH = 0,5.56 = 28 (g)
m\(H_2=0,25.2=0,5\left(g\right)\)
mdd = mK + mddH2O - mH2
= 19,5 + 261 - 0,5 = 280 (g)
\(C\%_{dd}=\dfrac{28.100}{280}=10\%\)
=> Chọn D
II. Tự luận
C1 :
\(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
\(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
C2 :
\(N_2O_5+H_2O\rightarrow2HNO_3\)
=> Pứ hóa hợp
\(Fe_2O_3+3CO\underrightarrow{t^o}2Fe+3CO_2\)
=> Pứ thế
C3:
Trích mẫu thử ở mỗi dung dịch , đánh số thứ tự , ta nhúng quỳ :
+ Quỳ chuyển đỏ : HCl
+ Quỳ chuyển xanh : NaOH
+ Quỳ không chuyển màu : NaCl
C4:
\(nCuO=\dfrac{2,4}{80}=0,03\left(mol\right)\)
\(CuO+H_2\rightarrow Cu+H_2O\)
0,03-->0,03--->0,03-->0,03
\(VH_2=0,03.22,4=0,672\left(l\right)\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
0,02 0,03 (mol)
\(mAl=0,02.27=0,54\left(g\right)\)

Gọi CTHH là: XH3
Theo đề, ta có: \(d_{\dfrac{XH_3}{H_2}}=\dfrac{M_{XH_3}}{M_{H_2}}=\dfrac{M_{XH_3}}{2}=8,5\left(lần\right)\)
=> \(M_{XH_3}=17\left(g\right)\)
Ta có: \(M_{XH_3}=M_X+1.3=17\left(g\right)\)
=> MX = 14(g)
Dựa vào bảng hóa trị, suy ra:
X là nitơ (N)
=> CTHH của hợp chất là NH3
Chọn B


a.\(Fe+2HCl\rightarrow FeCl2+H2\)
b.\(nFe=\dfrac{5.6}{56}=0.1mol\)
\(nHCl=\dfrac{3.65}{36.5}=0.1mol\)
\(0.1>\dfrac{0.1}{2}\) => Fe dư
c.Số mol Fe còn dư: 0.1 - 0.05 = 0.05mol
=> mFe = 0.05\(\times56=2.8g\)
d.\(V_{H2}=0.05\times22.4=1.12l\)





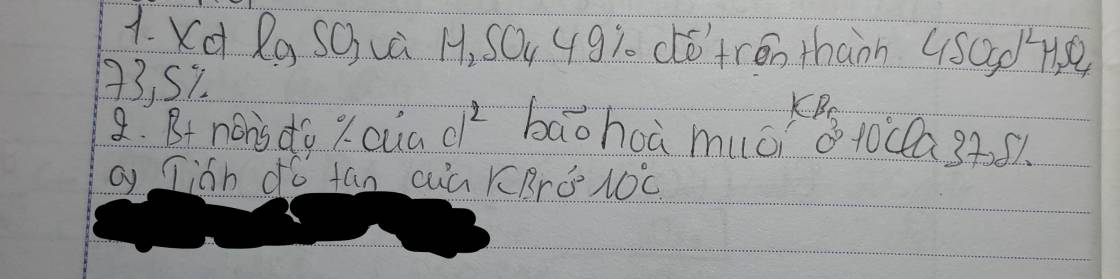 giải giúp mik vs ạ mik đang cần gấp!!!
giải giúp mik vs ạ mik đang cần gấp!!!

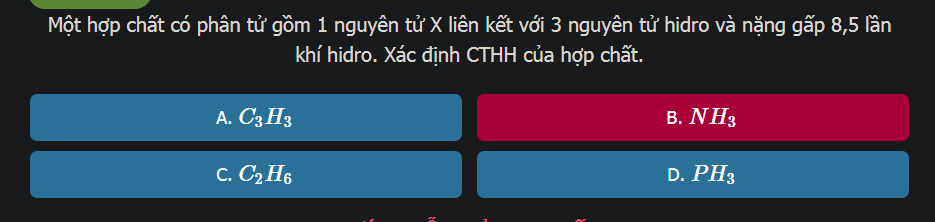 bạn nào giải thích giúp mik vs ạ. mik ko hỉu
bạn nào giải thích giúp mik vs ạ. mik ko hỉu


Gọi số hạt p và n và e lần lượt là P và N và E
Có: P = E
Theo đề cho, có:
P + N + E = 2P + N = 34
P + 3 - N = 2P - N =10
-> P=11 và N=12
-> E=11