
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


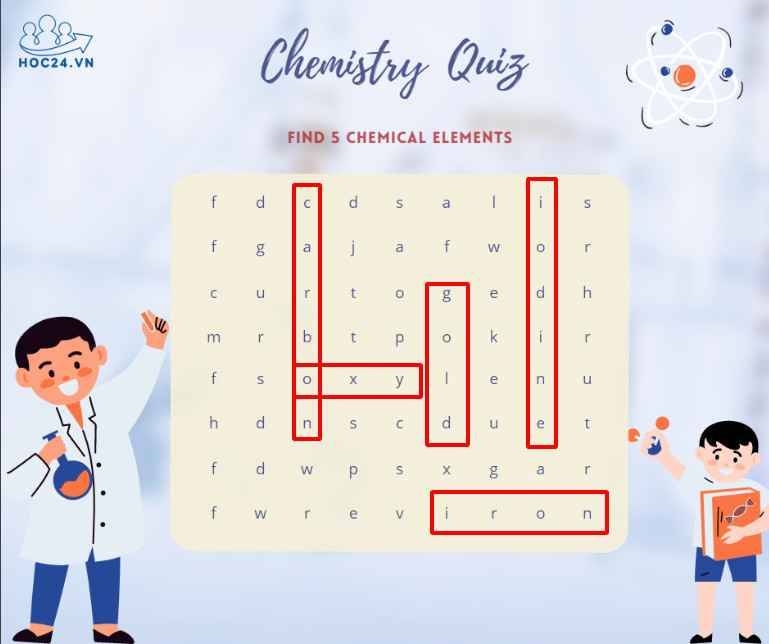
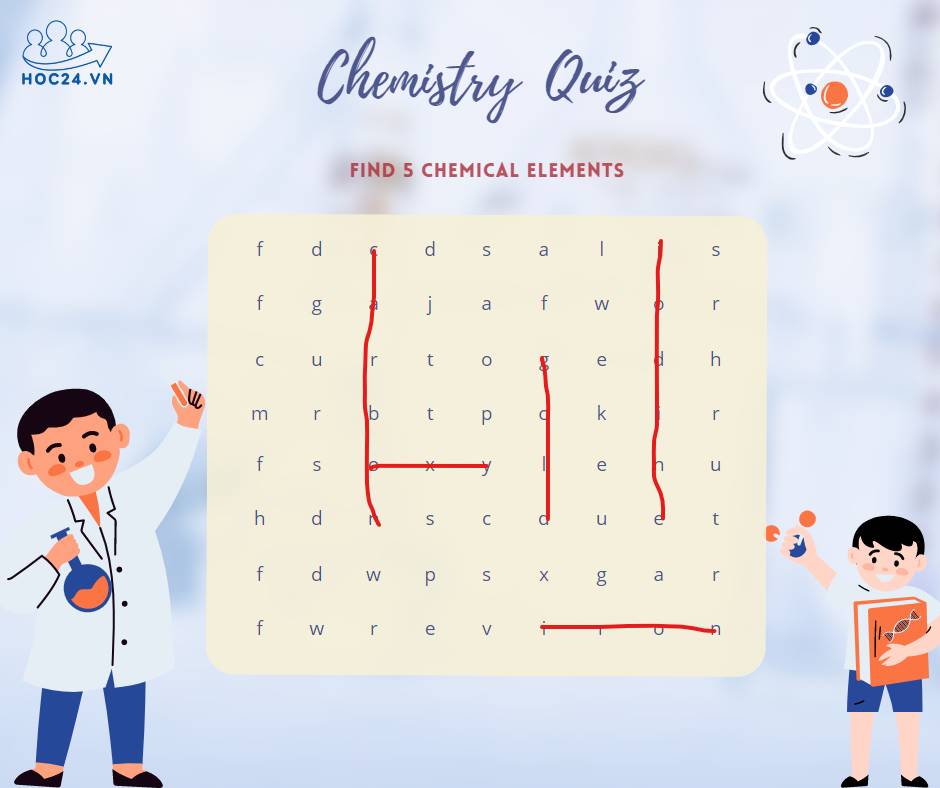
*cái oxy em k chắc á cô:<< em tìm được mấy nguyên tố này th ạ:<.

Bài 2) Ở 90 độ C:
- 100 gam nước hoà tan 50 gam KCl để tạo 150 gam dung dịch bão hoà ở nhiệt độ này
a) C% của dung dịch bão hoà tại 90 độ C là:
(Khối lượng chất tan/Khối lượng dung dịch) . 100%
<=> (50:150).100% = 33,33%
b) Ở 0 độ C:
Gọi m là khối lượng chất tan KCl ở 0o C => Khối lượng dung dịch tại nhiệt độ này là: 100+m
Theo đề bài ra ta có: m/100+m = 25,93%
=> m = 35 gam
Vậy ở 0 độ C độ tan của KCl trong nước là 35 gam
c) Ở 90 độ C:
100 gam nước hoà tan 50 gam KCl tạo 150 gam dd
=> 600 gam dung dịch tạo 200 gam KCl và 400 gam nước
- Ở 0 độ C:
100 gam nước hoà tan 35 gam KCl tạo 135 gam dd
=> 400 gam nước hoà tan được 140 gam KCl tạo 400 + 140 = 540 gam dung dịch
Vậy khi làm lạnh 600 gam dung dịch KCl từ 90 độ xuống 0 độ thì khối lượng dung dịch thu được là 540 gam

Câu 3:
N2+O2\(\overset{t^0}{\rightarrow}\)2NO
4NO+3O2+2H2O\(\rightarrow\)4HNO3
NO3- : làm tăng lượng phân đạm cho cây!


2a,
trích mẫu thử
dùng quỳ tím tách đc 3 nhóm
làm quỳ tím thành đỏ :HCl;H2SO4
làm quỳ tím thành xanh:NaOH
không làm đổi màu quỳ tím :NaCl
từ đó ta nhận biết được NaOH và NaCl
cho BaCl2 vào 2 dung dịch chưa phân biệt được nếu xuất hiện kết tủa -> H2SO4 còn lại là HCl
pthh : H2SO4+BaCl2=--->BaSO4+2HCl
























 Giúp mình giải vài câu thực tế Hoá nha..
Giúp mình giải vài câu thực tế Hoá nha..


 Giúp mình với
Giúp mình với

\(C_2H_5OH+O_2\underrightarrow{mengiam}CH_3COOH+H_2O\)
a, Ta có: \(V_{C_2H_5OH}=\dfrac{8.10}{100}=0,8\left(l\right)=800\left(cm^3\right)\)
\(\Rightarrow m_{C_2H_5OH}=800.0,8=640\left(g\right)\Rightarrow n_{C_2H_5OH}=\dfrac{640}{46}=\dfrac{320}{23}\left(mol\right)\)
Theo PT: \(n_{CH_3COOH\left(LT\right)}=n_{C_2H_5OH}=\dfrac{320}{23}\left(mol\right)\)
Mà: H = 92% \(\Rightarrow n_{CH_3COOH\left(TT\right)}=\dfrac{320}{23}.92\%=12,8\left(mol\right)\)
\(\Rightarrow m_{CH_3COOH}=12,8.60=768\left(g\right)\)
b, Ta có: \(m_{ddgiam}=\dfrac{768}{4\%}=19200\left(g\right)\)