Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
BTĐT cho dung dịch X ta có : 0,1 + 3z = t + 0,04.
![]()
![]()
![]()
![]()
![]()
![]()
nOH- phản ứng với Al3+ = 0,168 – 0,1 = 0,068mol < 3nAl(OH)3
=> nAl(OH)3= 4nAl3+ - nOH- => nAl3+ = (nAl(OH)3 + nOH-) : 4 = 0,02mol = z
![]()
= 0,12 mol

Đáp án B
BTĐT cho dung dịch X ta có : 0,1 + 3z = t + 0,04.
![]()
![]()
![]()
![]()
![]()
![]()
nOH- phản ứng với Al3+ = 0,168 – 0,1 = 0,068mol < 3nAl(OH)3
=> nAl(OH)3= 4nAl3+ - nOH- => nAl3+ = (nAl(OH)3 + nOH-) : 4 = 0,02mol = z
=> t = n N O 3 - = 0,1 + 3.0,02 - 0,04 = 0,12 mol

Đáp án D
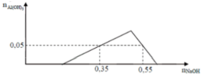
Ta có: x = 0,35 – 0,05.3 = 0,2
Tại điểm kết tủa cực đại là
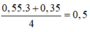
=> z = 0,2.
Khi thêm 0,27 Ba(OH)2 thì thu được kết tủa Z chứa
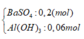
=> m = 51,28 gam

Tại nOH- = 0,35 thì Al(OH)3 chưa đạt cực đại ⇒ Al3+ còn dư
H+ + OH- → H2O
Al3+ + 3OH- → Al(OH)3
⇒ nOH- = nH+ + 3n↓ ⇒ 0,35 = x + 3.0,05 ⇒x = 0,2
Tại nOH- = 0,55 thì Al(OH)3 đạt cực đại và bị tan bớt 1 phần
H+ + OH- → H2O
0,2 → 0,2
Al3+ + 3OH- → Al(OH)3
y → 3y → y
Al(OH)3 + OH- → AlO2- + 2H2O
(y – 0,05) → (y – 0,05
⇒ nOH- = 0,2 + 3y + y – 0,05 = 0,55 ⇒ y = 0,1
Bảo toàn điện tích ⇒ 0,2 + 0,1.3 = 2z + 0,1 ⇒z = 0,2
Khi cho 0,27 mol Ba(OH)2 vào dung dịch X thì
Ba2+ + SO42- → BaSO4↓
0,2 → 0,2
H+ + OH- → H2O
0,2 → 0,2
Al3+ + 3OH- → Al(OH)3
0,1 → 0,3 → 0,1
Al(OH)3 + OH- → AlO2- + 2H2O
0,04 ← 0,04
⇒ mY = mBaSO4 + mAl(OH)3 = 0,2.233 + 0,06.78 = 51,28g ⇒ Chọn D.

Chọn đáp án B
Ta có: 1 mol dung dịch X chứa x+2y mol OH-
+ Ta có 1 mol dung dịch Y chứa y+2x mol OH-
+ Vì khi cho SO42- vào vẫn còn kết tủa nên lượng kết tủa tính trong bài hoàn toàn tính theo CO32-
+ Hấp thụ hết 0,04 mol CO2 vào 200 ml dung dịch X, thu được dung dịch M và 1,97 gam kết tủa
⇒ nOH– = 0,2×(x+2y)
⇒ nBaCO3 = 0,01, nBa(HCO3)2 = 0 , 04 - 0 , 01 2 = 0,015 mol
⇒ nOH– = 0,01×2 + 0,015×2 = 0,05 mol.
⇒ x + 2y = 0,25.
+ Nếu hấp thụ hết 0,0325 mol CO2 vào 200 ml dung dịch Y thì thu được dung dịch B và 1,4775 gam kết tủa.
nBaCO3 = 0,0075 ⇒ nHCO3– = 0,0325 – 0,0075 = 0,025.
⇒ nOH– = 0,2×(2x + y) = 0,025 + 0,0075×2 = 0,04 → 2x + y = 0,2.
⇒ x = 0,05 và y = 0,1

Phân tích thí nghiệm của dung dịch X với NaOH
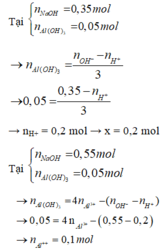

Thí nghiệm 2
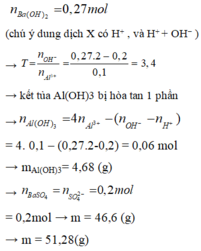
Đáp án C

Đáp án B
Coi phản ứng của 0,04 mol CO2 với dung dịch X là thí nghiệm 1 (TN1); phản ứng của Y với 0,0325 mol CO2 là thí nghiệm 2 (TN2).
Ở cả hai TN n BaCO 3 < n CO 2 . Mặt khác, dung dịch sau phản ứng ở hai TN phản ứng với KHSO4 đều tạo ra kết tủa. Suy ra : Dung dịch sau phản ứng còn chứa Ba2+. Ion CO 3 2 - tạo ra đã chuyển hết vào BaCO3. Dung dịch sau các phản ứng chứa
![]()
Sử dụng bảo toàn nguyên tố Ba, C và bảo toàn điện tích cho dung dịch sau phản ứng, ta có:
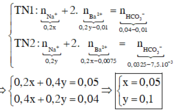
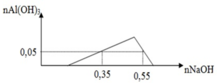
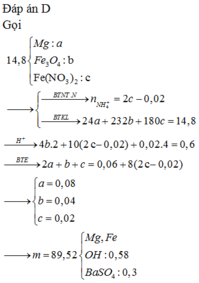
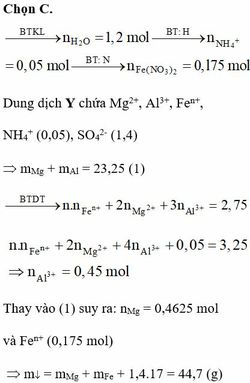
Ta có: nOH = nKOH + 2nBa(OH)2 = 0,168mol.
Cho Y vào X có các phản ứng sau:
H+ + OH- = H2O (1)
0,1 0,1
Al3+ + 3OH- = Al(OH)3¯ (2)
z 3z z
Al(OH)3 + OH- = AlO2- + 2H2O(3)
0,068-3z
Ba2+ + SO42- = BaSO4¯ (4)
0,012 0,02 0,012
® mAl(OH)3 = 3,732 – 233.0,012 = 0,936gam ® nAl(OH)3 dư = 0,012mol.
® z – (0,068-3z) = 0,012 ® z = 0,02; t = 0,1+3z-2.0,02=0,12 mol.