Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

R là Cu
X1 là CuO, X2 là CuSO4, X3 là Cu(NO3)2, X4 là Cu(OH)2
PTHH:
\(2Cu+O_2\underrightarrow{t^o}2CuO\)
\(CuO+H_2SO_4\rightarrow CuSO_4+H_2O\)
\(Cu+2H_2SO_{4\left(đ\right)}\underrightarrow{t^o}CuSO_4+SO_2+2H_2O\)
\(CuO+2HNO_3\rightarrow Cu\left(NO_3\right)_2+H_2O\)
\(Cu+4HNO_{3\left(đ\right)}\rightarrow Cu\left(NO_3\right)_2+2NO_2+2H_2O\)

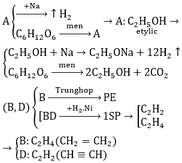
C không tác dụng với Na nhưng tác dụng được với NaOH
=> C : HCOOCH3→ HCOOCH + NaOH → HCOONa + CH3OH

E là este no, đơn chức => E được tạo thành từ 1 axit cacboxylic no, đơn chức, mạch hở và 1 ancol no, đơn chức, mạch hở.
từ X điều chế trực tiếp ra Y bằng một phản ứng => E là CH3COOC2H5.
PTPỨ:
CH3COOC2H5 + H2O => CH3COOH(Y) + C2H5OH(X)
C2H5OH + O2 (men giấm)=> CH3COOH + H2O

a, Đốt cháy A thu CO2 và H2O nên A chắc chắn gồm C và H, có thể có O.
Ta có: \(n_{CO_2}=\dfrac{6,6}{44}=0,15\left(mol\right)=n_C\)
\(n_{H_2}=\dfrac{2,7}{18}=0,15\left(mol\right)\Rightarrow n_H=0,15.2=0,3\left(mol\right)\)
Có: mC + mH = 0,15.12 + 0,3.1 = 2,1 (g) < mA
⇒ A gồm C, H và O.
b, Ta có: mO = 4,5 - 2,1 = 2,4 (g) \(\Rightarrow n_O=\dfrac{2,4}{16}=0,15\left(mol\right)\)
Giả sử CTPT của A là CxHyOz.
⇒ x : y : z = 0,15 : 0,3 : 0,15 = 1 : 2 : 1
⇒ CTĐGN của A là (CH2O)n.
Có: MA = 30. 2 = 60 (g/mol)
\(\Rightarrow n=\dfrac{60}{12+2+16}=2\)
Vậy: A là C2H4O2.
c, PT: \(2CH_3CHO+O_2\underrightarrow{Mn^{2+}}2CH_3COOH\)
\(CH_3COOH+NaOH\rightarrow CH_3COONa+H_2O\)
\(CH_3COONa+NaOH\xrightarrow[t^o]{CaO}CH_4+Na_2CO_3\)
Bạn tham khảo nhé!
Hicc, phần c chỉ có 2 PT cuối thôi ak, bạn bỏ PT đầu đi nhé!

Đặt công thức của oxit thu được là M2Ox ( trong đó x là hóa trị của kim loại)
Do trong oxit oxi chiếm 20% nên kim loại đó sẽ chiếm 80 % về khối lượng => 2M/16x = 80%/20%=4
<=> M = 32x.
Do M là kim loại nên hóa trị của nó là giá trị nguyên chạy trong khoảng 1 đến 3 (lớp 10 có học rồi). Thay lần lượt các giá trị vào x ta sẽ được M=64 và x=2 => M : Cu
Ta có :
2M + O2----> 2MO
2(M+16)
Vì oxi chiếm 20% khối lượng nên ta có:
2(M + 16) . 20% = 32
(2M + 32).20%=32
0,4M + 6.4 =32
0.4M = 32-6.4
0.4M =25.6 ===> M=64 (Cu)
Vậy kim loại đó là Cu

m rắn giảm = mO (oxit) => nO (oxit) = (1,6 – 1,408) : 16 = 0,012mol
Dễ thấy n = nO (oxit) = 0,012mol
=> nH2 ban đầu = 0,012 : 80% = 0,015
=> nFe = nH2= 0,015 → x = 0,015
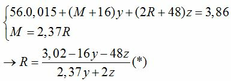
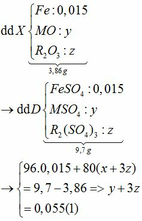
Ta có: CO + O(Oxit) → CO2
Vì: m(Rắn giảm) = mO(Oxit) → nO(Oxit) = (3,86 – 3,46) : 16 = 0,025
TH1: cả 2 oxit đều bị khử bởi CO
→ nO(Oxit) = y + 3z = 0,025 kết hợp với (1) loại
TH2: chỉ có MO bị khử bởi CO
→ nO(Oxit) = nMO = 0,025 → y = 0,025 kết hợp với (1) => z = 0,01
Kết hợp với (*) => M = 64 (Cu)
TH3: chỉ có R2O3 bị khử bởi CO
→ nO(Oxit) = 3.nR2O3 → z = 0,025/3 kết hợp với (1) => y = 0,03
Kết hợp với (*) y => M lẻ => loại
Vậy %m các chất trong X là: 21,76%; 51,81%; 26,43%
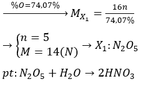
R + 02 ---> R2Oa (a là hóa trị của R)
Trong R2Oa : Oa chiếm 20%
2R chiếm 80%
Suy ra: có tỉ lệ
(2R/80)=(Oa/20) => (R/40) = (16a/20)
=>R=32a
Chọn a=2=>R=64
X1 : CuO
X2: CuSO4
X3: Cu(NO3)2
X4:CuCl2 hoặc Cu(OH)2
Cu + 2H2SO4đ ----->CuSO4 +SO2 +2H20
CuO+H2SO4 ----->CuSO4 + H20
3Cu + 8HNO3đ ----->3Cu(NO3)2 + 2NO +4H20
CuO+2HNO3 ----->Cu(NO3)2 + H20
Cu +HCl (không phản ứng)
CuO +2HCl --->CuCl2 +H20
R:Cu
X1:CuO
X4:Cu(OH)2
X2:CuCl2
X3:CuSO4