Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án : B
Từ dữ kiện đề bài ta tính được %H = 7,64% ; %C = 77.37%; %N = 15.05%
=> Công thức phân tử C6H7N

Ta có: \(n_{H_2O}=\dfrac{9,72}{18}=0,54\left(mol\right)\Rightarrow n_H=0,54.2=1,08\left(mol\right)\)
\(n_{CO_2}=\dfrac{21,12}{44}=0,48\left(mol\right)=n_C\)
\(n_{N_2}=\dfrac{0,224}{22,4}=0,01\left(mol\right)\Rightarrow n_{N\left(1,42\left(g\right)X\right)}=0,01.2=0,02\left(mol\right)\)
\(\Rightarrow n_{N\left(8,52\left(g\right)X\right)}=0,02.\dfrac{8,52}{1,42}=0,12\left(mol\right)\)
⇒ mC + mH + mN = 0,48.12 + 1,08.1 + 0,12.14 = 8,52 (g) = mX
→ X chứa C, H và N.
Gọi CTPT của X là CxHyNt.
⇒ x:y:t = 0,48:1,08:0,12 = 4:9:1
Mà: X chỉ chứa 1 nguyên tử N.
→ CTPT của X là C4H9N.

Gọi công thức phân tử của X là CxHyOz .
Sản phẩm cháy gồm CO2 và H2O.
Ở lần thí nghiệm thứ nhất, bình 1 chứa H2SO4 đậm đặc dư hấp thụ H2O và bình 2 chứa dung dịch nước vôi trong dư hấp thụ CO2.
Ở lần thí nghiệm thứ hai, bình 1 chứa CaO dư hấp thụ CO2 và toàn bộ hơi nước, bình 2 chứa P2O5 dư không hấp thụ gì vì toàn bộ lượng khí đã được hấp thụ ở bình 1. Do đó m2 = 0. Theo định luật bảo toàn khối lượng ta có
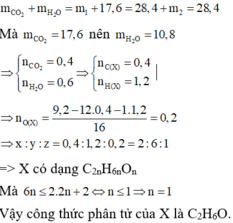

còn thiếu nguyên tố Ôxi và bạn chưa hề sử dụng tới dữ kiện là có 0,6gam hợp chất hữu cơ X

Chọn đáp án D
nC = nCO2 = n↓ = 0,02 mol.
mbình tăng = mCO2 + mH2O
⇒ nH2O = (1,24 - 0,02 × 44) ÷ 18 = 0,02 mol
⇒ nH = 0,04 mol.
mX = mC + mH + mO ⇒ mO = 0,64(g)
⇒ nO = 0,02 mol.
⇒ C : H : O = 0,02 : 0,04 : 0,02 = 1 : 2 : 1
⇒ CT nguyên: (CH2O)n.
30n = 30 ⇒ n = 1 ⇒ CTPT của X là CH2O

nCaCO3=0,02 mol=nCO2 ==>%C=(0,02.12):0,6=40%
m(bình tăng)=mCO2+mH2O=0,02.12+mH2O=1,24==>mH2O=0,36g
==>mH=(0,36.2):18=0,04 g
%H=6,67% =>%O=100-40-6,67=53,33%
CTĐGN CxHyOz
x:y:z=40/12 : 6,67 : 53,33/16
= 3,33 : 6,67 : 3,33 = 1: 2 : 1
=> CTĐGN : CH2O
CTPT : (CH2O)n M=30n=15.2 =>n=1
=> CTPT : CH2O

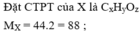
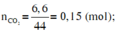
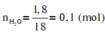


Đáp án : B
Từ dữ kiện đề bài ta tính được %H = 7,64% ; %C = 77.37%; %N = 15.05%
=> Công thức phân tử C6H7N