Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Khi điện phân hỗn hợp KF trong HF lỏng khan (đã được loại bỏ hết nước). Sở dĩ phải tránh sự có mặt của nước vì flo tác dụng với nước cho thoát ra O2.
2F2 + 2H2O → 4HF + O2
Phản ứng thật ra rất phức tạp : đầu tiên có phản ứng hóa học:
F2 + H2O → 2HF + O
Một số nguyên tử oxi kết hợp với flo cho OF2. Như vậy ta điều chế không được flo nguyên chất.

Khi điện phân hỗn hợp KF trong HF lỏng khan đã được loại bỏ hết nước. Sở dĩ phải tránh sự có mặt của nước vì flo tác dụng với nước cho thoát ra O2
2F2 + 2H2O → 4HF + O2 ↑

Khi điện phân hỗn hợp KF trong HF lỏng khan đã được loại bỏ hết nước. Sở dĩ phải tránh sự có mặt của nước vì flo tác dụng với nước cho thoát ra O2
2F2 + 2H2O → 4HF + O2 ↑
Phản ứng thật ra rất phức tạp: đầu tiên phải có phản ứng hóa học:
F2 + H2O → 2HF + O
Một số nguyên tử oxi kết hợp với flo cho OF2. Như vậy ta điều chế không được flo nguyên chất.

Do Flo có tính oxi hóa mạnh nhất nên F- không bị oxi hóa bởi các chất oxi hóa thông thường, mà phải dùng dòng điện.
A sai, vì Clo, brom cũng có tính oxi hóa mạnh mà vẫn điều chế được.
C sai, các hợp chất florua đều có tính khử.
D sai, flo có độ âm điện lớn nhất nhưng không giải thích được điều trên.

Điều chế HF, HCl bằng cách cho H 2 SO 4 đặc tác dụng với muối florua, clorua vì H 2 SO 4 à chất oxi hoá không đủ mạnh để oxi hoá được HF và HCl. Nói cách khác, HF và HCl có tính khử yếu, chúng không khử được H 2 SO 4 đặc
Ca F 2 + H 2 SO 4 → Ca SO 4 + 2HF
NaCl + H 2 SO 4 → NaH SO 4 + HCl
Nhưng không thể dùng phương pháp trên để điều chế HBr và HI vì H 2 SO 4 đặc oxi hoá được những chất này thành Br 2 và I 2 . Nói cách khác, HBr và HI là những chất có tính khử mạnh hơn HCl và HF.
NaBr + H 2 SO 4 → HBr + NaH SO 4
2HBr + H 2 SO 4 → Br 2 + SO 2 + 2 H 2 O
NaI + H 2 SO 4 → NaH SO 4 + HI
2HI + H 2 SO 4 → I 2 + SO 2 + 2 H 2 O

a)
SO2 + Br2 + 2H2O =.> 2HBr + H2SO4
SO2 đã khử Br2 có màu thành HBr không màu
Khi dẫn khí SO2 vào dung dịch axit H2S dung dịch bị vẩn đục màu vàng:
SO2 + 2H2S = 3S + 2H2O , SO2 đã oxi hóa H2S thành S
b)Khi cho clo vào nước thì: Cl2 + H2O --> HCl + HClO.
Khi cho flo vào nước thì flo do là chất oxi hóa mạnh sẽ bốc cháy trong nước nên không thể điều chế được nước clo:
2F2 + 2H2O --> 4HF + O2
c)dùng dd KI có lẫn hồ tinh bột
2KI + H20 +O3--->2 KOH +I2 + O2
a. + Cho SO2 vào dd Br2:
Ptpu: SO2 + Br2 + 2H2O \(\rightarrow\) H2SO4 + 2HBr
(chất khử)
Htg: dd Br2 bị mất màu
+ Cho SO2 vào dd H2S
Ptpu: SO2 + 2H2S \(\rightarrow\) 3S\(\downarrow\) + 2H2O
(chất oxi hóa)
Htg: dd bị vẩn đục màu vàng
b. + Điều chế được nước clo vì clo tan nhiều trong nước nhưng chỉ một phần khí clo tác dụng với nước theo ptpu:
Cl2 + H2O\(\leftrightarrow\) HCl + HClO
+ Còn Flo tan trong nước thì oxi hóa hoàn toàn nước ngay ở nhiệt độ thường theo ptpu:
4F2 + 4H2O \(\rightarrow\) 4HF + O2
Do đó F2 không thể tồn tại trong nước
c. Cho quỳ tím td với ozon và oxi, ta thấy khi quỳ tím td với ozon thì quỳ tím hóa xanh, còn oxi ko pư
pthh:
\(O_3+2KI+H_2O\rightarrow I_2+2KOH+O_2\) (oxi không có)
Do tạo ra KOH nên O3 làm xanh quỳ tím ẩm dd KI
\(2Ag+O_3\rightarrow Ag_2O+O_2\) ( oxi không có pư)

Do F2 có tính oxi hóa mạnh hơn Cl2 rất nhiều và có khả năng đốt cháy H2O → Người ta không điều chế nước F2.

Đáp án D
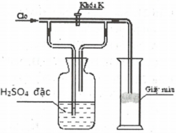
Phương trình phản ứng: MnO 2 + 4 HCl → MnCl 2 + Cl 2 ↑ + 2 H 2 O
Khí Cl2 thu được thường lẫn khí hidro clorua (khí HCl) và hơi nước. Sau khi đã loại bỏ khí HCl thì khí Cl2 còn lẫn hơi H2O
Khi đóng khoá K thì khí Cl2 lẫn hơi H2O sẽ phải đi qua H2SO4 đặc, khí thu được sau khi qua H2SO4 đặc là khí Cl2 khô (H2SO4 đặc có tính háo nước nên đã hấp thụ H2O). Khí Cl2 không tẩy được màu, do đó miếng giấy không mất màu.
Khi mở khoá K thì khí Cl2 có lẫn hơi H2O (khí Cl2 ẩm) sẽ đi đến miếng giấy màu mà không qua H2SO4 đặc, do đó miếng giấy mất màu vì Cl2 ẩm có tính tẩy màu:
Cl 2 + H 2 O ⇄ HCl + HClO
HClO là chất oxi hoá mạnh => HClO có tính tẩy màu, sát trùng,…
=> Cl2 ẩm có tính tẩy màu, sát trùng,…
Vậy phát biểu D sai.
Khi điện phân hỗn hợp KF trong HF lỏng khan (đã được loại bỏ hết nước). Sở dĩ phải tránh sự có mặt của nước vì flo tác dụng với nước cho thoát ra O2.
2F2 + 2H2O \(\rightarrow\) 4HF + O2
Phản ứng thật ra rất phức tạp : đầu tiên có phản ứng hóa học:
F2 + H2O \(\rightarrow\) 2HF + O
Một số nguyên tử oxi kết hợp với flo cho OF2. Như vậy ta điều chế không được flo nguyên chất.