Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

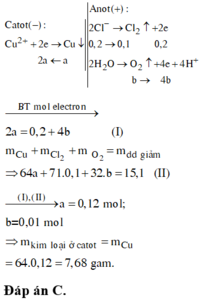
Đáp án A
![]()

Điện phân hết Cl-, mdd giảm = 0,05.71+ 0,05.64 = 6,75 g < 10,75 g => ở anot H2O bị điện phân
Ta có mdd giảm = (0,05+2x).64 + 0,05.71+32x = 10,75
=> x = 0,025
=> nCu2+ = 0,1 => Cu(NO3)2 dư
=> DD sau điện phân có: Cu(NO3)2, HNO3, KNO3

Đáp án D
Dung dịch Y làm quỳ tím hóa xanh → trong Y có O H -
→ H2O bị điện phân ở bên catot và bên anot C l - đã điện phân hết
Quá trình điện phân:
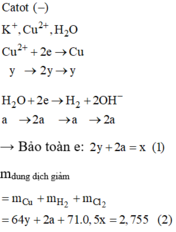
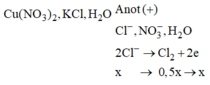


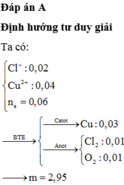
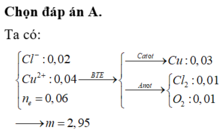
Đáp án A
Nhận thấy dung dịch Y làm quỳ tím
hóa xanh
→ Y chứa OH- và bên catot xảy ra
quá trình điện phân Cu2+, H2O
bên anot mới điện phân xong hết Cl-
Khi cho Y tác dụng với AgNO3
thu được kết tủa là Ag2O: 0,01 mol
→ nOH- = nAg+ = 0,02 mol
→ nH2 = 0,01 mol
Chú ý khối lượng dung dịch giảm
gồm Cu: y mol, H2: 0,01 mol,
Cl2: 0,5x mol
Khi đó có hệ
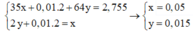
→ x : y = 10 : 3

Chọn B
nNaCl = 0,48 mol
Do khi cho Fe vào dung dịch X thì thấy thoát ra khí NO là sản phẩm khử duy nhất nên H2O đã bị điện phân ở anot.
Catot:
Cu2+ +2e → Cu
x…….2x……x
Anot:
Cl- -1e → 0,5Cl2
0,48…0,48…0,24
2H2O - 4e → O2 + 4H+
4y…..y…..4y
n e trao đổi = 2x = 0,48 + 4y (1)
m dung dịch giảm = mCu + mCl2 + mO2 => 64x + 71.0,24 + 32y = 51,6 (2)
Giải (1) và (2) => x = 0,48; y = 0,12
=> nH+ = 0,48 mol
3Fe + 8H+ + 2NO3- → 3Fe2+ + 2NO + 4H2O
0,18 ← 0,48
Fe + Cu2+ → Fe2+ + Cu
z z z
Khối lượng thanh sắt giảm: (z+0,18).56 – 64z = 6,24 => z = 0,48 mol
=> nCu(NO3)2 ban đầu = x + z = 0,48 + 0,48 = 0,96 mol
=> m = 0,96.188 = 180,48 gam


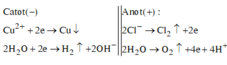



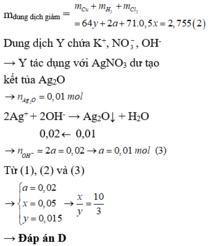
Đáp án B.
* Giả sử ở catot điện phân hết C u 2 +