Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) nC2H4Br2=47/188=0,25(mol)
n(CH4,C2H4)=11,2/22,4=0,5(mol)
PTHH: C2H4 + Br2 -> C2H4Br2
0,25<----------0,25<---------0,25(mol)
mBr2(p.ứ)=0,25 x 160= 40(g)
b) V(C2H4,đktc)=0,25 x 22,4= 5,6(l)
=> %V(C2H4)=(5,6/11,2).100=50%
=>%V(CH4)=100% - 50%= 50%

nBr2 = 0,125 mol
Khi đốt cháy nA = 0,25 mol
mNaOH ban đầu = 36g => nNaOH = 0,9 mol
Gọi x, y lần lượt là số mol của CO2 và H2O
mdd = 180 + 44x + 18y
Vì NaOH dư do đó chỉ tạo muối trung hòa
CO2 +2NaOH → Na2CO3 + H2O
x 2x
nNaOH dư = 0,9 – 2x
có 2 , 75 % = 40 ( 0 , 9 - 2 x ) 180 + 44 x + 18 y . 100 % (1)
=> 81,21x + 0,495y = 31,05n
2,8 lít khí A tác dụng với 0,125 mol Br2
=> 5,6 lít khí A tác dụng với 0,25 mol Br2
Gọi số mol khí của CH4, C2H4 và C2H2 lần lượt là a; b; c
Ta có a + b + c = 0,25 mol
Và b + 2c = 0,25
=> a = c
=> khi đốt cháy hỗn hợp A cho nCO2 = nH2O
Thay vào (1) => x = y = 0,38 mol
Bảo toàn C, H khi đốt cháy ta có
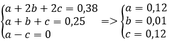
=> %VCH4 = %VC2H2 = 48%
%VC2H4 = 4%

1. \(n_{Br_2}=0,4.0,5=0,2\left(mol\right)\)
PT: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
Theo PT: \(n_{C_2H_4}=n_{Br_2}=0,2\left(mol\right)\Rightarrow V_{C_2H_4}=0,2.22,4=4,48\left(l\right)\)
2. \(n_{C_2H_4Br_2}=\dfrac{9,4}{188}=0,05\left(mol\right)\)
PT: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
Theo PT: \(n_{C_2H_4}=n_{C_2H_4Br_2}=0,05\left(mol\right)\)
\(\Rightarrow\%V_{C_2H_4}=\dfrac{0,05.22,4}{1,4}.100\%=80\%\)
\(\Rightarrow\%V_{CH_4}=100-80=20\%\)

a) C2H4 + Br2 --> C2H4Br2
b) \(n_{Br_2}=\dfrac{24}{160}=0,15\left(mol\right)\)
PTHH: C2H4 + Br2 --> C2H4Br2
0,15<--0,15----->0,15
=> \(\%V_{C_2H_4}=\dfrac{0,15.22,4}{7,84}.100\%=42,857\%\)
=> \(\%V_{CH_4}=\dfrac{7,84-0,15.22,4}{7,84}.100\%=57,143\%\)
c) mC2H4Br2 = 0,15.188 = 28,2 (g)

a, nBr2 = 8/160 = 0,05 (mol)
PTHH: C2H4 + Br2 -> C2H4Br2
Mol: 0,05 <--- 0,05 <--- 0,05
Vhh khí = 2,8/22,4 = 0,125 (mol)
%VC2H4 = 0,05/0,125 = 40%
%CH4 = 100% - 40% = 60%
b, nCH4 = 0,125 - 0,05 = 0,075 (mol)
PTHH: C2H4 + 3O2 -> (t°) 2CO2 + 2H2O
Mol: 0,05 ---> 0,15
CH4 + 2O2 -> (t°) CO2 + 2H2O
Mol: 0,075 ---> 0,15
Vkk = (0,15 + 0,15) . 5 . 22,4 = 33,6 (l)

\(n_{hh}=\dfrac{4.48}{22.4}=0.2\left(mol\right)\)
\(n_{Br_2}=\dfrac{16}{160}=0.1\left(mol\right)\)
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
\(0.1.........0.1\)
\(n_{CH_4}=0.2-0.1=0.1\left(mol\right)\)
\(\%V_{C_2H_4}=\%V_{CH_4}=\dfrac{0.1}{0.2}\cdot100\%=50\%\)
Em cung cấp thông tin đề câu b lại nhé !

B5:
1)
\(V_{thoát}=V_{CH_4\left(đktc\right)}=3,36\left(l\right)\\ \Rightarrow\%V_{\dfrac{CH_4}{B}}=\dfrac{3,36}{4,48}.100=75\%\Rightarrow\%V_{\dfrac{C_2H_4}{B}}=100\%-75\%=25\%\)
2)
\(CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\\ CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3\downarrow+H_2O\\ n_{CH_4}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\\ \Rightarrow n_{CaCO_3}=n_{CO_2}=n_{CH_4}=0,15\left(mol\right)\\ \Rightarrow m_{\downarrow}=m_{CaCO_3}=100.0,15=15\left(g\right)\)

300 ml dd Br2 có CM = :)?