Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án cần chọn là: A
Các chất có phản ứng tạo ra chất mới ở thể rắn và khí thì chất đó sẽ có khối lượng rắn nhỏ hơn.
Đặt số mol mỗi chất đem nung là 1 mol
Các chất khi nhiệt phân thu được rắn có khối lượng nhỏ hơn là: N a H C O 3 , N a N O 3 , F e O H 3 , F e S 2
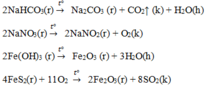
→ có 4 chất

Y: AlCl3,FeCl2
Z: H2
A: MgO,Cu,Fedư,Al2O3 dư
B: SO2
D: CaSO3
E: Fe(OH)2,Al(OH)3
G: Feo,Al2O3

Câu 3 :
Cho hỗn hợp X vào dung dịch HCl lấy dư:
PTHH: Al2O3 + 6HCl → 2AlCl3 + 3H2O
MgO + 2HCl → MgCl2 + H2O
Fe + 2HCl → FeCl2 + H2
Dung dịch Y gồm: AlCl3, MgCl2, FeCl2, HCl dư
Khí Z là H2
Chất rắn A là Cu
Cho A tác dụng với H2SO4 đặc nóng.
PTHH: Cu + 2H2SO4(đặc, nóng) → CuSO4 + SO2 + 2H2O
Khí B là SO2
Cho B vào nước vôi trong lấy dư
PTHH: SO2 + Ca(OH)2 → CaSO3 + H2O
Kết tủa D là CaSO3
Cho dung dịch NaOH vào Y tới khi kết tủa lớn nhất thì dừng lại.
PTHH: NaOH + HCl → NaCl + H2O
3NaOH + AlCl3 → Al(OH)3 + 3NaCl
2NaOH + MgCl2 → Mg(OH)2 + 2NaCl
2NaOH + FeCl2 → Fe(OH)2 + 2NaCl
Chất rắn E là: Al(OH)3, Mg(OH)2, Fe(OH)2
Nung E trong không khí

Chất rắn G là Al2O3, MgO, Fe2O3
Câu 5 :
Chỉ có Al là tác dụng được với NaOH
nH2 sinh ra = 3,36/22.4=0,15 (mol)
NaOH + Al + H20 ------> NaAl02(Natri aluminat) + H2
0,15 0,15
mAl= 0,15 . 27= 4,05 (g) ==> %mAl = 4,05 . 100/14.7=27,55%
Khi tác dụng với Hcl thì cả 3 kim loại đều tác dụng
n H2 sinh ra trong trường hợp này = 10,08 / 22,4=0,45 (mol)
Mg + 2HCl ------>MgCl2 + H2
x x x
2Al + 6HCl --------> 2AlCl3 + 3H2
0,15 0,15 0,225
Fe + 2HCl ---------> FeCl2 + H2
y y y
Đặt nMg=x, nFe=y
Ta được hệ phương trình
24x + 56y = 14,7 - 4,05= 10,65 (tính theo mMg và mFe)
x + y= 0,45 - 0,15= 0,3 (tính theo nH2)
==> x= 0,192 (mol), y=0,108 (mol)
==> mMg= 24 . 0,192 = 4,608 (g) ===> mMg = 4,608 .100/14,7 = 31,347 %
mFe= 14,7 - 4,608 - 4,05 = 6,042 (g) ===> mFe = 100% - 31,347% - 27,55% = 41,103%
dung dịch B gồm MgCl2, AlCl3, FeCl2
MgCl2 + 2NaOH ------> Mg(OH)2 + 2NaCl
0,192 0,192
AlCl3 + 3NaOH --------> Al(OH)3 + 3NaCl
0,225 0,225
FeCl2 + 2NaOH -------> Fe(OH)2 + 2NaCl
0,108 0,108
Mg(OH)2 ------> MgO + H2O
0,192 0,192
2Al(OH)3 -------> Al2O3 + 3H2O
0,225 0,1125
4Fe(OH)2 + O2 ------> 2Fe2O3 + 4H2O
0,108 0,054
m= 0,192 . 40 + 0,1125 . 102 + 0,054 . 160 = 27,795 (g)

Đáp án D
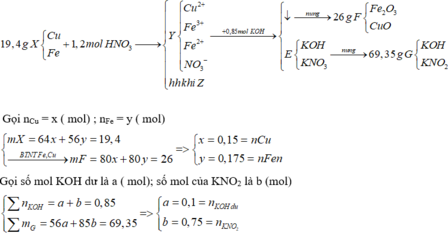
BTNT N => nN(trong Z) = nHNO3 – nNO3- = 1,2 – 0,75 = 0,45 (mol)
Ta thấy 3nFe + 2nCu = 0,875 > nNO3- = 0,75 => sản phẩm trong Y có cả Fe2+, Fe3+. HNO3 đã phản ứng hết
ne(nhường) = 3nFe3+ + 2nFe2+ + 2nCu2+ = nKOH pư = b = 0,75 (mol)
=> trung bình mỗi N+5 đã nhận 0,74/0,45 = 5/3 (electron)
=> NO2 : z ( mol) và NO: t (mol)
=> z + t = 0,45
=> Vhh Z = 0,45.22,4 = 10,08 (lít) gần nhất với 11,02 lít

Fe+4HNO3\(\rightarrow\)Fe(NO3)3+NO+2H2O
3M+8HNO3\(\rightarrow\)3M(NO3)2+2NO+4H2O
2Fe(NO3)3\(\rightarrow\)Fe2O3.......
M(NO3)2\(\rightarrow\)MO.....
Fe+H2SO4\(\rightarrow\)FeSO4+H2
M+H2SO4\(\rightarrow\)MSO4+H2
\(n_{H_2}=0,01mol\)
mO=1,6-1,2=0,4g\(\rightarrow\)nO=0,025mol
nO>nH2 suy ra M không tác dụng H2SO4
nFe=nH2=0,01mol
Gọi y là số mol M
56.0,01+My=1,2 suy ra My=0,64(1)
160.0,01/2+(M+16)y=1,6
(M+16)y=0,8(2)
từ (1) và (2) ta có: M+16=1,25M suy ra M=64(Cu)
b) y=0,64:64=0,01mol
dd B có: Fe(NO3)3: 0,01mol và Cu(NO3)2: 0,01mol
\(m_{Fe\left(NO_3\right)_3}=0,01.242=2,42g\)
\(m_{Cu\left(NO_3\right)_2}=0,01.188=1,88g\)
Fe+Ag2SO4\(\rightarrow\)FeSO4+2Ag(1)
Cu+Ag2SO4\(\rightarrow\)CuSO4+2Ag(2)
nAg(1)=2nFe=0,02mol\(\rightarrow\)mAg=0,02.108=2,16g
nAg(2)=2nCu=0,02mol\(\rightarrow\)mAg=0,02.108=2,16g
2,16+2,16=4,32>3,56g vậy phản ứng (2) Cu còn dư
D(Ag,Cu dư)
gọi số mol Cu phản ứng (2) là x
nAg=0,02+2x
nCu dư=0,01-x
108(0,02+2x)+64(0,01-x)=3,56 suy ra x=0,005
D( Ag: 0,03mol; Cu: 0,005 mol)
%Ag=\(\dfrac{0,03.108.100}{3,56}\approx91\%\)
%Cu=9%

Đáp án A
Chất rắn B nguyên chất nên B là Cu
=> Fe và Zn phản ứng hết.
G là ZnO


Đáp án cần chọn là: A
Các chất có phản ứng tạo ra chất mới ở thể rắn và khí thì chất đó sẽ có khối lượng rắn nhỏ hơn.
Đặt số mol mỗi chất đem nung là 1 mol
Các chất khi nhiệt phân thu được rắn có khối lượng nhỏ hơn là: N a H C O 3 , N a N O 3 , F e O H 3 , F e S 2
2 N a H C O 3 r → t ° N a 2 C O 3 r + C O 2 ↑ k + H 2 O h
2 N a H C O 3 r → t ° 2 N a C O 2 r + O 2 k
2 F e O H 3 r → t ° F e 2 O 3 r + 3 H 2 O h
2 F e S 2 r + 11 O 2 → t ° 2 F e 2 O 3 r + 8 S O 2 k
→ có 4 chất