Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

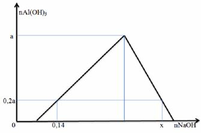
Vì nAl(OH)3 max = a → nAlCl3 = a
Giả sử số mol của AlCl3 và HCl trong mỗi phần là a, b
Bảo toàn Cl: 3a + b = 0,5 (1)
HCl + NaOH → NaCl + H2O
b → b
– Tại nNaOH = 0,14: kết tủa đang lên max (chưa bị hòa tan)
AlCl3 + 3NaOH → Al(OH)3↓ + 3NaCl
0,6a ← 0,2a
=> b + 0,6a = 0,14 (2)
Từ (1) và (2) => a = 0,15 và b = 0,05
– Tại nNaOH = x: kết tủa bị hòa tan một phần
Al(OH)3 + NaOH → NaAlO2 + 2H2O
0,12 → 0,12
Dư: 0,03
→ x = 0,05 + 3.0,15 + 0,12 = 0,62 (mol)
Vậy x = 0,62

$KHCO_3 + 2HCl \to KCl +CO_2 + H_2O$
$CaCO_3 + 2HCl \to CaCl_2 + CO_2 + H_2O$
$CO_2 + Ba(OH)_2 \to BaCO_3 + H_2O$
$CO_2 + 2Ba(OH)_2 \to Ba(HCO_3)_2$
TH1 : $Ba(OH)_2$ dư
$n_{CO_2} = n_{BaCO_3} = 0,1(mol)$
$M_{KHCO_3} = M_{CaCO_3} = 100(g/mol)$
Suy ra:
$m = 0,1.100 = 10(gam)$
TH2 : Kết tủa tan 1 phần
$n_{Ba(HCO_3)_2} = n_{Ba(OH)_2} - n_{BaCO_3} = 0,05(mol)$
$n_{CO_2} = 2n_{Ba(HCO_3)_2} + n_{BaCO_3} = 0,2(mol)$
$m = 0,2.100 = 20(gam)$

Hỗn hợp khí B gồm CO và CO2 khi tác dụng với dd chứa 0,025 mol Ca(OH)2 chắc chắc tạo 2 muối
Ta có: \(n_{CaCO_3}=\dfrac{2}{100}=0,02\left(mol\right)\)
PTHH: \(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3\downarrow+H_2O\)
0,02______0,02______0,02 (mol)
\(2CO_2+Ca\left(OH\right)_2\rightarrow Ca\left(HCO_3\right)_2\)
0,01_____0,005_______0,005 (mol)
\(\Rightarrow n_{CO_2}=0,03\left(mol\right)\) \(\Rightarrow m_{CO_2}=0,03\cdot44=1,32\left(g\right)\)
Bảo toàn nguyên tố: \(n_{CO\left(p/ứ\right)}=n_{CO_2}=0,03\left(mol\right)\) \(\Rightarrow m_{CO}=0,03\cdot28=0,84\left(g\right)\)
Bảo toàn khối lượng: \(m_A=m_{oxit}+m_{CO}-m_{CO_2}=1,12\left(g\right)\)
PTHH: \(2A+2zHCl\rightarrow ACl_z+zH_2\uparrow\) (z là hóa trị của A)
Ta có: \(n_{H_2}=\dfrac{0,448}{22,4}=0,02\left(mol\right)\)
\(\Rightarrow n_A=\dfrac{0,04}{z}\left(mol\right)\) \(\Rightarrow M_A=\dfrac{1,12}{\dfrac{0,04}{z}}=28z\)
Ta thấy với \(z=2\) thì \(M_A=56\) \(\Rightarrow\) Kim loại A là Fe
Gọi công thức oxit cần tìm là FexOy
Bảo toàn Oxi: \(n_{O\left(oxit\right)}=2n_{CO_2}-n_{CO}=0,03\left(mol\right)\)
Xét tỉ lệ \(x:y=0,02:0,03=2:3\)
Vậy công thức oxit là Fe2O3

Gọi $n_{Na_2CO_3\ pư} = 0,1a(mol) ; n_{NaHCO_3\ pư} = 0,3a(mol)$
$Na_2CO_3 + H_2SO_4 \to Na_2SO_4 + CO_2 + H_2O$
$2NaHCO_3 + H_2SO_4 \to Na_2SO_4 + 2CO_2 + 2H_2O$
Theo PTHH :
$n_{H_2SO_4} = 0,1a + 0,3a.0,5 = 0,15 \Rightarrow a = 0,6$
$n_{CO_2} = 0,1a + 0,3a = 0,24(mol)$
Bảo toàn C :
$n_{BaCO_3} = 0,1 + 0,3 - 0,24 = 0,16(mol)$
Bảo toàn S :
$n_{BaSO_4} = n_{H_2SO_4} = 0,15(mol)$
Suy ra :
$m_{ktua} = 0,16.197 + 0,15.233 = 66,47(gam)$

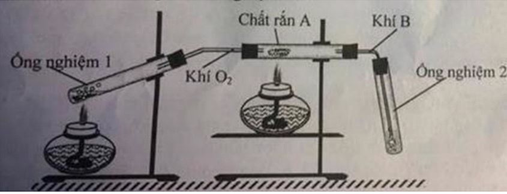
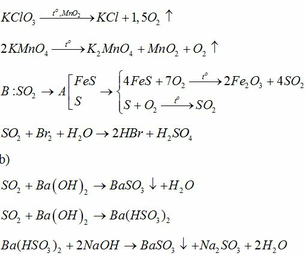

Do ở 2 TN, lượng CO2 thu được khác nhau
=> HCl hết trong cả 2 TN
TN1:
Na2CO3 + HCl --> NaCl + NaHCO3
a----------->a---------------->a
NaHCO3 + HCl --> NaCl + CO2 + H2O
________(b-a)------------->(b-a)
=> nCaCO3(TN1) = nCO2(TN1) = b-a (mol)
TN2:
Na2CO3 + 2HCl --> 2NaCl + CO2 + H2O
__________b------------------>0,5b
=> nCaCO3(TN2) = nCO2(TN2) = 0,5b
Do mCaCO3(TN1) = m; mCaCO3(TN2) = 2m
=> 2. nCaCO3(TN1) = nCaCO3(TN2)
=> 2(b-a) = 0,5b
=> 2b - 2a = 0,5b
=> 2a = 1,5b
=> a : b = 3 : 4