Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Bài 7:
\(n_{Fe}=\dfrac{1000}{55,85}\left(mol\right)\)
Trong 1 kg sắt thì khối lượng electron là:
\(m_e=\dfrac{1000}{55,85}.26.9,1094.10^{-28}\approx4240,723.10^{-28}\left(g\right)\approx4240,723.10^{-31}\left(kg\right)\)
Bài 8:
\(m_{Ne}=20,179.0,16605.10^{-23}=3,35072295.10^{-23}\left(g\right)\)

\(m_F=1,6605.10^{-27}.18,998=31,546179.10^{-27}\left(kg\right)\)

\(m_{Ne}=20,179.0,16605.10^{-23}\\ =3,35072295.10^{-23}\left(g\right)=3,35072295.10^{-26}\left(kg\right)\)
\(m_N=14,007.0,16605.10^{-23}\\ =2,32586235.10^{-23}\left(g\right)=2,32586235.10^{-26}\left(kg\right)\)
\(m_{Mg}=24,305.0,16605.10^{-23}\\ =4,03584525.10^{-23}\left(g\right)=4,03584525.10^{-26}\left(kg\right)\)
\(m_{Fe}=55,845.0,16605.10^{-23}\\ =9,27306225.10^{-23}\left(g\right)=9,27306225.10^{-26}\left(kg\right)\)
Khí neon có hai đồng vị biết nguyên tử khối trung bình của neon là 20,18 tính phần trăm từng đồng vị


\(KL_{Ne}=20,179\times0,16605\times10^{-23}=3,3507\times10^{-23}\left(g\right)=3,3507\times10^{-26}\left(kg\right)\)

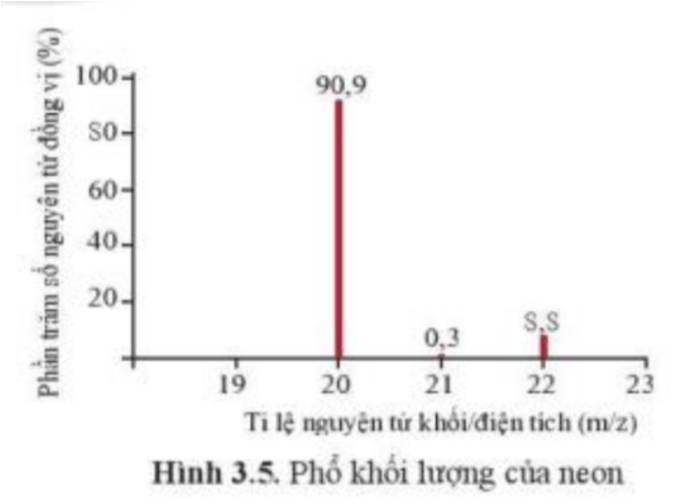
a) Neon có 3 đồng vị bền:
+ Đồng vị 20Ne chiếm 90,9%
+ Đồng vị 21Ne chiếm 0,3%
+ Đồng vị 22Ne chiếm 8,8%
b) Công thức tính nguyên tử khối trung bình: \(M = \frac{{aA + bB + cC + {\text{dD}} + ...}}{{100}}\)
=> \({M_{Ne}} = \frac{{90,9.20 + 0,3.21 + 8,8.22}}{{100}} = 20,18\)
Vậy nguyên tử khối trung bình của Neon là 20,18.

Ta có: ZM + ZX = (142 + 42) : 4 = 46.
2ZM – 2ZX = 12 (tổng số hạt mang điện là 2Z)
Dễ dàng tìm được ZM = 26, ZX = 20. Vậy M là Fe, X là Ca.
c) Áp dụng mở rộng công thức trên trong giải ion
Ø Nếu ion là Xx+ thì ZX = (S + a + 2x) : 4
Ø Nếu ion Yy- thì ZY = (S + a – 2y) : 4
Vậy khác biệt của công thức này với công thức ban đầu đó là thêm giá trị của điện ion (cách nhớ: nếu ion +, thì đem + 2 lần giá trị điện ion, nếu âm thì – 2 lần giá trị điện ion âm)
- 1u = 1.6605*10-27 kg nhé bạn.
- MNe = 20.179u = 20.179 * 1.6605*10-27 = 3.3507*10-26 kg