Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

3) đầu tiên bạn viết PTHH đi:Na2CO3 + 2HCL - 2NaCl + H2O + Co2
nNa2CO3=1.886mol
nHCL=3.287mol
chú ý nha số ko dc chẳng nên mình lấy đến phần nghìn nhé!
Bạn suy ra dc số Na2CO3 dư, tính theo số mol HCl
mNaCL=192.2895g
m Na2Co3 (dư)=25.705g
khối lượng dd:200+120=320g
C% củ từng chất:Na2Co3=8%
NaCl=60%
Gọi côg thức hoá học của oxit Kim loại hoá trị 3 là X2O3
X2O3 + 3H2SO4 -----------> X2(SO4)3 + 3H2O
Khối lượng dd X2(SO4)3 sau PƯ là
m(dd)X2(SO4)3 = 10,2 + 331,8 = 342 (g)
Khối lượng chất tan X2(SO4)3 sau PƯ là
m(ct>X2(SO4)3 = 342 . 10 : 100 = 34,2 (g)
Theo pt PƯ : nX2O3 = nX2(SO4)3
=> 10,2 trên (2Mx+48) = 34,2 trên (2Mx + 288)
=> 34,2 .( 2Mx + 48 ) = 10,2 .(2Mx +288)
=> 68,4Mx + 1641,6 = 20,4Mx + 2937,6
=> 48Mx = 1296
=> Mx = 27
Do đó kim loại X là Al
Côg thức hoá học của oxit kim loại là Al2O3
b, Số mol của Al2O3 là
nAl2O3 = 10,2 : 102 = 0,1 (mol)
Theo pt PƯ nAl2O3 = 3nH2SO4
=>nH2SO4 = 0,3 (mol)
Khối lượng của H2SO4
mH2SO4 = 0,3 . 98 = 29,4 (g)
Phần trăm dung dịch của axit H2SO4
C%(dd)H2SO4 = 29,4 : 331,8 .100% ~ 8.87%

Bạn ơi đề không rõ ràng gì hết
theo mình 3,36 là mdung dịch trước phản ứng và mdung dịch sau phản ứng = 3,08 gam thì mới ra Mg
=> mH2 = 3,36 - 3,08 = 0,28
=> nH2 = \(\dfrac{0,28}{2}\) = 0,14 ( mol )
2X + 2nHCl \(\rightarrow\) 2XCln + nH2
\(\dfrac{0,28}{n}\)...........................0,14
=> \(\dfrac{0,28}{n}=\dfrac{3,36}{M_X}\)
=> vì n là hóa trị của kim loại
=> 1 \(\le\) n \(\le\) 3
| n | 1 | 2 | 3 |
| MX | 12 | 24 | 36 |
| loại | nhận | loại |
=> X là Mg

Giả sử KL có hóa trị n.
Ta có: mKL + mSO4 = m muối
⇒ mSO4 = 2,4 (g) \(\Rightarrow n_{H_2}=n_{H_2SO_4}=n_{SO_4}=\dfrac{2,4}{96}=0,025\left(mol\right)\)
BT e, có: n.nKL = 2nH2 \(\Rightarrow n_{KL}=\dfrac{0,05}{n}\left(mol\right)\)
\(\Rightarrow M_{KL}=\dfrac{1,4}{\dfrac{0,05}{n}}=28n\left(g/mol\right)\)
Với n = 2 thì M = 56 (g/mol) là thỏa mãn.
Vậy: KL cần tìm là sắt (Fe).

B1:
Gọi kim loại cần tìm là R
PTHH
2R+ xH2SO4----->R2(SO4)x +xH2
Ta có
n\(_{H2}=\frac{4,48}{22,4}=0,2\left(mol\right)\)
Theo pthh
n\(_R=\frac{2}{x}n_{H2}=\frac{0,4}{x}\left(mol\right)\)
M\(_R=\frac{4,48}{0,4:x}=\frac{11,2}{x}\left(\frac{g}{mol}\right)\)
Ta có
| x | 1 | 2 | 3 |
| M\(_R\) | 11,2 | 5,6 | 3,7 |
Bạn xem lại đề thử nhé

nZn= 0,1 mol ; nH2SO4= 0,2 mol
a) Zn + H2SO4 → ZnSO4 + H2↑
ban đầu: 0,1 mol 0,2 mol
PƯ: 0,1 mol 0,1 mol 0,1 mol 0,1 mol
b) VH2 = 0,1 x 22,4 = 2,24 (l)
c) Dung dịch có: 0,1 mol ZnSO4 và 0,1 mol H2SO4 dư
mdung dịch = mZn + mdung dịch H2SO4 - mH2 = 6,5 + 200 - 0,1 x 2 = 206,3 (g)
%ZnSO4 = 0,1 x 161 : 206,3 x 100% = 7,80%
%H2SO4= 0,1 x 98 : 206,3 x 100% = 4,75%
\(n_{H_2SO_4}=0,1\cdot0,15=0,015mol\)
\(A+H_2SO_4\rightarrow ASO_4+H_2\)
0,015 0,015
Mà \(n_A=\dfrac{m_A}{M_A}=\dfrac{0,975}{M_A}=0,015\Rightarrow n_A=65\left(đvC\right)\)
\(\Rightarrow\) A là nguyên tố Zn(kẽm).

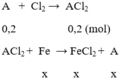
số mol FeCl2 là n = 0,25 . 0,4 = 0,1 (mol)
gọi x là số mol Fe phản ứng
khối lượng kim loại tăng là Δm = mA - mFe = Ax – 56x = 0,8
x = 0,1 → A.0,1 – 56.0,1 = 0,8 → A = 64. A là Cu
số mol Cu là nCu = 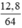 = 0,2 (mol)
= 0,2 (mol)
số mol CuCl2 → n(CuCl2) = nCu = 0,2 (mol)
nồng độ mol/l CuCl2 là C(M(CuCl2)) = 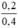 = 0,5M
= 0,5M

2A+6HCl->2ACl3+3H2
0,2----0,6------------0,3 mol
n H2=\(\dfrac{6,72}{22,4}\)=0,3 mol
=>\(\dfrac{5,4}{A}\)=0,2
=>A=27 g\mol
=>A là nhôm (Al)
CMHCl=\(\dfrac{0,6}{0,5}\)=1,2M
\(5,4gA+500mlHCl->X:ACl3+6,72lH2\)
nH2 = 0,3 ( mol )
=> nAl = 2/3.nH2 = 0,2 ( mol )
( Cân bằng PTHH )
Ta có :
M = \(\dfrac{5,4}{0,2}=27\left(\dfrac{g}{mol}\right)\)
=> Đó là Al
\(n_R=\dfrac{5,4}{R}\left(mol\right)\)
\(2R\left(\dfrac{5,4}{R}\right)+3H_2SO_4\left(\dfrac{8,1}{R}\right)\rightarrow R_2\left(SO_4\right)_3\left(\dfrac{2,7}{R}\right)+3H_2\left(\dfrac{8,1}{R}\right)\)
Theo PTHH \(n_{R_2\left(SO_4\right)_3}=\dfrac{2,7}{R}\left(mol\right)\)
\(\Rightarrow m_{R_2\left(SO_4\right)_3}=\dfrac{2,7.\left(2R+288\right)}{R}\left(g\right)\) \(\left(1\right)\)
\(n_{H_2}=\dfrac{8,1}{R}\left(mol\right)\)
\(\Rightarrow m_{H_2}=\dfrac{16,8}{R}\left(g\right)\)
\(m_{ddsau}=5,4+395,2-\dfrac{16,8}{R}\left(g\right)\)
Theo đề dung dịch muối sau phản ứng có nồng độ 8,55%
\(\Rightarrow8,55=\dfrac{\dfrac{2,7.\left(2R+288\right)}{R}}{5,4+395,2-\dfrac{16,8}{R}}.100\)
\(\Rightarrow R=27\left(Al\right)\)
Theo PTHH: \(n_{H_2SO_4}=\dfrac{8,1}{R}=\dfrac{8,1}{27}=0,3\left(mol\right)\)
\(\Rightarrow m_{H_2SO_4}=29,4\left(g\right)\)
\(\Rightarrow C\%_{H_2SO_4}\left(bđ\right)=\dfrac{29,4}{395,2}.100=7,44\%\)