Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đổi : 600ml=0,6l
\(n_{N2O}+n_{NO}=\frac{3,36}{22,4}=0,15\left(mol\right)\)
\(\frac{d_{N2O,NO}}{kk}=1,195\)
\(\rightarrow M_{N2O,NO}=34,655\)
\(\rightarrow44n_{N2O}+30n_{NO}=34,655.0,15=5,19825\left(2\right)\)
(1)(2) \(\rightarrow n_{N2O}=0,05,n_{NO}=0,1\)
\(3n_{Fe}+2n_{Mg}=0,7\)
\(56n_{Fe}+24n_{Mg}=10,4\)
\(\rightarrow n_{Fe}=0,1\left(mol\right),n_{Mg}=0,2\left(mol\right)\)
\(n_{Fe}=nFe\left(NO_3\right)_3,n_{Mg}=nMg\left(NO_3\right)_2\)
\(\rightarrow n_{HNO3}=2n_{Mg\left(NO3\right)2}+3n_{Fe\left(NO3\right)3}+n_{NO}+n_{N2O}\)
\(=0,2.2+0,1.3+0,1+0,05.2=0,9\left(mol\right)\)
\(\rightarrow CM_{HNO3}=\frac{0,9}{0,6}=1,5M\)

Gọi: nFe = nCu = x (mol)
⇒ 56x + 64x = 12 ⇒ x = 0,1 (mol)
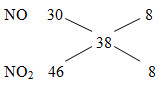
Gọi: \(\left\{{}\begin{matrix}n_{NO}=a\left(mol\right)\\n_{NO_2}=b\left(mol\right)\end{matrix}\right.\)
BT e, có: 3nFe + 2nCu = 3nNO + nNO2
⇒ 3a + 2b = 0,5 (1)
Mà: Tỉ khối của X với H2 là 19.
\(\Rightarrow\dfrac{30a+46b}{a+b}=19.2\left(2\right)\)
Từ (1) và (2) ⇒ a = b = 0,1 (mol)
\(\Rightarrow V_{hh}=\left(0,1+0,1\right).22,4=4,48\left(l\right)\)

Có \(A\left\{{}\begin{matrix}n_{SO_2}+n_{O_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\\\dfrac{64.n_{SO_2}+32.n_{O_2}}{n_{SO_2}+n_{O_2}}=25,6.2=51,2\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}n_{SO_2}=0,3\left(mol\right)\\n_{O_2}=0,2\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}\%V_{SO_2}=\dfrac{0,3}{0,5}.100\%=60\%\\\%V_{O_2}=\dfrac{0,2}{0,5}.100\%=40\%\end{matrix}\right.\)
Gọi số mol SO2 phản ứng là x (mol)
PTHH: 2SO2 + O2 --> 2SO3
Trc pư: 0,3 0,2 0
Pư: x------>0,5x------>x
Sau pư: (0,3-x) (0,2-0,5x) x
=> \(M_B=\dfrac{m_B}{n_B}=\dfrac{m_A}{n_B}=\dfrac{25,6}{\left(0,3-x\right)+\left(0,2-0,5x\right)+x}=32.2=64\)
=> x = 0,2
=> \(B\left\{{}\begin{matrix}SO_2:0,1\left(mol\right)\\O_2:0,1\left(mol\right)\\SO_3:0,2\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}\%V_{SO_2}=\dfrac{0,1}{0,1+0,1+0,2}.100\%=25\%\\\%V_{O_2}=\dfrac{0,1}{0,1+0,1+0,2}.100\%=25\%\\\%V_{SO_3}=\dfrac{0,2}{0,1+0,1+0,2}.100\%=50\%\end{matrix}\right.\)
- Xét hỗn hợp khí A:
Gọi x,y lần lượt là số mol của SO2 và O2 trong hỗn hợp. (x,y>0) (mol)
\(x+y=\dfrac{11,2}{22,4}=0,5\left(1\right)\\ Mà:M_A=25,6.M_{H_2}=25,6.2=51,2\left(\dfrac{g}{mol}\right)\\ \Leftrightarrow\dfrac{64x+32y}{0,5}=51,2\\ \Leftrightarrow64x+32y=25,6\left(2\right)\\ \left(1\right),\left(2\right)\Rightarrow\left\{{}\begin{matrix}x+y=0,5\\64x+32y=25,6\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,3\\y=0,2\end{matrix}\right.\\ \Rightarrow\%V_{\dfrac{SO_2}{A}}=\dfrac{0,3}{0,5}.100=60\%\Rightarrow\%V_{\dfrac{O_2}{A}}=100\%-60\%=40\%\)
- Xét hỗn hợp khí B:
Gọi a là số mol SO3 được tạo thành trong hhB (mol) (a,b>0)
\(PTHH:2SO_2+O_2\rightarrow\left(xt,t^o\right)2SO_3\\ \Rightarrow n_{SO_2\left(hhB\right)}=0,3-a\left(mol\right)\\ n_{O_2\left(hhB\right)}=0,2-0,5a\left(mol\right)\\ M_{hhB}=32.M_{H_2}=32.2=64\left(\dfrac{g}{mol}\right)\\ \Leftrightarrow\dfrac{80a+\left(0,2-0,5a\right).32+\left(0,3-a\right).64}{a+\left(0,2-0,5a\right)+\left(0,3-a\right)}=64\\ \Leftrightarrow a=0,2\\ \Rightarrow hhB\left\{{}\begin{matrix}SO_3:0,2\left(mol\right)\\SO_2:0,1\left(mol\right)\\O_2:0,1\left(mol\right)\end{matrix}\right.\\ \Rightarrow\%V_{\dfrac{SO_3}{hhB}}=\dfrac{0,2}{0,2+0,1+0,1}.100=50\%\\ \%V_{\dfrac{SO_2}{hhB}}=\%V_{\dfrac{O_2}{hhB}}=\dfrac{0,1}{0,2+0,1+0,1}.100=25\%\)
Em xem có gì không hiểu thì hỏi lại nhá!

MX= 19.2=38
=> nN2=nNO2=x
mFe + mO = moxit
=> mO = moxit- mFe = 7,36-5,6=1,76 gam
=> nO = 0,11 mol
Fe0 →Fe3+ + 3e
0,1 0,3
O0 +2e →O2- N+5 + 3e → N+2 N+5 +1e → N+4
0,11 0,22 3x x x x
Bảo toàn e: 0,3 = 0,22+3x+x =0,22+4x =>x= 0,02
=> nkhí = 2x=0,04 mol
=> Vkhí = 0,04.22,4=0,896 lít=896 ml

\(Fe\left(x\right)+2HCl\left(2x\right)\rightarrow FeCl_2+H_2\left(x\right)\)
\(M\left(y\right)+2HCl\left(2y\right)\rightarrow MCl_2+H_2\left(y\right)\)
Gọi số mol của Fe, M lần lược là x,y thì ta có
\(56x+My=4\left(1\right)\)
\(n_{H_2}=\frac{2,24}{22,4}=0,1\)
\(\Rightarrow x+y=0,1\left(2\right)\)
Nếu chỉ dùng 2,4 g M thì
\(n_{HCl}=2n_M=\frac{2.2,4}{M}=\frac{4,8}{M}< 0,5\left(3\right)\)
Từ (1), (2), (3) ta có hệ: \(\left\{\begin{matrix}56x+My=4\\x+y=0,1\\\frac{4,8}{M}< 0,5\end{matrix}\right.\)
\(\Leftrightarrow\left\{\begin{matrix}56\left(0,1-y\right)+My=4\\x=0,1-y\\\frac{4,8}{M}< 0,5\end{matrix}\right.\)
\(\Leftrightarrow\left\{\begin{matrix}y\left(56-M\right)=1,6\\x=0,1-y\\M>9,6\end{matrix}\right.\)
\(\Rightarrow9,6< M< 56\)
Tới đây thì chọn kim loại nào có hóa trị II mà nằm trong khoản đó và kiểm tra thỏa mãn hệ phương trình là xong.
Hung Nguyen: giải thích hộ mình ở chỗ dấu ngoặc nhọn thứ 2 đc ko. mình ko hiểu từ dấu ngoặc nhọn thứ nhất làm thế nào để ra đc dấu ngoặc nhọn thứ 2. cảm ơn trước nha ![]()

Ta có: \(\left\{{}\begin{matrix}n_{HCl}=0,796.0,5=0,398\left(mol\right)\\n_{H_2SO_4}=0,796.0,75=0,597\left(mol\right)\end{matrix}\right.\)
\(n_{H_2}=\dfrac{4,368}{22,4}=0,195\left(mol\right)\)
BTNT H, có: \(n_{HCl}+2n_{H_2SO_4}=2n_{H_2}+2n_{H_2O}\Rightarrow n_{H_2O}=0,601\left(mol\right)\)
Theo ĐLBT KL, có: m hh + m axit = m muối + mH2 + mH2O
⇒ m = m muối = 26,43 + 0,398.36,5 + 0,597.98 - 0,195.2 - 0,601.18 = 88,255 (g)

Bài 1:
PTHH: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
\(Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\)
Ta có: \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)=n_{Fe}\)
\(\Rightarrow\%m_{Fe}=\dfrac{0,1\cdot56}{37,6}\cdot100\%\approx14,89\%\)
\(\Rightarrow\%m_{Fe_2O_3}=85,11\%\)
Bài 3:
PTHH: \(2HNO_3+Ba\left(OH\right)_2\rightarrow Ba\left(NO_3\right)_2+2H_2O\)
Ta có: \(\left\{{}\begin{matrix}n_{HNO_3}=0,05\cdot1=0,05\left(mol\right)\\n_{Ba\left(OH\right)_2}=\dfrac{342\cdot5\%}{171}=0,1\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,05}{2}< \dfrac{0,1}{1}\) \(\Rightarrow\) Axit p/ứ hết, Bazơ còn dư sau p/ứ
\(\Rightarrow\) Dung dịch sau p/ứ làm quỳ tím hóa xanh
Theo PTHH: \(n_{Ba\left(NO_3\right)_2}=\dfrac{1}{2}n_{HNO_3}=0,025\left(mol\right)\) \(\Rightarrow m_{Ba\left(NO_3\right)_2}=0,025\cdot261=6,525\left(g\right)\)