K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.
Các câu hỏi dưới đây có thể giống với câu hỏi trên

6 tháng 10 2018
Chọn B.
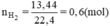
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2 ↓
Al2O3 + 2NaOH → 2NaAlO2 + H2O
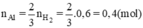
⇒ mAl = 27.0,4 = 10,8 (gam); mAl2O3 = 31,2 - 10,8 = 20,4 (gam).

22 tháng 8 2019
Đáp án A
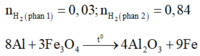
Vì phần 1 tác dụng với dung dịch NaOH có xuất hiện khí nên trong Y có Al dư.
Do đó Y gồm Fe, A12O3 và Al.

Khi cho phần 1 tác dụng với dung dịch NaOH dư có:
n Al = 2 3 n H 2 ⇒ a = 0 , 02
Khi cho phần 2 tác dụng với dung dịch HC1 dư:

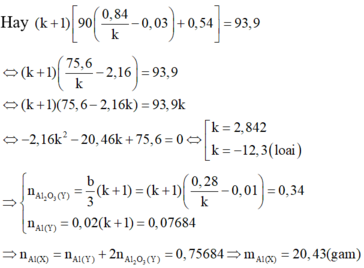
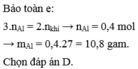
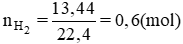
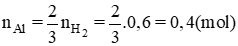

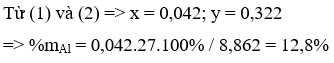

Cho 31,2 gam hỗn hợp bột Al và AL2O3 tác dụng với dung dịch NaOH dư thoát ra 13,44 lít khí phần trăm khối lượng của Al trong hỗn hợp ban đầu
2Al(x)+2H2O+2NaOH→3H2(1,5x)+2NaAlO2
Al2O3+2NaOH→H2O+2NaAlO2
Gọi số mol của Al và Al2O3 lần lược là x, y
⇒27x+102y=31,2(1)
nH2=13,44\22,4=0,6(mol
⇒1,5x=0,6(2)⇒1,5x=0,6(2)
Từ (1) và (2) ta có hệ:
{27x+102y=31,2
1,5x=0,6
⇔{x=0,4y=0,2
⇔{mAl=0,4.27=10,8
mAl2O3=0,2.102=20,4
bạn tính % ra nha