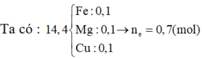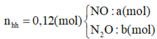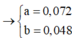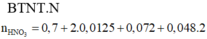Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án : B
X + O2 vừa đủ => Z : NO2 ; N2O ; N2
=> khí T gồm N2O và N2 có M = 40g và n = 0,2 mol
=> nN2O = 0,15 ; nN2 = 0,05 mol
=> nNO = nX – nT = 0,1 mol
NaOH + Y => kết tủa lớn nhất gồm Mg(OH)2 và Al(OH)3
=> mkết tủa – mKL = 39,1 = mOH => nOH = 2,3 mol
Vì nAl : nMg = 5 : 4 => nAl = 0,5 ; nMg = 0,4 mol
Bảo toàn e : 2nMg + 3nAl = 3nNO + 8nN2O + 10nN2 + 8nNH4NO3
=> nNH4NO3 = 0,0375 mol
=> nHNO3 pứ = 10nNH4NO3 + 4nNO + 10nN2O + 12nN2 = 2,875 mol
Thực tế lầy dư axit 20% so với phản ứng => nHNO3 đầu = 3,45 mol
=> mdd HNO3 đầu = 1086,75g
Bảo toàn khối lượng : mKL + mdd HNO3 = mdd sau + mkhí
=> mdd sau = 1098,85g
=> C%Al(NO3)3 = 9,69%

Đáp án : D
Vì %V của N2 và NO2 bằng nhau => Qui đổi về NO và N2O
Coi hỗn hợp gồm NO và N2O với tổng số mol = 0,5 và MZ = 35,6g.
Áp dụng qui tắc đường chéo ta có : nNO = 0,3 mol ; nN2O = 0,2 mol
, nHNO3 = 4nNO + 10nN2O = 4.0,3 + 10.0,2 = 3,2 mol

Đáp án : A
Y có %VN2 = %VNO2 => qui 2 khí này về NO và N2O => Y có N2O và NO có M = 35,6g và nY = 0,5 mol => nNO = 0,3 ; nN2O = 0,2 mol
,nHNO3 pứ = 4nNO + 10nN2O = 3,2 mol

Đáp án : B
n hh X = 6,72: 22,4 = 0,3 mol
n hh Z = 4,48 : 22,4 = 0,2 mol
M ¯ hh Z = 20.2 = 40
Z gồm N2 và N2O
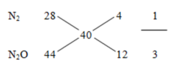
=> n N2 = 0,05 mol
n N2O = 0,15 mol
=> n NO = n X – n Z = 0,1 mol
Mặt khác, có hh A (Mg, Al) => Kết tủa chứa Al(OH)3 và Mg(OH)2
m → m+ 39,1
Gọi n Mg = a mol => n Al = 1,25a mol
m hh A = 24a + 33,75a = 57,75 a = m
m↓ = 58a + 97,5 a = 57,75a + 39,1
<=> a = 0,4 mol
=> n Mg = 0,4; n Al = 0,5 mol
Mg → Mg+2 + 2e
0,4 0,8
Al → Al+3 + 3e
0,5 1,5
N+5 + 10e → N2
0,5 0,05
N+5 + 8e → N-3
8a a
N+5 + 3e → N+2
0,3 0,1
2N+5 + 8e → N2O
1,2 0,15
Bảo toàn electron, ta có: 0,8 + 1,5 = 0,3 + 1,2 + 0,5 + 8a
<=> 8a = 0,3
<=> a = 0,0375 mol
=> ∑ n HNO3p.ư = n NO3 – (muối của KL) + n N(sp khử) + 2 n NH4NO3
= 2,3 + 0,1 + 0,15. 2 + 0,05. 2 + 0,0375. 2
= 2,875 mol
=> n HNO3 t.t = 3,45 mol => mdd HNO3 = (3,45. 63)/ 0,2 = 1086,75 g
=> m dd sau p.ư = m KL + m HNO3 – n khí
= 0,4. 24 + 0,5. 27 + 1086,75 – 0,1. 30 – 0,05. 28 – 0,15. 44
= 1098,85 gam
C% Al(NO3)3 = 106,5 : 1098,85 = 9,7%

Đáp án : D
.nX = 0,3 mol ; nZ = 0,2 mol
Chỉ có NO phản ứng với O2 tạo NO2 bị hấp thụ vào nước
=> nNO = 0,3 – 0,2 = 0,1 mol
MZ= 40g (Z gồm N2 và N2O )
=> nN2 = 0,05 mol ; nN2O = 0,15 mol
.m(g) P : Mg,Al -> Kết tủa lớn nhất : Mg(OH)2 ; Al(OH)3 : (m + 39,1)g
=> mOH = (m + 39,1) – m = 39,1g => nOH = 2,3 mol = 2nMg + 3nAl
Lại có : nMg : nAl = 4 : 5 => nMg = 0,4 mol ; nAl = 0,5 mol
Bảo toàn e : 2nMg + 3nAl = 10nN2 + 8nN2O + 3nNO + 8nNH4NO3
=> nNH4NO3 = 0,0375 mol
=> Bảo toàn N : nHNO3 pứ = 2nMg + 3nAl + 2nN2 + nNO + 2nN2O + 2nNH4NO3
=> nHNO3 pứ = 2,875 mol
=> nHNO3 đầu = 3,45 mol => mdd HNO3 = 1086,75g
=> mdd sau = mP + mdd HNO3 - mkhí = 1098,85g
=> %CAl(NO3)3 = 9,69%

Chọn đáp án D
gt ⇒ nFe = nMg = nCu = 0,1 mol || N2 = nNO2 ⇒ ghép: N2 + NO2 = N3O2 = N2O.NO = N2O + NO.
► Quy hỗn hợp khí về N2O và NO với số mol x và y || nkhí = x + y = 0,12 mol. HNO3 dư ⇒ Fe lên +3.
● mFe(NO3)3 + mMg(NO3)2 + mCu(NO3)2 = 0,1 × 242 + 0,1 × 148 + 0,1 × 188 = 57,8(g) < 58,8(g).
⇒ chứa muối NH4NO3 ⇒ nNH4NO3 = (58,8 - 57,8) ÷ 80 = 0,0125 mol. Bảo toàn electron:
3nFe + 2nMg + 2nCu = 8nN2O + 3nNO + 8NH4NO3 ⇒ 8x + 3y = 0,6 mol ||⇒ x = 0,048 mol; y = 0,072 mol.
► nHNO3 = 10nN2O + 4nNO + 10nNH4NO3 = 0,893 mol ⇒ chọn D.