Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

2 khí là NO và H2. Dễ tính NO = 0.1; H2 = 0.075
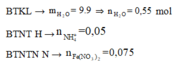
BTNT O →nZnO= 0.2
Đặt nMg = a; nAl =b.
Lập hệ → %nMg = 32%
Đáp án D

Chọn đáp án D.
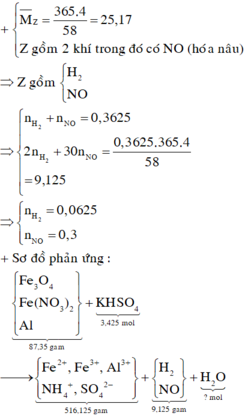
Khí hóa nâu ngoài không khí là NO.


Gần với giá trị 30 nhất.

Đáp án D
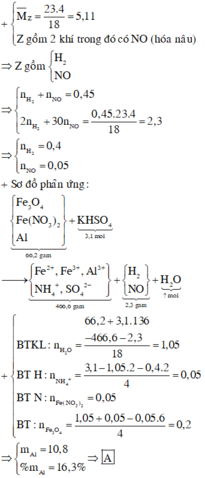
Khí hóa nâu ngoài không khí là NO.
![]() => Khí còn lại có phân tử khối < 18 => Khí còn lại là H2.
=> Khí còn lại có phân tử khối < 18 => Khí còn lại là H2.
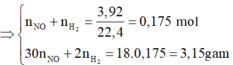
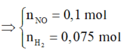
· Áp dụng bảo toàn khối lượng có:
![]()
![]()
Có:
![]()
=> Chứng tỏ có sản phẩm N H 4 + :
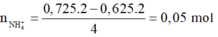
· Áp dụng bảo toàn N có: n F e ( N O 3 ) 2
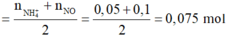
· Áp dụng bảo toàn nguyên tố O có:
![]()
![]()
· Đặt số mol của Mg, Al lần lượt là a, b
![]()
= 8,85
Vì có sản phẩm H2 tạo thành nên sau phản ứng Fe vẫn ở dạng Fe (II).
Áp dụng bảo toàn electron có:
![]()
![]()
Suy ra
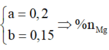
=> 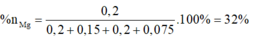
Gần với giá trị 30 nhất.

Đáp án A
Khí gồm NO x mol và H2 y mol
x+y=0,14
30x+2y=5,5.4.0,14
=>x=0,1; y=0,04
BTKL: mH2O=mX+mKHSO4--(m muối+mNO+mH2)
=>mH2O=48,165+1,68.136-(259,525+0,1.30+0,04.2)=14,04 gam=>nH2O=0,78 mol
BTNT H: nHSO4-=4nNH4+ +2nH2 + 2nH2O=>nNH4+=0,01 mol
nH+=4nNO+2nH2+10nNH4+ + 2nO
=>nO=0,55 mol=>nFe3O4=0,1375 mol
BT e: 3nAl=3nNO+2nH2+8nNH4++2nFe3O4
=>nAl=0,245 mol
=>%mAl=13,7%
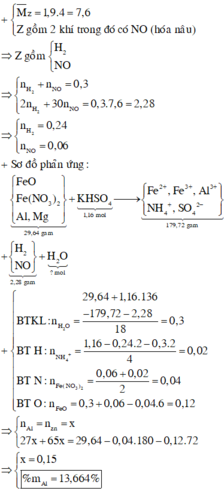


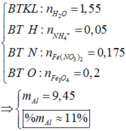


Đáp án A