Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Tổng hợp (1) và (2) ta có :
Cứ 3 x 22,4 m 3 hỗn hợp khí CO và H 2 qua Fe 2 O 3 thì thu được 2 x 56 kg Fe. 268,8 m 3 hỗn hợp khí CO và H 2 qua Fe 2 O 3 thì thu được x kg Fe.
x = 268,8 x 2 x 56/(3x22,4) = 448(kg) Fe

a) PTHH: \(Fe_2O_3+3CO\underrightarrow{t^o}2Fe+3CO_2\uparrow\)
\(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
b) Phản ứng vừa đủ
Ta có: \(n_{khí}=\dfrac{268800}{22,4}=12000\left(mol\right)\)
\(\Rightarrow n_{Fe}=\dfrac{2}{3}n_{khí}=8000\left(mol\right)\) \(\Rightarrow m_{Fe}=8000\cdot56=448000\left(g\right)=448\left(kg\right)\)
đề lạ v tận 268 800 l mà không cho khối lượng hay pư vừa đủ :vv

\(\text{mcr giảm =16x30%=4,8(g)}\)
\(\Rightarrow\text{m cr giảm=mO trong Fe2O3=4,8(g)}\)
\(\Rightarrow\text{nO=0,3(mol)}\)
\(\Rightarrow\text{nFe=11,2/56=0,2(mol)}\)
=>CTHH là Fe2O3
\(\text{b) Fe2O3+3CO}\rightarrow\text{2Fe+3CO2}\)
\(\text{nCO2=0,3(mol)}\)
\(\text{nCa(OH)2=0,2(mol)}\)
=>Tạo 2 muối
Ca(OH)2(a mol)+CO2->CaCO3+H2O
Ca(OH)2(b mol)+2CO2->Ca(HCO3)2
Ta có:
\(\left\{{}\begin{matrix}\text{a+b=0,2}\\\text{a+2b=0,3}\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}\text{a= 0,1}\\b=0,1\end{matrix}\right.\)
\(\Rightarrow\text{mCa(HCO3)2=16,2(g)}\)

a)
$Fe_2O_3 + 3CO \xrightarrow{t^o} 2Fe +3 CO_2$
$Fe + 2HCl \to FeCl_2 + H_2$
$RO + H_2 \xrightarrow{t^o} R + H_2O$
b)
Coi m = 160(gam)$
Suy ra: $n_{Fe_2O_3} = 1(mol)$
Theo PTHH :
$n_{RO} = n_{H_2} = n_{Fe} = 2n_{Fe_2O_3} = 2(mol)$
$M_{RO} = R + 16 = \dfrac{160}{2} = 80 \Rightarrow R = 64(Cu)$
Vậy oxit là CuO

Phương trình hóa học :
3CO + Fe 2 O 3 → t ° 3 CO 2 + 2Fe (1)
3 H 2 + Fe 2 O 3 → t ° 3 H 2 O + 2Fe (2)

n Ba(OH)2 = 2.0,2=0,4 mol
\(Ba\left(OH\right)_2+SO_2->BaSO_3+H_2O\)
0,4 ................0,4...........0,4
m BaSO3 = 0,4. ( 138+32+16.3)=87,2 g
v SO2 = 0,4.22,4=8,96 lít
m BaSO3 = 0,4. ( 137+32+16.3)=86,8 g
xin lũi nha mình nhìn nhầm bạn thông cảm

\(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
0,1 0,2 0,1 0,1
\(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(a,\%m_{Zn}=\dfrac{0,1.65}{10}.100\%=65\%\)
\(\%m_{Cu}=100\%-65\%=35\%\)
\(b,V_{HCl}=\dfrac{0,2}{2}=0,1\left(l\right)\)

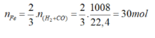
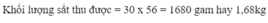

a) Phương trình hóa học :
\(3CO+Fe_2O_3\rightarrow^{t^o}3CO_2+2Fe\left(1\right)\)
\(3H_2+Fe_2O_3\rightarrow^{t^o}3H_2O+2Fe\left(2\right)\)
b) Tổng hợp (1) và (2) ta có :
Cứ 3 x 22,4 m3 hỗn hợp khí CO và H2 qua Fe203 thì thu được 2 x 56 kg Fe. 268,8 m3 hỗn hợp khí CO và H2 qua Fe203 thì thu được x kg Fe.
x=\(\frac{268,8.2.56}{3.22,4}=448kg\)
Fe2O3 + 3CO\(\rightarrow\) 2Fe + 3CO2
Fe2O3 + 3H2\(\rightarrow\) 2Fe + 3H2O
Nhân thấy CO và H2 đều khử Fe2O3 theo cùng tỉ lệ
Ta có: n hỗn hợp khí=\(\frac{268,8}{22,4}\)=12 kmol
Theo ptpu: nFe=\(\frac{2}{3}\) n hỗn hợp khí=\(\frac{2}{3}.\) 12=8 kmol
\(\rightarrow\) mFe=8.56=448 kg