Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

FeCl2 + 3AgNO3 → 2AgCl↓ + Ag↓ + Fe(NO3)3
0,04 ←0,12 → 0,08 0,04 0,04
Vậy: m(kết tủa) = mAgCl + mAg = 143,5 . 0,08 + 108 . 0,04 → m = 15,8(g)

nHCl = 0,1. 0,8 = 0,08 (mol) ; nAl2(SO4)3 = 0,1.0,5 = 0,05 (mol) => nAl3+ = 0,1 (mol); nSO42- = 0,15 (mol)
Gọi số mol Ba là x (mol)
Ba + 2HCl → BaCl2 + H2↑
Ba + 2H2O → Ba(OH)2 + H2↑
3BaCl2 + Al2(SO4)3 → 3BaSO4 ↓+ 2AlCl3
3Ba(OH)2 + Al2(SO4)3 → BaSO4↓ + 2Al(OH)3↓
Ba(OH)2 + 2Al(OH)3 → Ba(AlO2)2 + 4H2O
Vì dd X + HCl sinh ra 0,78 gam kết tủa Al(OH)3 : 0,1 (mol) nên trong dung dịch X chắc chắn có chứa Ba(AlO2)2 => lượng OH- sinh ra đã hòa tan 1 phần lượng kết tủa Al(OH)3
Ba + 2H+ → Ba2+ + H2↑
0,04 ← 0,08 (mol)
Ba + 2H2O → Ba2+ + 2OH- + H2↑
(x – 0,04 ) → (2x – 0,08) (mol)
Ba2+ + SO42- → BaSO4
3OH- + Al3+ → Al(OH)3↓
OH- + Al(OH)3 → AlO2- + 2H2O
Vì Al(OH)3 bị hòa tan 1 phần
=> nOH - > 3nAl3+
=> 2x – 0,08 > 3. 0,1
=> x > 0,19
=> nBa2+ > 0,19 (mol) => SO42- bị kết tủa hết => nBaSO4 = nSO42- = 0,15 (mol)
Mặt khác: nOH- = 4nAl3+ - nAl(OH)3 còn lại => nAl(OH)3 còn lại = 0,48 – 2x (mol)
=> nAl(OH)3 còn lại = 0,32 – 2x (mol)
mdd giảm = mBaSO4 + mAl(OH)3 còn lại + mH2 - mBa
=> 0,15.233 + (0,48 – 2x).78 + 2x - 137x = 14,19
=> 291x = 58,2
=> x = 0,2 (mol)
=> mBa = 0,2. 137 = 27,4 (g)
Vậy dung dịch X chứa:
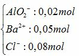 + V ml HCl 1M→ Al(OH)3: 0,01 (mol)
+ V ml HCl 1M→ Al(OH)3: 0,01 (mol)
TH1: AlO2- dư, H+ hết
AlO2- + H+ + H2O → Al(OH)3↓
=> nH+ = nAl(OH)3 = 0,01 (mol) => VHCl = n: CM = 0,01 (lít) = 10 (ml)
TH2: AlO2- , H+ đều phản ứng hết, kết tủa sinh ra bị hòa tan 1 phần
AlO2- + H+ + H2O → Al(OH)3↓
0,02 → 0,02 → 0,02 (mol)
H+ + Al(OH)3 → Al3+ + 2H2O
0,01← (0,02 – 0,01) (mol)
=> nH+ = 0,02 + 0,01 = 0,03 (mol) => VHCl = n : CM = 0,03 (lít) = 30 (ml)
nHCl = 0,1. 0,8 = 0,08 (mol) ; nAl2(SO4)3 = 0,1.0,5 = 0,05 (mol) => nAl3+ = 0,1 (mol); nSO42- = 0,15 (mol)
Gọi số mol Ba là x (mol)
Ba + 2HCl → BaCl2 + H2↑
Ba + 2H2O → Ba(OH)2 + H2↑
3BaCl2 + Al2(SO4)3 → 3BaSO4 ↓+ 2AlCl3
3Ba(OH)2 + Al2(SO4)3 → BaSO4↓ + 2Al(OH)3↓
Ba(OH)2 + 2Al(OH)3 → Ba(AlO2)2 + 4H2O
Vì dd X + HCl sinh ra 0,78 gam kết tủa Al(OH)3 : 0,1 (mol) nên trong dung dịch X chắc chắn có chứa Ba(AlO2)2 => lượng OH- sinh ra đã hòa tan 1 phần lượng kết tủa Al(OH)3
Ba + 2H+ → Ba2+ + H2↑
0,04 ← 0,08 (mol)
Ba + 2H2O → Ba2+ + 2OH- + H2↑
(x – 0,04 ) → (2x – 0,08) (mol)
Ba2+ + SO42- → BaSO4
3OH- + Al3+ → Al(OH)3↓
OH- + Al(OH)3 → AlO2- + 2H2O
Vì Al(OH)3 bị hòa tan 1 phần
=> nOH - > 3nAl3+
=> 2x – 0,08 > 3. 0,1
=> x > 0,19
=> nBa2+ > 0,19 (mol) => SO42- bị kết tủa hết => nBaSO4 = nSO42- = 0,15 (mol)
Mặt khác: nOH- = 4nAl3+ - nAl(OH)3 còn lại => nAl(OH)3 còn lại = 0,48 – 2x (mol)
=> nAl(OH)3 còn lại = 0,32 – 2x (mol)
mdd giảm = mBaSO4 + mAl(OH)3 còn lại + mH2 - mBa
=> 0,15.233 + (0,48 – 2x).78 + 2x - 137x = 14,19
=> 291x = 58,2
=> x = 0,2 (mol)
=> mBa = 0,2. 137 = 27,4 (g)
Vậy dung dịch X chứa:
+ V ml HCl 1M→ Al(OH)3: 0,01 (mol)
TH1: AlO2- dư, H+ hết
AlO2- + H+ + H2O → Al(OH)3↓
=> nH+ = nAl(OH)3 = 0,01 (mol) => VHCl = n: CM = 0,01 (lít) = 10 (ml)
TH2: AlO2- , H+ đều phản ứng hết, kết tủa sinh ra bị hòa tan 1 phần
AlO2- + H+ + H2O → Al(OH)3↓
0,02 → 0,02 → 0,02 (mol)
H+ + Al(OH)3 → Al3+ + 2H2O
0,01← (0,02 – 0,01) (mol)
=> nH+ = 0,02 + 0,01 = 0,03 (mol) => VHCl = n : CM = 0,03 (lít) = 30 (ml)

a)
$MCO_3 \xrightarrow{t^o} MO + CO_2$
$CO_2 + Ba(OH)_2 \to BaCO_3 + H_2O$
$CO_2 + Ba(OH)_2 \to Ba(HCO_3)_2$
b)
$n_{Ba(OH)_2} = 0,15(mol) ; n_{BaCO_3} = \dfrac{19,7}{197} = 0,1(mol)$
$n_{Ba(HCO_3)_2} = n_{Ba(OH)_2} - n_{BaCO_3} = 0,05(mol)$
$n_{CO_2} = n_{BaCO_3} + 2n_{Ba(HCO_3)_2} = 0,2(mol)$
$n_{MCO_3} = n_{CO_2} = 0,2(mol)$
$m_A = m_{MCO_3} - m_{CO_2} = 20 - 0,2.44 = 11,2(gam)$
c)
$M_{MCO_3} = M + 60 = \dfrac{20}{0,2} = 100$
$\Rightarrow M = 40(Canxi)$
Vậy CTHH : $CaCO_3$

nHCl = 0,4.0,5 = 0,2 mol; nH2SO4 = 0,08.0,5 = 0,04 mol
nH+ = nHCl + 2nH2SO4 = 0,28 mol
Đặt số mol của Zn và Mg trong hỗn hợp ban đầu là x và y (mol)
Ta có: 65x + 24y = 5,34 (1)
Zn + 2H+ → Zn2+ + H2
x → 2x → x (mol)
Mg + 2H+ → Mg2+ + H2
y → 2y → y (mol)
Dung dịch Y gồm có:
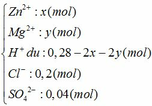
Ta thấy: nH+ + 2nZn2+ + 2nMg2+ (= 0,28 mol) < nNaOH (= 0,3 mol)
=> NaOH dư, Zn(OH)2 bị tan một phần
=> nNaOH hòa tan kết tủa = 0,3 – 0,28 = 0,02 mol
H+ + OH- → H2O
0,28-2x-2y → 0,28-2x-2y (mol)
Zn2+ + 2OH- → Zn(OH)2
x → 2x → x (mol)
Mg2+ + 2OH- → Mg(OH)2
y → 2y → y (mol)
Zn(OH)2 + 2OH- → ZnO22- + H2O
0,01 ← 0,02 (mol)
Khối lượng kết tủa thu được sau phản ứng: m kết tủa = mMg(OH)2 + mZn(OH)2
=> 99(x-0,01) + 58y = 8,43 <=> 99x + 58y = 9,42 (2)
Từ (1) và (2) ta có:

Ta có: nKOH : nBa(OH)2 = 0,4:0,05 = 8
Giả sử số mol của KOH và Ba(OH)2 lần lượt là 8a và a (mol)
=> nBa2+ = a (mol); nOH- = nKOH + 2nBa(OH)2 = 10a (mol)
- Khi kết tủa Mg(OH)2 và Zn(OH)2 đạt giá trị lớn nhất: nOH- = nH+ dư + 2nZn2+ + 2nMg2+
=> 10a = 0,04 + 2.0,06 + 2.0,06 => a = 0,028 mol
Ta thấy a < nSO42- => BaSO4 chưa đạt cực đại
- Giả sử sau khi Mg(OH)2 và Zn(OH)2 đạt cực đại ta thêm 8b mol KOH và b mol Ba(OH)2:
+ Lượng kết tủa sinh thêm là lượng BaSO4: nBaSO4 = nBa(OH)2 = b mol
=> mBaSO4 = 233b (gam)
+ Lượng kết tủa bị tan ra: nZn(OH)2 = nOH-: 2 = 10b : 2 = 5b (mol)
=> mZn(OH)2 = 99.5b = 495b (gam)
Ta thấy khối lượng kết tủa sinh ra nhỏ hơn khối lượng kết tủa bị tan nên khối lượng kết tủa lớn nhất là thời điểm Mg(OH)2 và Zn(OH)2 đạt cực đại. Khi đó: nBa(OH)2 = a = 0,028 mol
=> V = 0,028 : 0,05 = 0,56 (lít)
Kết tủa sau phản ứng gồm có:
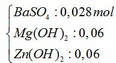
Mg(OH)2 → t ∘ MgO + H2O
0,06 mol → 0,06 mol
Zn(OH)2 → t ∘ ZnO + H2O
0,06 mol → 0,06 mol
=> m = mBaSO4 + mMgO + mZnO = 0,028.233 + 0,06.40 + 0,06.81 = 13,784 gam

a. Các phản ứng có thể xảy ra :
P2O5 + 3H2O -> 2H3PO4
KOH + H3PO4 -> KH2PO4 + H2O
2KOH + H3PO4 -> K2HPO4 + 2H2O
3KOH + H3PO4 -> K3PO4 + 3H2O
b.Gọi nP2O5 = x mol
=> nH3PO4(X) = 0,01+ 2x (mol)
, nKOH = 0,1 mol
+) TH1 : Nếu KOH dư => chất rắn gồm : (0,01 + 2x) mol K3PO4 ; (0,07 – 6x) mol KOH
=> 6,48 = 212(0,01 + 2x) + 56(0,07 – 6x) => x = 0,005 mol => m = 0,71g
=> 6,48g X gồm : 4,24g K3PO4 và 2,24g KOH
+) TH2 : Nếu chất rắn gồm : (0,08 – 2x) mol K3PO4 ; (4x – 0,07) mol K2HPO4
, mK3PO4 < 6,48g => 0,08 – 2x < 0,03 => x > 0,025
=> 6,48 = 212(0,08 - 2x) + 174(4x – 0,07) => x = 0,00625 mol (L)
+) TH3 : Nếu chất rắn gồm : (0,09 - 2x) mol K2HPO4 ; (4x – 0,08) mol KH2PO4
,mK2HPO4 < 6,48g => 0,09 – 2x < 0,037 => x > 0,043
=> 6,48 = 174(0,09 - 2x) + 136(4x – 0,08) => x = 0,0086 mol (L)
+) TH4 : Nếu H3PO4 dư => nKH2PO4 = 0,1 mol => mKH2PO4 = 13,6g > 6,48g (L)

Nhận xét: nAl(OH)3 = 0,05 < nAlCl3 → kết tủa chưa đạt tối đa.
TH1: kết tủa chưa bị hòa tan
Ba(OH)2 + 2HCl → BaCl2 + 2H2O
0,025 ← 0,05
3Ba(OH)2 + 2AlCl3 → 3BaCl2 + 2Al(OH)3↓
0,075 ← 0,05
→ nBa(OH)2 = 0,1 → V = 100 ml
TH2: kết tủa bị hòa tan một phần
Ba(OH)2 + 2HCl → BaCl2 + 2H2O
0,025 ← 0,05
3Ba(OH)2 + 2AlCl3 → 3BaCl2 + 2Al(OH)3↓
0,15 ← 0,1 → 0,1
Ba(OH)2 + 2Al(OH)3 → Ba(AlO2)2 + 4H2O
0,025 ← 0,05
Dư: 0,05
→ nBa(OH)2 = 0,2 → V = 200 ml
Vậy có 2 giá trị của V là: 100 và 200

Câu 1 mik ko bít:)
Câu 2
-Lấy mẫu thử và đánh dấu
-Dẫn các mẫu thử vài nước vôi trong
+Mẫu thử xuất hiện kết tủa trắng ban đầu là \(CO_2\)
\(CO_2+Ca\left(OH\right)_2\Rightarrow CaCO_3+H_2O\)
+Mẫu thử không hiện tượng chất ban đầu là \(CH_4,C_2H_4,C_2H_2\left(I\right)\)
-Dẫn nhóm \(\left(I\right)\)vào dung dịch \(brom\)
+Mẫu thử làm mất màu dung dịch \(brom\) chất ban đầu là:\(C_2H_4,C_2H_2\left(II\right)\)
\(C_2H_4+Br_2\Rightarrow C_2H_4Br_2\\ C_2H_2+2Br_2\Rightarrow C_2H_2Br_4\)
+Mẫu thử không hiện tượng chất ban đầu là \(CH_4\)
-Cho \(AgO_2\)vào nhóm \(\left(II\right)\)
+Mẫu thử xuất hiện kết tủa vàng chất ban đầu là \(C_2H_2\)
\(C_2H_2+Ag_2O\)--\(NH_3\)-->\(C_2Ag_2+H_2O\)
+Mẫu thử không hiện tượng chất ban đầu là \(C_2H_4\)
áp dụng công thức nghe nè
1. Tác dụng với kim loại
- Dung dịch muối có thể tác dụng với kim loại tạo thành muối mới và kim loại mới.
2. Tác dụng với axit
- Muối có thể tác dụng được với axit tạo thành muối mới và axit mới.
* Điều kiện xảy ra phản ứng: sản phẩm tạo thành phải có chất khí hoặc chất kết tủa hoặc nước
Ví dụ: BaCl2 + H2SO4 → 2HCl + BaSO4↓
CaCO3 + 2HCl → CaCl2 + CO2↑ + H2O
NaCl không phản ứng với dung dịch H2SO4 vì không sinh ra chất khí, chất kết tủa hay nước.
3. Tác dụng với dung dịch muối
- Hai dung dịch muối có thể tác dụng với nhau tạo thành hai muối mới.
* Điều kiện xảy ra phản ứng: sản phẩm tạo thành phải có chất khí hoặc chất kết tủa hoặc nước
Ví dụ: AgNO3 + NaCl → NaNO3 + AgCl↓
Fe(NO3)2 không phản ứng với dung dịch NaCl vì không sinh ra chất khí, chất kết tủa hay nước.
4. Tác dụng với dung dịch bazơ
- Dung dịch bazơ có thể tác dụng với dung dịch bazơ tạo thành muối mới và bazơ mới.
* Điều kiện xảy ra phản ứng: sản phẩm tạo thành phải có chất khí hoặc chất kết tủa hoặc nước
Ví dụ: Na2CO3 + Ba(OH)2 → 2NaOH + BaCO3↓
5. Phản ứng phân hủy muối
- Một số muối bị phân hủy ở nhiệt độ cao như: KClO3, KMnO4, CaCO3,…
Ví dụ: 2KClO3 to→→to 2KCl + 3O2
CaCO3 to→→to CaO + CO2
II. PHẢN ỨNG TRAO ĐỔI TRONG DUNG DỊCH
1. Định nghĩa: Phản ứng trao đổi là phản ứng hóa học, trong đó hai hợp chất tham gia phản ứng trao đổi với nhau những thành phần cấu tạo của chúng để tạo ra những hợp chất mới không tan hoặc chất khí.
2. Điều kiện xảy ra phản ứng trao đổi
Phản ứng trao đổi trong dung dịch của các chất chỉ xảy ra nếu sản phẩm tạo thành có chất không tan hoặc chất khí hoặc nước.
Ví dụ: CuSO4 + 2NaOH → Na2SO4 + Cu(OH)2↓
K2SO4 + NaOH: Phản ứng không xảy ra.
Chú ý: phản ứng trung hòa cũng thuộc loại phản ứng trao đổi và luôn xảy ra.
Ví dụ: H2SO4 + 2NaOH → Na2SO4 + 2H2O

Ba(OH)2 + Mg(HCO3)2 → BaCO3↓ + MgCO3↓ + 2H2O
0,1 ← 0,1
Dư: 0,075