Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Theo đề bài ta có : \(\left\{{}\begin{matrix}nFe2O3=\dfrac{1,6}{160}=0,01\left(mol\right)\\mHCl=\dfrac{100.1}{1000}=0,1\left(mol\right)\end{matrix}\right.\)
Ta có PTHH :
Fe2O3 + 6HCl \(\rightarrow\) 2FeCl3 + 3H2O
0,01mol...0,06mol
Theo PTHH ta có : \(nFe2O3=\dfrac{0,01}{1}mol< nHCl=\dfrac{0,1}{6}mol\)
=> Số mol của HCl dư ( tính theo số mol của Fe2O3)
Vì giả sử thể tích dung dịch sau phản ứng không đổi nên ta có :
CM\(_{HCl\left(d\text{ư}\right)}=\dfrac{\left(0,1-0,06\right)}{0,1}=0,4\left(M\right)\)
Vậy..............

Theo đề ta có : \(\left\{{}\begin{matrix}nFe2O3=\dfrac{1,6}{160}=0,01\left(mol\right)\\nHCl=0,1.1=0,1\left(mol\right)\end{matrix}\right.\)
Ta có PTHH :
\(Fe2O3+6HCl->2FeCl3+3H2O\)
0,01mol.........0,06mol
Theo PTHH ta có : \(nFe2O3=\dfrac{0,01}{1}mol< nHCl=\dfrac{0,1}{6}mol=>nHCl\left(d\text{ư}\right)\)
=> \(CM_{\text{dd}HCl\left(d\text{ư}\right)}=\dfrac{0,1-0,06}{0,1}=0,4\left(M\right)\)
Vậy...

a)
$n_{MgO} = \dfrac{8}{40} = 0,2(mol)$
$MgO + 2HCl \to MgCl_2 + H_2O$
$n_{HCl} = 2n_{MgO} = 0,4(mol) \Rightarrow V_{dd\ HCl} = \dfrac{0,4}{1} = 0,4(lít)$
b)
$n_{MgCl_2} = n_{MgO} = 0,2(mol) \Rightarrow C_{M_{MgCl_2}} = \dfrac{0,2}{0,4} = 0,5M$
c)
$MgCl_2 + 2NaOH \to Mg(OH)_2 + 2NaCl$
$n_{NaOH} = 2n_{MgCl_2} = 0,4(mol)$
$n_{Mg(OH)_2} = n_{MgCl_2} = 0,2(mol)$
Suy ra :
$V = \dfrac{0,4}{1} = 0,4(lít)$
$m_{Mg(OH)_2} = 0,2.58 = 11,6(gam)$
\(n_{MgO}=\dfrac{8}{40}=0,2mol\)
\(MgO+2HCl\rightarrow MgCl_2+H_2O\)
0,2 0,4 0,2 0,2
a)\(V_{HCl}=\dfrac{0,4}{1}=0,4\left(l\right)=400ml\)
c) \(MgCl_2+2NaOH\rightarrow Mg\left(OH\right)_2+2NaCl\)
0,2 0,2
\(\Rightarrow V_{NaOH}=\dfrac{0,2}{1}=0,2\left(l\right)=200ml\)

PTHH: \(CaCl_2+Na_2CO_3\rightarrow CaCO_3\downarrow+2NaCl\)
a+b) Ta có: \(n_{CaCl_2}=0,1\cdot2=0,2\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{CaCO_3}=0,2\left(mol\right)\\n_{NaCl}=0,4\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{CaCO_3}=0,2\cdot100=20\left(g\right)\\C_{M_{NaCl}}=\dfrac{0,4}{0,1+0,2}\approx1,33\left(M\right)\end{matrix}\right.\)
c) PTHH: \(CaCO_3+2HCl\rightarrow CaCl_2+H_2O+CO_2\)
Theo PTHH: \(n_{HCl}=2n_{CaCO_3}=0,4\left(mol\right)\) \(\Rightarrow m_{ddHCl}=\dfrac{0,4\cdot36,5}{10\%}=146\left(g\right)\)
a.PTHH:CaCl2+Na2CO3--->CaCO3+2NaCl
Ta có:nCaCl2=0,2
=>nCaCO3=nCaCl2=0,2(mol)=>mCaCO3(kết tủa)=100.0,2=2(g)
b.Vdd=100+200=300(ml)=0,3(l)
CM Nacl=(2.0,2)/0,3=4/3(M)(Đề cho 2 chất td vừa đủ nên dd sau pứ chỉ có NaCl)
c.CaCO3+2HCl--->CaCl2+CO2+H2O
nHCl(cần dùng)=2.0.2=0,4(mol)=>mHCl=36,5.0,4=14,6(g)
=>mddHCl=14,6/10%=146(g)

\(300(ml)=0,3(l)\\ n_{HCl}=1.0,3=0,3(mol);n_{Fe}=\dfrac{5,6}{56}=0,1(mol)\\ a,PTHH:Fe+2HCl\to FeCl_2+H_2\\ \text{LTL: }\dfrac{n_{Fe}}{1}<\dfrac{n_{HCl}}{2}\Rightarrow HCl\text{ dư}\\ \Rightarrow n_{HCl(dư)}=0,3-0,1.2=0,1(mol)\\ \Rightarrow m_{HCl(dư)}=0,1.36,5=3,65(g)\\ b,n_{FeCl_2}=n_{Fe}=0,1(mol)\\ \Rightarrow \begin{cases} C_{M_{FeCl_2}}=\dfrac{0,1}{0,3}=0,33M\\ C_{M_{HCl(dư)}}=\dfrac{0,1}{0,3}=0,33M \end{cases}\)

$n_{CaO} = \dfrac{11,2}{56} = 0,2(mol)$
$n_{HCl} = 0,5.1 = 0,5(mol)$
$CaO + dư2HCl \to CaCl_2 + H_2O$
Ta thấy :
$n_{CaO} : 1 < n_{HCl} : 2$ nên $HCl$ dư
$n_{HCl\ pư} = 2n_{CaO} = 0,4(mol)$
$m_{HCl\ dư} = (0,5 - 0,4).36,5 = 3,65(gam)$
$n_{CaCl_2} = n_{CaO} = 0,2(mol)$
$C_{M_{HCl\ dư}} = \dfrac{0,1}{0,5} = 0,2M$
$C_{M_{CaCl_2}} = \dfrac{0,2}{0,5} = 0,4M$
\(n_{CaO}=\dfrac{11,2}{56}=0,2\left(mol\right)\\ n_{HCl}=0,5.1=0,5\left(mol\right)\\ CaO+2HCl\xrightarrow[]{}CaCl_2+H_2O\\ \Rightarrow\dfrac{0,2}{1}< \dfrac{0,5}{2}\Rightarrow HCl.dư\\ n_{HCl\left(pư\right)}=0,2.2=0,4\left(mol\right)\\ n_{HCl\left(dư\right)}=0,5-0,4=0,1\left(mol\right)\\ m_{HCl\left(dư\right)}=0,1.36,5=3,65\left(g\right)\\ n_{CaCl_2}=n_{CaO}=0,2mol\\ C_{M_{CaCl_2}}=\dfrac{0,2}{0,5}=0,4\left(M\right)\\ C_{M_{HCl}}=\dfrac{0,1}{0,5}=0,2\left(M\right)\)

\(a.n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\\ n_{HCl}=0,2.1,5=0,3\left(mol\right)\\ Mg+2HCl\rightarrow MgCl_2+H_2\\ Vì:\dfrac{0,3}{2}< \dfrac{0,2}{1}\\ \Rightarrow Mgdư\\ n_{H_2}=n_{MgCl_2}=\dfrac{0,3}{2}=0,15\left(mol\right)\\ V_{H_2\left(đktc\right)}=0,15.22,4=3,36\left(l\right)\\ b.V_{ddsau}=V_{ddHCl}=0,2\left(l\right)\\ C_{MddMgCl_2}=\dfrac{0,15}{0,2}=0,75\left(M\right)\)

a) Phương trình hóa học của phản ứng:
b) Theo pt (1): nCl2 = nMnCl2 = nMnO2 = 0,8 mol
Theo pt (2): nNaCl = nNaClO = nCl2 = 0,8 mol
nNaOH pư = 2. nCl2 = 2. 0,8 = 1,6 mol
⇒ nNaOH dư = 2 - 1,6 = 0,4 mol
Nồng độ mol/l của các chất trong dung dịch sau phản ứng:
CM (NaCl) = CM (NaClO) = CM(MnCl2) = 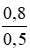
CM (NaOH)dư = 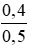
tích cho mình nha![]()
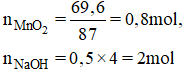
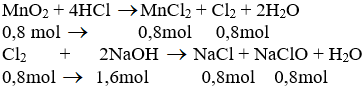
PTHH: Fe2O3 + 6HCl --> 2FeCl3 + 3H2O
-nFe2O3=0,01;nHCl=0,1
-Theo pt: nHCl=6nFe2O3=6*0,01=0,06(mol)
=>nHCl dư=0,1-0,06=0,04
CM HCl=0,04/0,1=0,4M