Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{C_6H_5Cl}=\dfrac{78}{112,5}=\dfrac{52}{75}\left(mol\right)\)
\(n_{C_6H_6}=\dfrac{78}{78}=1\left(mol\right)\)
PTHH:
\(C_6H_6+Cl_2\xrightarrow[t^o]{Fe}C_6H_5Cl\)
1------------------>1
\(\Rightarrow H=\dfrac{\dfrac{52}{75}}{1}.100\%=69,33\%\)

nC6H5Br=\(\frac{3,925}{6.12+5+80}\)=0,025(mol)
PTHH: C6H6+Br2 \(\xrightarrow[t^o]{Fe}\) C6H5Br + HCl
(mol) 0,025 0,025 0,025
mC6H6=\(\frac{0,025.\left(12x6+6\right)}{75\%}\)=2,6 (g)
mBr2=\(\frac{0,025.160}{75\%}\)=5,3(g)

nC6H6 = 0,3 mol
C6H6 + Br2 → C6H5Br + HBr
0,3........................0,3
⇒ mC6H5Br = 0,3.157.\(\dfrac{90}{100}\) = 42,39 (g)

Phương trình hoá học của phản ứng giữa benzen và clo
C 6 H 6 + Cl 2 → t ° C 6 H 5 Cl + HCl
Theo phương trình hoá học : số mol C 6 H 6 = số mol C 6 H 5 Cl
Vì hiệu suất 80% và clo dư nên số mol clobenzen thu được là :
n C 6 H 5 Cl = 15,6/78 x 80/100 = 0,16mol
=> m C 6 H 5 Cl = 0,16 x 112,5 = 18g

nclobenzen=0.6933 mol
=> H = 69.33% ( bài này đối với Cl tác dụng với 87g benzen nha)

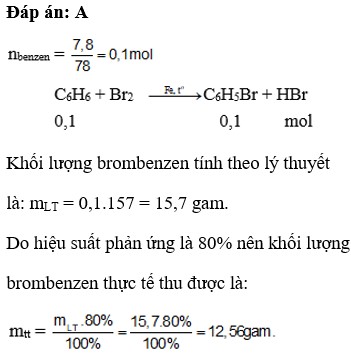

C6H6 + Br2 --(Fe, nhiệt)--> C6H5Br + HBr
nC6H6 = \(\frac{15,6}{78}\) = 0,2 mol
nC6H5Br (lý thuyết) = 0,2 (mol)
mC6H5Br (lý thuyết) = 0,2.157 = 31,4 (g)
H = \(\frac{14,8.100}{31,4}\)=47,13 %