Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Nồng độ NaOH nhỏ nhất là lượng NaOH đủ để kết tủa với 0,01 mol Al3+
⇒ n N a O H = 0 , 01 . 3 = 0 , 03 ⇒ [ N a O H ] = 0 , 03 0 , 2 = 0 , 15

Đáp án B
6NH3+ Al2(SO4)3+ 6H2O→ 2Al(OH)3+3 (NH4)2SO4 (1)
NaOH + Al(OH)3 → NaAlO2+ H2O (2)
Có nAl(OH)3= nNaOH= 0,01.2= 0,02 mol
→ nAl2(SO4)3= 1 2 . nAl(OH)3= 0,01 mol
→ CM Al2(SO4)3= 0,01/ 0,02= 0,5M

a)nHCl= 0,1 , nNaOh=0,4 khi phân li ra ta thu được các ion; H+, Cl- Na+, OH- Vdung dịch sau = 0,1+0,4=0,5(l)
nH+=nCl-=0,1 [H+]=[Cl-]=0,1/0,5=0,2 (M)
nNa+=nOH-=0,4 [Na+]=[OH-]=0,4/0,5=0,8
b)nH+=0,1 nOH-=0,4 --> OH- dư --> nOHdư=0,4-0,1=0,3 --> [OHdư ]=0,3/0,5=0,6 --> pOh=0,23--> ph=14-0,23=13,77

Câu 1:
Ta có: \(n_{H_3PO_4}=0,15.1=0,15\left(mol\right)\)
\(n_{NaOH}=0,225.1=0,225\left(mol\right)\)
\(\Rightarrow\dfrac{n_{NaOH}}{n_{H_3PO_4}}=\dfrac{0,225}{0,15}=1,5\)
⇒ Pư tạo muối NaH2PO4 và Na2HPO4.
a, Giả sử: \(\left\{{}\begin{matrix}n_{NaH_2PO_4}=x\left(mol\right)\\n_{Na_2HPO_4}=y\left(mol\right)\end{matrix}\right.\)
BTNT Na, có: x + 2y = 0,225 (1)
BTNT P, có: x + y = 0,15 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,075\left(mol\right)\\y=0,075\left(mol\right)\end{matrix}\right.\)
⇒ mNaH2PO4 = 0,075.120 = 9 (g)
mNa2HPO4 = 0,075.142 = 10,65 (g)
b, \(C_{M_{NaH_2PO_4}}=C_{M_{Na_2HPO_4}}=\dfrac{0,075}{0,375}=0,2M\)
Câu 2:
Ta có: \(n_{H_3PO_4}=0,15\left(mol\right)\)
\(n_{KOH}=0,35\left(mol\right)\)
\(\Rightarrow\dfrac{n_{KOH}}{n_{H_3PO_4}}=2,333\)
Vậy: Pư tạo muối Na2HPO4 và Na3PO4.
a, Giả sử: \(\left\{{}\begin{matrix}n_{Na_2HPO_4}=x\left(mol\right)\\n_{Na_3PO_4}=y\left(mol\right)\end{matrix}\right.\)
BTNT Na, có: 2x + 3y = 0,35 (1)
BTNT P, có: x + y = 0,15 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,1\left(mol\right)\\y=0,05\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_{Na_2HPO_4}=0,1.142=14,2\left(g\right)\)
\(m_{Na_3PO_4}=0,05.164=8,2\left(g\right)\)
b, Ta có: \(\left\{{}\begin{matrix}C_{M_{Na_2HPO_4}}=\dfrac{0,1}{0,5}=0,2M\\C_{M_{Na_3PO_4}}=\dfrac{0,05}{0,5}=0,1M\end{matrix}\right.\)
Bạn tham khảo nhé!

\(n_{NaOH}=0,25.4=1\left(mol\right)\\ n_{Al_2\left(SO_4\right)_3}=2.0,05=0,1\left(mol\right)\\ PTHH:6NaOH+Al_2\left(SO_4\right)_3\rightarrow2Al\left(OH\right)_3+3Na_2SO_4\\ Vì:\dfrac{1}{6}>\dfrac{0,1}{1}\\ \Rightarrow NaOHdư\\ \rightarrow n_{Al\left(OH\right)_3}=2.0,1=0,2\left(mol\right)\\ m_{kt}=m_{Al\left(OH\right)_3}=78.0,2=15,6\left(g\right)\)
\(n_{NaOH}=0.25\cdot4=1\left(mol\right)\)
\(n_{Al_2\left(SO_4\right)_3}=0.05\cdot2=0.1\left(mol\right)\)
\(Al_2\left(SO_4\right)_3+6NaOH\rightarrow2Al\left(OH\right)_3+3Na_2SO_4\)
Lập tỉ lệ :
\(\dfrac{0.1}{1}< \dfrac{1}{6}\) \(\Rightarrow NaOHdư\)
\(n_{NaOH\left(dư\right)}=1-0.6=0.4\left(mol\right)\)
\(n_{Al\left(OH\right)_3}=0.1\cdot2=0.2\left(mol\right)\)
\(NaOH+Al\left(OH\right)_3\rightarrow NaAlO_2+2H_2O\)
\(n_{NaOH}>n_{Al\left(OH\right)_3}\)
=> Kết tủa tan hoàn toàn
\(m_{\downarrow}=0\)
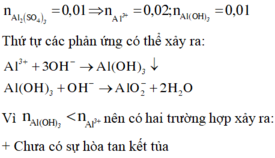

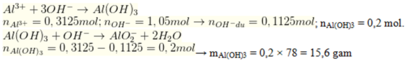
Đáp án A
Sau phản ứng Vdung dịch = 150 + 100 = 250 ml = 0,25 lít