Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
6NH3+ Al2(SO4)3+ 6H2O→ 2Al(OH)3+3 (NH4)2SO4 (1)
NaOH + Al(OH)3 → NaAlO2+ H2O (2)
Có nAl(OH)3= nNaOH= 0,01.2= 0,02 mol
→ nAl2(SO4)3= 1 2 . nAl(OH)3= 0,01 mol
→ CM Al2(SO4)3= 0,01/ 0,02= 0,5M

Đáp án D
• 0,1V mol NaOH + 0,01 mol Al2(SO4)3 → ↓ Al(OH)3
Nung ↓ → 0,005 mol Al2O3
→ nAl(OH)3 = 0,01 mol.
• V lớn nhất khi NaOH dư
6NaOH + Al2(SO4)3 → 2Al(OH)3↓ + 3Na2SO4 (*)
NaOH + Al(OH)3 → NaAlO2 + 2H2O (**)
Theo (*) nNaOH = 0,01 × 6 = 0,06 mol; nAl(OH)3 = 0,01 × 2 = 0,02 mol.
Theo (**) nAl(OH)3 phản ứng = 0,02 - 0,01 = 0,01 mol
→ nNaOH = 0,01 mol
→ ∑nNaOH = 0,06 + 0,01 = 0,07 mol
→ VNaOH = 0,07 : 0,1 = 0,7 lít = 700 ml

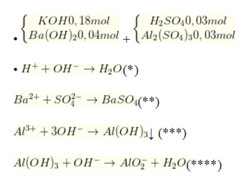
n O H - = n H + = 0 , 06 m o l T h e o ( * * ) n B a S O 4 = n B a 2 + = 0 , 04 m o l T h e o ( * * * ) n O H - = 3 x 0 , 03 x 2 = 0 , 18 m o l ; n A l ( O H ) 3 = 0 , 03 x 2 = 0 , 06 m o l T h e o ( * * * * ) n O H - = 0 , 18 + 0 , 04 x 2 - 0 , 06 - 0 , 18 = 0 , 02 m o l n A l ( O H ) 3 d ư = 0 , 06 - 0 , 02 = 0 , 04 m o l .
→ m↓ = mAl(OH)3 + mBaSO4 = 0,04 × 78 + 0,04 × 233 = 12,44 gam
→ Đáp án đúng là đáp án D

Đáp án C
Trong 100ml dd X có 0,1 mol Ba2+, 0,15 mol .
Trong 200ml dung dịch X có 0,2 mol Cl-.
Do đó trong 50 ml dung dịch X có 0,05 mol Ba2+, 0,075 mol , 0,05 mol Cl- và x mol K+
Theo định luật bảo toàn điện tích được x = 0,025
Khi cô cạn xảy ra quá trình:


Đáp án C
+ Lấy 100 ml dung dịch X phản ứng với dung dịch NaOH dư, kết thúc các phản ứng thu được 19,7 gam kết tủa⇒ n BaCO3 = n Ba2+ 0,1 mol . Lấy 100 ml dung dịch X tác dụng với dung dịch Ba(OH)2 dư, sau khi các phản ứng kết thúc thu được 29,55 gam kết tủa
⇒ n BaCO3- = n HCO3- = 0,15 mol
⇒ Trong 100ml ddX có 0,1 mol Ba2+ , 0,15 mol HCO3- .
+ Cho 200 ml dung dịch X phản ứng với lượng dư dung dịch AgNO3, kết thúc phản ứng thu được 28,7 gam kết tủa ⇒ Trong 200ml ddX có nCl- = n AgCl = 0,2 mol
⇒ Trong 50ml ddX có 0,05 mol Ba2+ ; 0,075 mol HCO3- , 0,05 mol Cl- ⇒ nK+ = 0,025
2HCO3- → CO32- + CO2 + H2O
0,075 → 0,0375 0,0375(mol)
Khi đun sôi đến cạn: mkhan = m HCO3- + m Ba2+ + m K+ + m Cl- - m CO2 – m H2O
= 0,05.137 + 0,075.61 + 0,05.35,5 + 0,025.39 – 0,0375.44 - 0,0375.18 = 11,85g

Đáp án D
• 0,42 mol NaOH + 0,02 mol Fe2(SO4)3; 0,04 mol Al2(SO4)3 → 500ml X + ↓
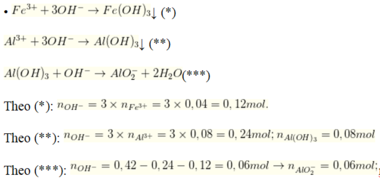
nAl(OH)3 = 0,08 - 0,06 = 0,02 mol
Vậy sau phản ứng 500ml dung dịch X gồm 0,06 mol Na[Al(OH)4]; 0,18 mol Na2SO4
→ CM các chất trong X là CMNa2SO4 = 0,06 : 0,5 = 0,12 M;
CMNa[Al(OH)4] = 0,18 : 0,5 = 0,36 M

Nhận thấy 36,9 gam kết tủa gồm BaSO4 : 0,15 mol và Al(OH)3 : 0,025 mol
Vì nAl(OH)3 = 0,025 mol < <nOH- = 0,3 + 0,3x mol → xảy ra hiện tượng hòa tan kết tủa
Al3+ + 3OH- → Al(OH)3
Al3+ + 4OH- → Al(OH)4-
Luôn có 4nAl3+ = nOH- + nAl(OH)3 → nOH- = 0,3 + 0,3x = 4×0,1 -0,025= 0,375 mol → x= 0,25 mol
→ Đáp án B

\(n_{NaOH}=0,25.4=1\left(mol\right)\\ n_{Al_2\left(SO_4\right)_3}=2.0,05=0,1\left(mol\right)\\ PTHH:6NaOH+Al_2\left(SO_4\right)_3\rightarrow2Al\left(OH\right)_3+3Na_2SO_4\\ Vì:\dfrac{1}{6}>\dfrac{0,1}{1}\\ \Rightarrow NaOHdư\\ \rightarrow n_{Al\left(OH\right)_3}=2.0,1=0,2\left(mol\right)\\ m_{kt}=m_{Al\left(OH\right)_3}=78.0,2=15,6\left(g\right)\)
\(n_{NaOH}=0.25\cdot4=1\left(mol\right)\)
\(n_{Al_2\left(SO_4\right)_3}=0.05\cdot2=0.1\left(mol\right)\)
\(Al_2\left(SO_4\right)_3+6NaOH\rightarrow2Al\left(OH\right)_3+3Na_2SO_4\)
Lập tỉ lệ :
\(\dfrac{0.1}{1}< \dfrac{1}{6}\) \(\Rightarrow NaOHdư\)
\(n_{NaOH\left(dư\right)}=1-0.6=0.4\left(mol\right)\)
\(n_{Al\left(OH\right)_3}=0.1\cdot2=0.2\left(mol\right)\)
\(NaOH+Al\left(OH\right)_3\rightarrow NaAlO_2+2H_2O\)
\(n_{NaOH}>n_{Al\left(OH\right)_3}\)
=> Kết tủa tan hoàn toàn
\(m_{\downarrow}=0\)