Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Câu 3.
a, \(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
PTHH: Zn + H2SO4 → ZnSO4 + H2
Mol: 0,1 0,1 0,1 0,1
b,\(V_{H_2}=0,1.22,4=2,24\left(l\right)\)
c,\(m_{ZnSO_4}=0,1.161=16,1\left(g\right)\)
\(m_{ddsaupư}=6,5+\dfrac{0,1.98.100}{25}-0,1.2=45,5\left(g\right)\)
\(\Rightarrow C\%_{ddZnSO_4}=\dfrac{16,1.100\%}{45,5}=35,4\%\)

\(n_{H2}=\dfrac{22,4}{22,4}=1\left(mol\right)\)
a) Pt : \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2|\)
2 3 1 3
a 0,6 1,5a
\(Mg+H_2SO_4\rightarrow MgSO_4+H_2|\)
1 1 1 1
b 0,4 1b
b) Gọi a là số mol của Al
b là số mol của Mg
\(m_{Al}+m_{Mg}=20,4\left(g\right)\)
⇒ \(n_{Al}.M_{Al}+n_{Mg}.M_{Mg}=20,4g\)
⇒ 27a + 24b = 20,4g (1)
The phương trình : 1,5a + 1b = 1(2)
Từ(1),(2), ta có hệ phương trình :
27a + 24b = 20,4g
1,5a + 1b = 1
⇒ \(\left\{{}\begin{matrix}a=0,4\\b=0,4\end{matrix}\right.\)
\(m_{Al}=0,4.27=10,8\left(g\right)\)
\(m_{Mg}=0,4.24=9,6\left(g\right)\)
c) \(n_{H2SO4\left(tổng\right)}=0,6+0,4=1\left(mol\right)\)
\(V_{ddH2SO4}=\dfrac{1}{0,2}=5\left(l\right)\)
Chúc bạn học tốt

a) Đặt số mol của MO, M(OH)2, MCO3 tương ứng là x, y, z.
Nếu tạo muối trung hòa ta có các phản ứng:
MO + H2SO4 →MSO4 + H2O (1)
M(OH)2 + H2SO4 →MSO4 + 2H2O (2)
MCO3 + H2SO4 →MSO4 + H2O + CO2 (3)
Nếu tạo muối axít ta có các phản ứng:
MO + 2H2SO4 →M(HSO4)2 + H2O (4)
M(OH)2 + 2H2SO4 →M(HSO4)2 + 2H2O (5)
MCO3 + 2H2SO4 →M(HSO4)2 + H2O + CO2 (6)
Ta có :
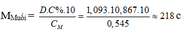
– TH1: Nếu muối là MSO4 M + 96 = 218 M = 122 (loại)
– TH2: Nếu là muối M(HSO4)2 M + 97.2 = 218 M = 24 (Mg)
Vậy xảy ra phản ứng (4, 5, 6) tạo muối Mg(HSO4)2
b) Theo (4, 5, 6) Số mol CO2 = 0,448/22,4 = 0,02 molz = 0,02 (I)
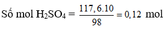
2x + 2y + 2z = 0,12 (II)
Đề bài: 40x + 58y + 84z = 3,64 (III)
Giải hệ (I, II, III): x = 0,02; y = 0,02; z = 0,02
%MgO = 40.0,02.100/3,64 = 21,98%
%Mg(OH)2 = 58.0,02.100/3,64 = 31,87%
%MgCO3 = 84.0,02.100/3,64 = 46,15%

\(a.n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\\ Đặt:\left\{{}\begin{matrix}n_{Al}=a\left(mol\right)\\n_{Mg}=b\left(mol\right)\end{matrix}\right.\left(a,b>0\right)\\ 2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\\ Mg+H_2SO_4\rightarrow MgSO_4+H_2\\ \rightarrow\left\{{}\begin{matrix}27a+24b=5,1\\1,5a+b=0,25\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,1\\b=0,1\end{matrix}\right.\\ \left\{{}\begin{matrix}\%m_{Al}=\dfrac{27.0,1}{5,1}.100\approx52,941\%\\\%m_{Mg}\approx47,059\%\end{matrix}\right.\)
\(b.m_{ddH_2SO_4}=\dfrac{0,25.98.100}{9,8}=250\left(g\right)\\ m_{ddsau}=m_{Al,Mg}+m_{ddH_2SO_4}-m_{H_2}=5,1+250-0,25.2=254,6\left(g\right)\\ C\%_{ddAl_2\left(SO_4\right)_3}=\dfrac{0,05.342}{254,6}.100\approx6,716\%\\ C\%_{ddMgSO_4}=\dfrac{0,1.120}{254,6}.100\approx4,713\%\)

a)
2Al + 3H2SO4 → Al2(SO4)3 +3H2
Mg + H2SO4 → MgSO4 + H2
b. n H2 = 8,96/22,4 =0,4 mol
Gọi x và y là số mol của Al và Mg ta có hệ
27x+ 24y = 7,8 (1)
1,5x+ y = 0,4 (2)
Từ 1 và 2 => x = 0,2 ; y = 0,1
Khối lượng của Al và Mg là:
mAg = 0,2.27=5,4(gam)
mMg = 7,8 – 5,4 = 2,4(gam)
c. Theo phương trình số mol của H2SO4 là : 0,3 + 0,1 = 0,4(mol)
Thể tích dung dịch H2SO4 2M đã tham gia phản ứng là:
V = 0,4/2=0,2 lít
Gọi nMg = a (mol); nAl = b (mol)
=> 24a + 27b = 7,8 (1)
nH2 = 8,96/22,4 = 0,4 (mol)
PTHH:
Mg + H2SO4 -> MgSO4 + H2
a ---> a ---> a ---> a
2Al + 3H2SO4 -> 2Al2(SO4)3 + 3H2
b ---> 1,5b ---> b ---> 1,5b
=> a + 1,5b = 0,4 (2)
(1)(2) => a = 0,1 (mol); b = 0,2 (mol)
mMg = 0,1 . 24 = 2,4 (g)
mAl = 0,2 . 27 = 5,4 (g)
nH2SO4 = 0,1 + 0,3 . 1,5 = 0,4 (mol)
VddH2SO4 = 0,3/2 = 0,2 (l)

Câu 1:
\(n_{H_2}=\dfrac{2.91362}{22.4}=0.13mol\)
\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
a a a a
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
2b 3b b 3b
Ta có: \(\left\{{}\begin{matrix}24a+54b=2.58\\a+3b=0.13\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0.04\\b=0.03\end{matrix}\right.\)
\(m_{Mg}=0.04\times24=0.96g\)
\(m_{Al}=0.03\times2\times27=1.62g\)
\(V_{H_2SO_4}=\dfrac{0.04+3\times0.03}{0.5}=0.26l\)
Câu 2:
\(n_{H_2}=\dfrac{3.136}{22.4}=0.14mol\)
\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
a a a a
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
b b b b
Ta có: \(\left\{{}\begin{matrix}24a+56b=4.96\\a+b=0.14\end{matrix}\right.\)\(\Leftrightarrow\left\{{}\begin{matrix}a=0.09\\b=0.05\end{matrix}\right.\)
\(m_{Mg}=0.09\times24=2.16g\)
\(m_{Fe}=0.05\times56=2.8g\)
\(C\%_{H_2SO_4}=\dfrac{0.14\times98\times100}{200}=6.86\%\)
Câu 3:
\(n_{H_2}=\dfrac{1.568}{22.4}=0.07mol\)
\(Ba+H_2SO_4\rightarrow BaSO_4+H_2\)
a a a a
\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
b b b b
Ta có: \(\left\{{}\begin{matrix}137a+24b=3.94\\a+b=0.07\end{matrix}\right.\)\(\Leftrightarrow\left\{{}\begin{matrix}a=0.02\\b=0.05\end{matrix}\right.\)
\(m_{Ba}=0.02\times137=2.74g\)
\(m_{Mg}=0.05\times24=1.2g\)
\(CM_{H_2SO_4}=\dfrac{0.07}{0.1}=0.7M\)

a. PTHH : Mg + 2HCl ➝ MgCl2 + H2 (1)
b. theo bài : nH2 = 3,36 : 22,4 = 0,15 (mol)
theo (1) nMg = nH2 = 0,15 (mol)
➞ mMg = 0,15 ✖ 24 = 3,6 (g)
➞ %mMg = (3,6 : 5)✖100 = 72%
➞ %mCu = 100% - 72% = 28%
c. theo (1) nHCl = 2nH2 = 2✖0,15 = 0,3 (mol)
mHCl = 0,3✖36,5 = 10,95(g)
➜mddHCl = (10,95✖100):14,6 = 75(g)
d. dung dịch Y : MgCl2
mdd(spư)= 3,6+75-0,3 = 78,3(g)
theo (1) nMgCl2 = nH2 = 0,15(mol)
mMgCl2 = 0,15✖95 = 14,25(g)
C%MgCl2 = (14,25 : 78,3)✖100 = 18,199%



Tham khảo
Ta có pthh
2Al + 3H2SO4 →→ Al2(SO4)3 + 3H2 (1)
Mg + H2SO4 →→ MgSO4 + H2 (2)
Theo đề bài ta có
VH2=1568 ml =1,568 l
-> nH2=1,56822,4=0,07(mol)1,56822,4=0,07(mol)
Gọi x là số mol của H2 tham gia vào pthh 1
Số mol của H2 tham gia vào pthh2 là 0,07 -x mol
Theo pthh 1 và 2 ta có
nAl=2/3 nH2=2/3x mol
nMg=nH2=(0,07-x) mol
Theo đề bài ta có hệ pt
27.2/3x + 24.(0,07-x)=1,41
⇔⇔ 18x + 1,68 - 24x = 1,41
⇔⇔ -6x = -0,27
-> x= 0,045 mol
-> nAl=2/3.0,045=0,03 mol
nMg=(0,07-0,045)=0,025 mol
Ta có
nH2SO4 (1) và (2) = nH2 = 0,07 mol
-> mct=mH2SO4=0,07.98=6,68 g
mddH2SO4=mct.100%C%=6,68.100%1,96%=350gmct.100%C%=6,68.100%1,96%=350g
mdd(sau-phan-ung) = mhh + mddH2SO4 - mH2 = 1,41 +350 - (0,07.2)=351,27 g
Theo pthh 1
nAl2(SO4)3=1/2nAl=1/2.0,03=0,015 mol
->mAl2(SO4)3=0,015.342=5,13 g
Theo pthh 2
nMgSO4=nMg=0,025 mol
->mMgSO4=0,025.120=3g
⇒⇒ C%Al2(SO4)3=5,13351,27.100%≈1,46%Al2(SO4)3=5,13351,27.100%≈1,46%
C%MgSO4=3351,27.100%≈0,854%