Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

n H 2 = 0,336 22,4 = 0,015 m o l
Ta có:
n O H - t r o n g b a z ơ = 2 . n H 2 = 2 . 0 , 015 = 0 , 03 m o l
m b a z ơ = m k i m l o ạ i + m O H - = 0 , 85 + 0 , 03 . 17 = 1 , 36 g a m .
Chọn A.

1.
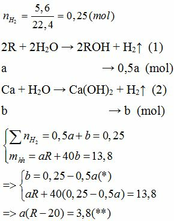
Vì b > 0, từ (*) => a < 0,25/0,5 = 0,5 thế vào (**)
=> R – 20 > 7,6
=> R > 27,6 (***)
Khi cho 8,58 gam R tác dụng với lượng dư HCl thì lượng H2 thoát ra lớn hơn 2,24 (lít)
2R + 2HCl → 2RCl + H2↑ (3)
Theo PTHH (3):
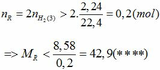
Từ (***) và (****) => 27, 6 < MR < 42,9
Vậy MR = 39 (K) thỏa mãn
2.
Ta có:
=> nKOH = nK = 0,2 (mol)
nCa(OH)2 = nCa = 0,15 (mol)
∑ nOH- = nKOH + 2nCa(OH)2 = 0,2 + 2.0,15 = 0,5 (mol)
Khi cho hỗn hợp Z ( N2, CO2) vào hỗn hợp Y chỉ có CO2 phản ứng
CO2 + OH- → HCO3- (3)
CO2 + 2OH- → CO32- + H2O (4)
CO32- + Ca2+ → CaCO3↓ (5)
nCaCO3 = 8,5/100 = 0,085 (mol) => nCO32-(5) = nCaCO3 = 0,085 (mol)
Ta thấy nCaCO3 < nCa2+ => phương trình (5) Ca2+ dư, CO32- phản ứng hết
TH1: CO2 tác dụng với OH- chỉ xảy ra phản ứng (4)
Theo (4) => nCO2 = nCO32-(4) = nCaCO3 = 0,085 (mol)
=> VCO2(đktc) = 0,085.22,4 = 1,904 (lít)
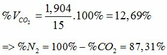
TH2: CO2 tác dụng với OH- xảy ra cả phương trình (3) và (4)
Theo (4): nCO2 = nCO32- = 0,085 (mol)
nOH- (4) = 2nCO32- = 2. 0,085 = 0,17 (mol)
=> nOH- (3)= ∑ nOH- - nOH-(4) = 0,5 – 0,17 = 0,33 (mol)
Theo PTHH (3): nCO2(3) = nOH- = 0,33 (mol)
=> ∑ nCO2(3+4) = 0,085 + 0,33 = 0,415 (mol)
=> VCO2 (ĐKTC) = 0,415.22,4 = 9,296 (lít)
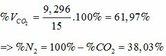

2Al + F e 2 O 3 → A l 2 O 3 + 2Fe
n H 2 (p1) = 3,08/22,4 = 0,1375 mol
n H 2 (p2) = 0,84/22,4 = 0,0375 mol
Thấy phần 2 tác dụng với NaOH sinh ra khí, suy ra sản phẩm có Al dư.
Vậy rắn Y gồm A l 2 O 3 , Fe và Al dư.
Phần 2:
2Al + 2NaOH + 2 H 2 O
→ 2 N a A l O 2 + 3 H 2
Theo PTPU ta có:
n A l (p2) = 2/3 n H 2 (p2)
= 2/3 . 0,0375 = 0,025 mol
⇒ n A l (p1) = n A l (p2) = 0,025 mol
Phần 1:
Fe + H 2 S O 4 → F e S O 4 + H 2 (*)
2Al + 3 H 2 S O 4
→ A l 2 S O 4 3 + 3 H 2 (**)
Theo (**) ta có:
n H 2 (**) = 3/2 n A l (p1)
= 3/2 . 0,025 = 0,0375 mol
⇒ n H 2 (*) = n H 2 (p1) - n H 2 (**)
= 0,1375 - 0,0375 = 0,1 mol
⇒ n F e (p1) = n H 2 (*)=0,1 mol
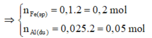
⇒ n A l pư = n F e sp = 0,2 mol
⇒ n F e 2 O 3 = 1/2 . n F e sp
= 1/2 . 0,2 = 0,1 mol
m h h = m F e 2 O 3 + m A l p u + m A l d u
= 0,1.160+0,05.27+0,2.27=22,75g
⇒ Chọn D.

\(a)n_{Fe}=\dfrac{5,6}{56}=0,1mol\\ n_{Mg}=\dfrac{4,8}{24}=0,2mol\\ Fe+2HCl\rightarrow FeCl_2+H_2\)
0,1 0,2 0,1 0,1
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
0,2 0,4 0,2 0,2
\(V_{H_2}=\left(0,1+0,2\right).22,4=6,72l\\ b)V_{ddHCl}=\dfrac{0,2+0,4}{2}=0,3l\\ c)m_{muối}=0,1.127+95.0,2=31,7g\)

Lần trước em đăng đề thiếu nên mới không làm được nhé em !
a) Đặt x, y lần lượt là số mol Ba,Al trong hỗn hợp A
Cho m gam A + H2O dư
=> Phần không tan C là Al dư
Ba + 2H2O → Ba(OH)2 + H2
x--------------------->x-------->x
2Al + Ba(OH)2 + 2H2O → Ba(AlO2)2 + 3H2
2x<-----x---------------------------->x----------->3x
=>\(n_{H_2}=x+3x=\dfrac{1,344}{22,4}=0,06\) (1)
Cho 2m gam A + Ba(OH)2 dư
=> Số mol Ba,Al lần lượt là 2x; 2y
Vì kiềm dư nên cả 2 kim loại đều tan hết
Ba + 2H2O → Ba(OH)2 + H2
2x------------------->2x-------->2x
2Al + Ba(OH)2 + 2H2O → Ba(AlO2)2 + 3H2
2y----->y-------------------------->y----------->3y
=>\(n_{H_2}=2x+3y=\dfrac{20,832}{22,4}=0,93\) (2)
Từ (1), (2) => x=0,015 (mol) ; y=0,3(mol)
\(\Rightarrow m_{Ba}=0,015.137=2,005\left(mol\right);m_{Al}=0,3.27=8,1\left(g\right)\)
b) Dung dịch B chứa Ba(AlO2)2 : 0,015(mol)
\(n_{Al\left(OH\right)_3}=\dfrac{0,78}{78}=0,01\left(mol\right)\)
TH1: Kết tủa chưa đạt giá trị max và còn Ba(AlO2)2 dư
Ba(AlO2)2 + 2HCl + 2H2O → BaCl2 + 2Al(OH)3
Theo PT: \(n_{HCl}=n_{Al\left(OH\right)_3}=0,01\left(mol\right)\)
=> \(CM_{HCl}=\dfrac{0,01}{0,05}=0,2M\)
TH2: Kết tủa đạt giá trị max và bị HCl dư hòa tan 1 phần
Ba(AlO2)2 + 2HCl + 2H2O → BaCl2 + 2Al(OH)3
0,015-------->0,03----------------------------->0,03
\(n_{Al\left(OH\right)_3\left(bihoatan\right)}=0,03-0,01=0,02\left(mol\right)\)
Al(OH)3 + 3HCl → AlCl3 + 3H2O
0,02-------->0,06
=> \(\Sigma n_{HCl}=0,03+0,06=0,09\left(mol\right)\)
=> \(CM_{HCl}=\dfrac{0,09}{0,05}=1,8M\)

Tính % thể tích các khí :
% V C 2 H 2 = 0,448/0,896 x 100% = 50%
% V CH 4 = % V C 2 H 6 = 25%

\(n_{H2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
a) Pt : \(2Na+2H_2O\rightarrow2NaOH+H_2|\)
2 2 2 1
a 0,5a
\(2K+2H_2O\rightarrow2KOH+H_2|\)
2 2 2 1
b 0,5b
b) Gọi a là số mol của Na
b là số mol của K
\(m_{Na}+m_K=10,1\left(g\right)\)
⇒ \(n_{Na}.M_{Na}+n_K.M_K=10,1g\)
⇒ 23a + 39b = 10,1g (1)
Theo phương trình : 0,5a + 0,5b = 0,15(2)
Từ(1),(2), ta có hệ phương trình :
23a + 39b = 10,1g
0,5a + 0,5b = 0,15
⇒ \(\left\{{}\begin{matrix}a=0,1\\b=0,2\end{matrix}\right.\)
\(m_{Na}=0,1.23=2,3\left(g\right)\)
\(m_K=0,2.39=7,8\left(g\right)\)
0/0Na = \(\dfrac{2,3.100}{10,1}=22,77\)0/0
0/0K = \(\dfrac{7,8.100}{10,1}=77,23\)0/0

Ca + 2 H 2 O → C a O H 2 + H 2
x……...x………x….mol
Ba + 2 H 2 O → B a O H 2 + H 2
y……y……..y……mol
Giải hệ phương trình:
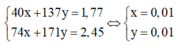
⇒ n H 2 = x+y = 0,02 mol
⇒ V H 2 = 0,02.22,4 = 0,448 lit
⇒ Chọn B.
⇒ Chọn D.