Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Fe + 2HCl --> FeCl2 + H2
nFe = \(\dfrac{11,2}{56}\)=0,2 mol . Theo tỉ lệ phản ứng => nFeCl2 = nH2 = 0,2 mol
a. H2 + CuO --> Cu + H2O
nCuO = nH2 => mCuO = 0,2 . 80 = 16 gam
b. mFeCl2 = 0,2 .127= 25,4 gam

PTPU :
Fe + 2HCl --> FeCl2 + H2
H2 + CuO --> Cu + H2O
TBR, ta có nFe = 11,2 /56 = 0,2 (mol)
Theo PTHH, nFeCl2 = nH2 = 0,2 mol
Theo PTHH nCuO = nH2 => mCuO = 0,2 . 80 = 16 gam
TBR, ta có: mFeCl2 = 0,2 .127= 25,4 gam
Vậy

\(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
Pt : \(Fe+2HCl\rightarrow FeCl_2+H_2|\)
1 2 1 1
0,2 0,4 0,2 0,2
a) \(n_{H2}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
\(V_{H2\left(dktc\right)}=0,2.22,4=4,48\left(l\right)\)
b) \(n_{FeCl2}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
⇒ \(m_{FeCl2}=0,2.127=25,4\left(g\right)\)
c) \(n_{HCl}=\dfrac{0,2.2}{1}=0,4\left(mol\right)\)
⇒ \(m_{HCl}=0,.4.36,5=14,6\left(g\right)\)
Chúc bạn học tốt

Bài 1: Ta có: \(n_{Mg}=\dfrac{24}{24}=1\left(mol\right)\)
PT: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
____1_____2_____________1 (mol)
a, Ta có: \(V_{H_2}=1.22,4=22,4\left(l\right)\)
b, Ta có: \(m_{HCl}=2.36,5=73\left(g\right)\)
Bài 2: Ta có: \(n_{CuO}=\dfrac{100}{80}=1,25\left(mol\right)\)
PT: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
___1,25_______1,25__1,25 (mol)
a, Ta có: \(m_{Cu}=1,25.64=80\left(g\right)\)
b, \(m_{H_2O}=1,25.18=22,5\left(g\right)\)
Bạn tham khảo nhé!

PTHH
Fe + 2HCl --> FeCl2 + H2
PT: 1 2 1 1 (mol)
Đề: 0,2 0,4 0,2 0,2 (mol)
Số mol của fe là : nfe = m : M =11,2 : 56=0,2 mol
Tính n H2 bằng cách áp dụng quy tắc tam suất đó bạn
Vh2 = n . 22.4 =0,2 .22,4 = 4,48 (l)
khối lượng của FeCl2 là
mfecl2 = n.M =0,2 .127 = 25,4(g)
khối lg của hcl là
m hcl = n.M =0,4 . 36,5 = 14,6 (g)

PTHH: Fe + 2HCl--> FeCl2 + H2
Ta có : nFe= \(\dfrac{11,2}{56}\)= 0,2 ( mol)
a. Tìm V gì bạn??
b. Theo pthh, ta có: nFeCl2= nFe= 0,2( mol)
.=> mFeCl2= 0,2.127=25,4(g)
c. Theo pthh, ta có nHCl= 2nFe= 0,4( mol)
=> mHCl= 0,4.36,5=14,6(g)

Ta có: \(n_{Fe}=\dfrac{8,4}{56}=0,15\left(mol\right)\)
\(n_{CuO}=\dfrac{16}{80}=0,2\left(mol\right)\)
\(PTHH:\)
\(Fe+2HCl--->FeCl_2+H_2\left(1\right)\)
\(CuO+H_2\overset{t^o}{--->}Cu+H_2O\left(2\right)\)
a. Theo PT(1): \(n_{H_2}=n_{Fe}=0,15\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,15.22,4=3,36\left(lít\right)\)
b. Ta thấy: \(\dfrac{0,15}{1}< \dfrac{0,2}{1}\)
Vậy CuO dư.
Theo PT(2): \(n_{Cu}=n_{H_2}=0,15\left(mol\right)\)
\(\Rightarrow m_{Cu}=0,15.64=9,6\left(g\right)\)
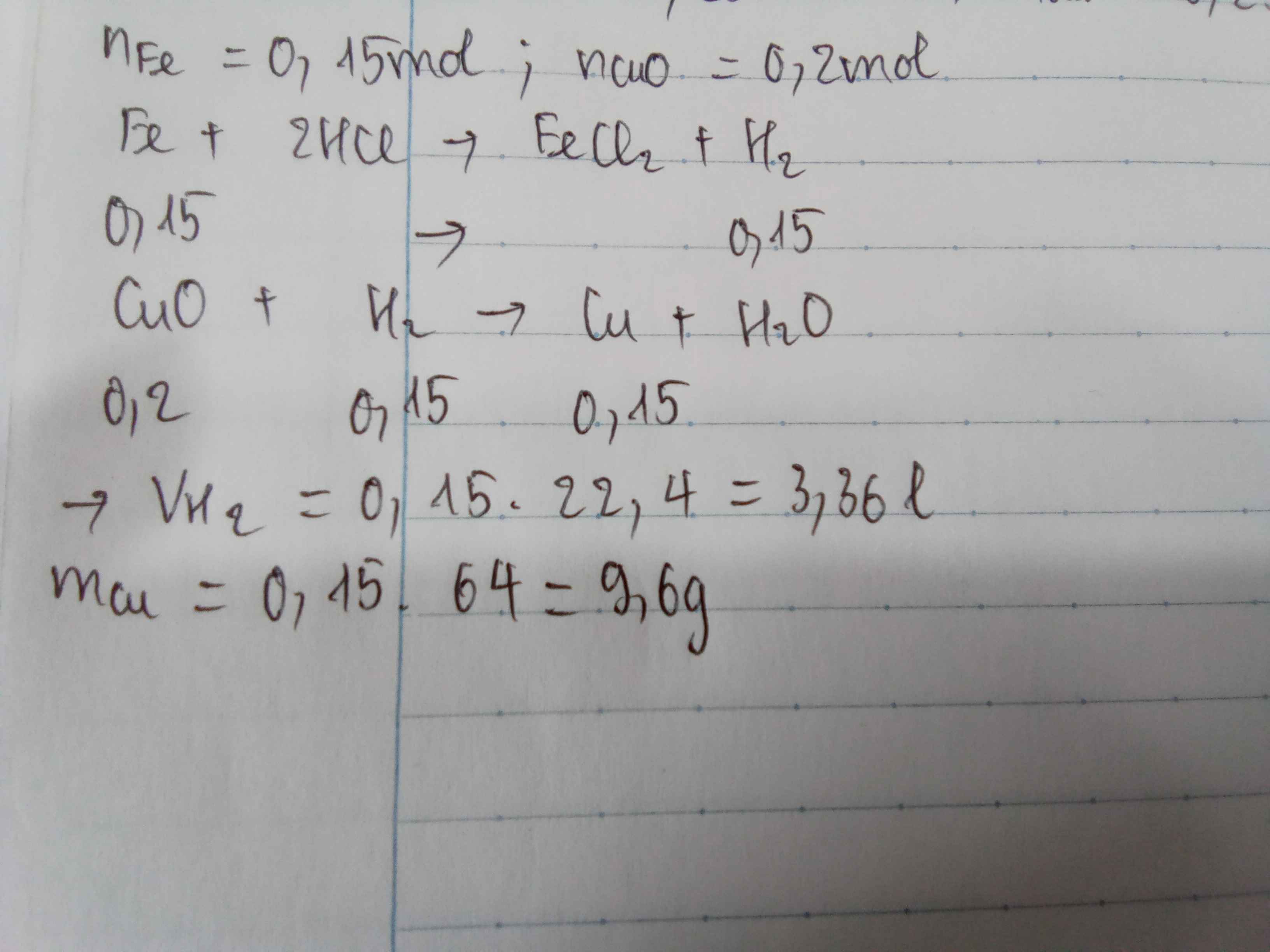

a) PTHH: Fe + 2HCl ===> FeCl2 + H2
H2 + CuO =(nhiệt)=> Cu + H2O
Ta có: nFe = \(\frac{11,2}{56}=0,2\left(mol\right)\)
=> nH2 = nCuO = nFe = 0,2 (mol)
=> mCuO = 0,2 x 80 = 16 (gam) = m
b) Theo phương trình, nFeCl2 = nFe = 0,2 (mol)
=> mFeCl2 = 0,2 x 127 = 25,4 (gam)
nFe=m:M=11,2:56=0,2mol
PT:Fe+HCl--->FeCl2+H2
theo PT:1mol:1mol:1mol:1mol
theo đề:0,2mol:0,2mol:0,2mol:0,2mol
CuO+H2--->Cu+H2O
theo PT:1mol:1mol:1mol:1mol
theo đề:0,2mol:0,2mol:0,2mol:0,2mol
a.mCuO=n.M=0,2.80=16g
b.mFeCl2=n.M=0,2.127=25,4g