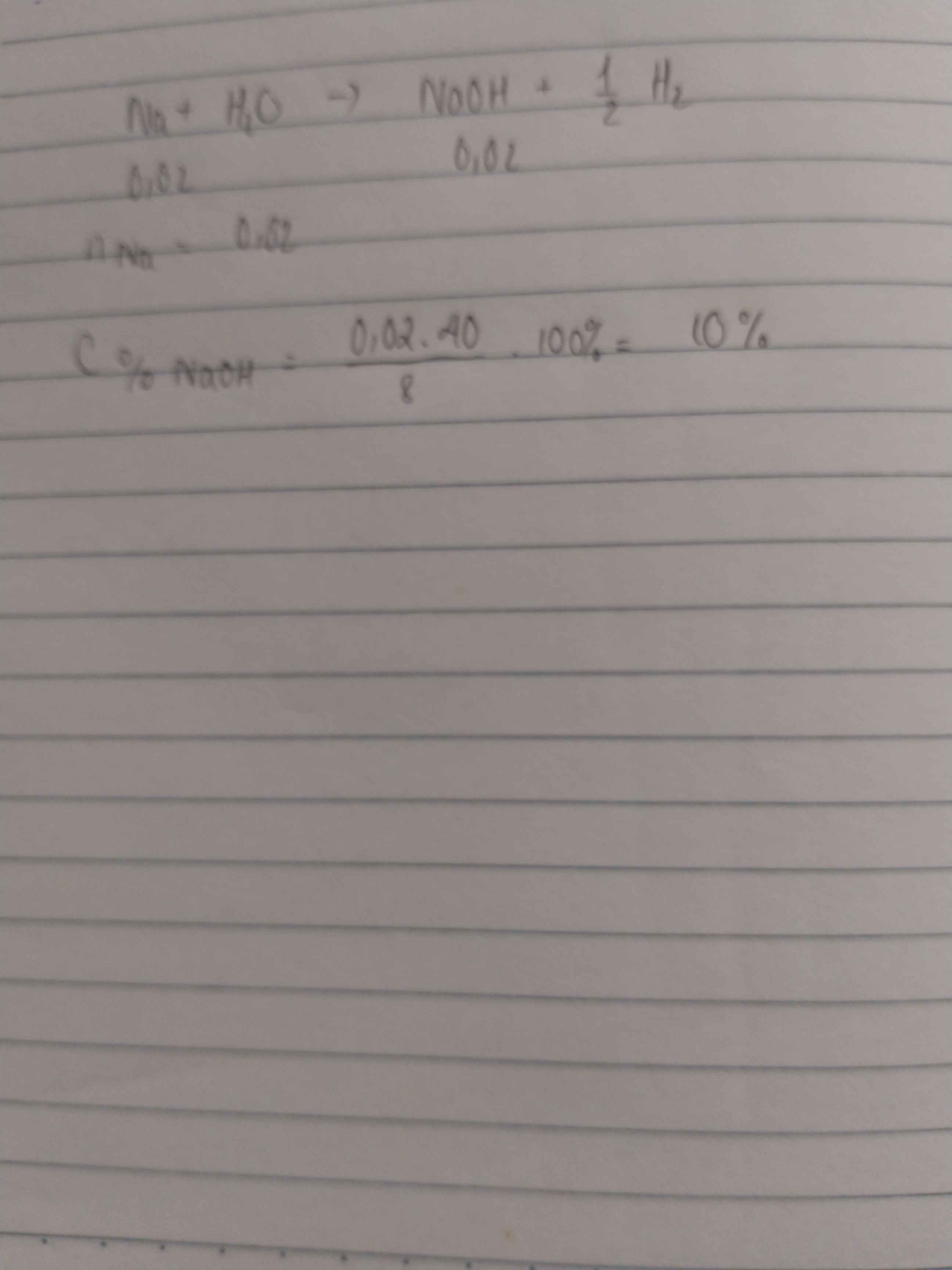Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) \(n_{FeCl_3}=\dfrac{16,25}{162,5}=0,1\left(mol\right)\)
PTHH: Fe2O3 + 6HCl --> 2FeCl3 + 3H2O
0,05<----0,3<-----0,1
=> \(m_{Fe_2O_3}=0,05.160=8\left(g\right)\)
b)
\(m_{HCl\left(bd\right)}=91,25.16\%=14,6\left(g\right)\)
mdd sau pư = 8 + 91,25 = 99,25 (g)
\(\left\{{}\begin{matrix}C\%\left(FeCl_3\right)=\dfrac{16,25}{99,25}.100\%=16,373\%\\C\%\left(HCldư\right)=\dfrac{14,6-0,3.36,5}{99,25}.100\%=3,678\%\end{matrix}\right.\)

MnO 2 + HCl → MnCl 2 + Cl 2 + 2 H 2 O
Cl 2 + 2NaOH → NaCl + NaClO + H 2 O
n MnO 2 = 0,2 mol; n NaOH = 0,729 mol
Theo phương trình (1) ta có: n Cl 2 = n MnO 2 = 0,2 mol
Theo phương trình (2) ta có: 2 n Cl 2 < n NaOH ⇒ NaOH dư
Dung dịch A gồm: n NaCl = n NaClO = n Cl 2 = 0,2 mol
n NaOH dư = 0,729 – 2.0,2 = 0,329 mol
m dd A = m Cl 2 + m dd NaOH = 0,2.71 + 145,8 = 160g
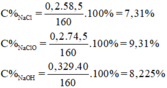

a) \(n_{Al}=\dfrac{8,64}{27}=0,32\left(mol\right)\)
\(n_{HCl}=\dfrac{365.10\%}{36,5}=1\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
Xét tỉ lệ \(\dfrac{0,32}{2}< \dfrac{1}{6}\) => Al hết, HCl dư
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
0,32-->0,96---->0,32--->0,48
=> \(V_{H_2}=0,48.22,4=10,752\left(l\right)\)
b) Trong Y chứa AlCl3 và HCl dư
\(m_{AlCl_3}=0,32.133,5=42,72\left(g\right)\)
c) mdd sau pư = 8,64 + 365 - 0,48.2 = 372,68 (g)
\(\left\{{}\begin{matrix}C\%\left(AlCl_3\right)=\dfrac{42,72}{372,68}.100\%=11,463\%\\C\%\left(HCldư\right)=\dfrac{\left(1-0,96\right).36,5}{372,68}.100\%=0,392\%\end{matrix}\right.\)

\(n_{Na}=\dfrac{9,2}{23}=0,4\left(mol\right)\)
PTHH: 2Na + 2H2O --> 2NaOH + H2
_____0,4----------------->0,4----->0,2
=> mNaOH = 0,4.40 = 16(g)
mdd = 9,2 + 50 - 0,2.2 = 58,8(g)
=> \(C\%=\dfrac{16}{58,8}.100\%=27,21\%\)
=> D

a,
- Giả sử X là F (không tạo kết tủa) \(\Rightarrow\) Y là Cl.
\(AgNO_3+NaCl\rightarrow NaCl+AgNO_3\)
\(\rightarrow n_{NaCl}=n_{AgCl}=0,331\left(mol\right)\)
\(\Rightarrow m_{NaCl}=19,36< 22\left(g\right)\left(TM\right)\)
- Giả sử X, Y đều tạo kết tủa. Gọi chung là R.
nNaR= nAgR
\(\Rightarrow\frac{22}{23+R}=\frac{47,5}{108+R}\)
\(\Leftrightarrow47,5\left(23+R\right)=22\left(108+R\right)\)
\(\Leftrightarrow R=50,3\left(Cl;Br\right)\left(TM\right)\)
Vậy NaX, NaY có thể là NaF, NaCl hoặc NaCl, NaBr.
b,
- Trường hợp NaF, NaCl:
mNaCl= 19,36g
\(\Rightarrow C\%_{NaCl}=\frac{19,36.100}{200}=9,68\%\)
\(m_{NaF}=22-19,36=2,64\left(g\right)\)
\(\Rightarrow C\%_{NaF}=\frac{2,64.100}{200}=1,32\%\)
Trường hợp NaCl, NaBr
Gọi x là mol NaCl; y là mol NaBr
Bảo toàn nguyên tố, n muối= n kết tủa
\(\Rightarrow58,5x+103y=22;143,5x+188y=47,5\)
\(\Rightarrow\left\{{}\begin{matrix}x=0,2\\y=0,1\end{matrix}\right.\)
\(C\%_{NaCl}=\frac{0,2.58,5.100}{200}=5,85\%\)
\(C\%_{NaBr}=\frac{0,1.103.100}{200}=5,15\%\)