Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
nOH- = 2,75.10-1 = 0,275 mol; nH+ = 2,25.10-1 = 0,225 mol
H+ + OH- → H2O
0,225 0,275
nOH- dư = 0,05 mol; nCl- = nHCl = 0,225 mol; nBa2+ = 0,1375 mol
Dung dịch sau phản ứng có chứa BaCl2: 0,1125 mol; Ba(OH)2 dư 0,025 mol
Nồng độ mol của BaCl2 là 0,1125/5 = 0,0225M
Nồng độ mol của Ba(OH) 2 dư là 0,025/5 = 5.10-3M

\(n_{Ba\left(OH\right)_2}=0,3.0,1=0,03\left(mol\right)\\ n_{HCl}=0,2.0,15=0,03\left(mol\right)\\ Ba\left(OH\right)_2+2HCl\rightarrow BaCl_2+2H_2O\\ Vì:\dfrac{n_{Ba\left(OH\right)_2\left(đề\right)}}{n_{Ba\left(OH\right)_2\left(PTHH\right)}}=\dfrac{0,03}{1}>\dfrac{n_{HCl\left(đề\right)}}{n_{HCl\left(PTHH\right)}}=\dfrac{0,03}{2}\\ \Rightarrow Ba\left(OH\right)_2dư\\ n_{Ba\left(OH\right)_2\left(p.ứ\right)}=\dfrac{n_{HCl}}{2}=\dfrac{0,03}{2}=0,015\\ n_{Ba\left(OH\right)_2\left(dư\right)}=0,03-0,015=0,015\left(mol\right)\\ \left[OH^-\right]=2.\left[Ba\left(OH\right)_2\left(dư\right)\right]=\dfrac{0,015}{0,3+0,2}=0,03\left(M\right)\\ \Rightarrow pH=14+log\left[OH^-\right]=14+log\left[0,03\right]\approx12,477\)
Nồng độ mol/lít các ion trong dd A:
\(\left[OH^-\left(dư\right)\right]=0,06\left(M\right)\left(nt\right)\\\left[Cl^-\right]=2.\left[BaCl_2\right]=2.\left(\dfrac{0,015}{0,5}\right)=0,06\left(M\right)\\ \left[Ba^{2+}\right]=0,03+ 0,03=0,06\left(M\right)\)

Đáp án A
nH+ = 0,01.0,2 =0,002 ⇒ nH2SO4 = 0,001
nOH- = 0,1 . 0,1 = 0,01 ⇒ nBa(OH)2 =0,005
⇒ Ba(OH)2 dư
⇒ nBaSO4 = n H2SO4 = 0,001 ⇒ m↓ = 0,233g
Đáp án A.

Đáp án B
nH+ ban đầu = 0,1.2.0,1 + 0,2.0,1 + 0,3.0,1 = 0,07
dung dịch C có pH=1 ⇒ nH+/C = 0,1.(0,3 + V)
⇒ nH+ ban đầu = nH+/C + nOH- ⇒ 0,07 = 0,1.(0,3 + V) + 0,2V +0,1.2V
⇒ V =0,08l

a, \(n_{OH^-}=10^{-1}.V_A\left(mol\right)\)
\(n_{H^+}=10^{-2}.V_B\left(mol\right)\)
\(n_{OH^-dư}=10^{-2}.\left(V_A+V_B\right)\left(mol\right)\)
Ta có: \(n_{OH^-}-n_{OH^-dư}=n_{H^+}\)
\(\Leftrightarrow10^{-1}.V_A-10^{-2}.\left(V_A+V_B\right)=10^{-2}.V_B\)
\(\Leftrightarrow0,09V_A=0,02V_B\)
\(\Rightarrow\dfrac{V_A}{V_B}=\dfrac{2}{9}\)
b, Ta có: \(\left\{{}\begin{matrix}V_A+V_B=0,55\\\dfrac{V_A}{V_B}=\dfrac{2}{9}\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}V_A=0,1\left(l\right)\\V_B=0,45\left(l\right)\end{matrix}\right.\)
\(n_{BaCl_2}=\dfrac{1}{2}n_{Cl^-}=\dfrac{1}{2}n_{H^+}=\dfrac{1}{2}.10^{-2}.0,1=0,0005\left(mol\right)\Rightarrow m_{BaCl_2}=0,104\left(g\right)\)
\(n_{Ba\left(OH\right)_2}=\dfrac{1}{2}n_{OH^-dư}=\dfrac{1}{2}.10^{-2}.0,55=0,00275\left(mol\right)\Rightarrow m_{Ba\left(OH\right)_2}=0,047025\left(g\right)\)
\(\Rightarrow\%m_{Ba\left(OH\right)_2}=\dfrac{0,047025}{0,047025+0,104}.100\%=31,14\%\)
\(\Rightarrow\%m_{BaCl_2}=62,86\%\)

Chọn B
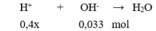
Dung dịch sau phản ứng có pH = 2 < 7 nên dung dịch sau phản ứng có H + dư
→ 0,4x – 0,033 = 10 - 2 .0,3 → x = 0,09
a, \(\left[H^+\right]=10^{-5}\Rightarrow n_{H^+}=0,22.10^{-5}\left(mol\right)\)
\(\left[OH^-\right]=10^{-5}\Rightarrow n_{OH^-}=0,18.10^{-5}\left(mol\right)\)
\(\Rightarrow n_{H^+dư}=0,04.10^{-5}=4.10^{-7}\left(mol\right)\)
\(\Rightarrow\left[H^+\right]=\dfrac{4.10^{-7}}{0,22+0,18}=10^{-8}\)
\(\Rightarrow pH=8\)