Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a)
\(m_{C_2H_2} = m_{tăng} = 5,2\ gam\\ \Rightarrow n_{C_2H_2} = \dfrac{5,2}{26} = 0,2(mol)\)
Vậy :
\(\%V_{C_2H_2} = \dfrac{0,2.22,4}{8,96}.100\% = 50\%\\ \%V_{CH_4} = 100\%-50\% = 50\%\)
b)
\(n_{CH_4} = n_{C_2H_2} = 0,2(mol)\)
CH4 + O2 \(\xrightarrow{t^o}\) CO2 + H2O
0,2.........................0,2...................................(mol)
C2H2 + \(\dfrac{5}{2}\)O2 \(\xrightarrow{t^o}\) 2CO2 + H2O
0,2................................0,4.................................(mol)
CO2 + Ca(OH)2 → CaCO3 + H2O
(0,2+0,4)............................(0,2+0,4)........................................(mol)
\(\Rightarrow m_{CaCO_3} =(0,2 + 0,4).100 = 60(gam)\)

PTHH: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
a) Ta có: \(n_{Br_2}=\dfrac{4}{160}=0,025\left(mol\right)=n_{C_2H_4}\)
\(\Rightarrow\%V_{C_2H_4}=\dfrac{0,025}{\dfrac{5,6}{22,4}}\cdot100\%=10\%\) \(\Rightarrow\%V_{CH_4}=90\%\)
b) Theo PTHH: \(n_{C_2H_4Br_2}=n_{Br_2}=0,025mol\)
\(\Rightarrow m_{C_2H_4Br_2}=0,025\cdot188=4,7\left(g\right)\)
c) Ta có: \(n_{CH_4}=\dfrac{1}{22,4}=\dfrac{5}{112}\left(mol\right)=n_{O_2}\)
\(\Rightarrow\left\{{}\begin{matrix}m_{CH_4}=\dfrac{5}{112}\cdot16\approx0,71\left(g\right)\\m_{O_2}=\dfrac{5}{112}\cdot32\approx1,43\left(g\right)\end{matrix}\right.\)
Vậy 1 lít Metan nhẹ hơn 1 lít Oxi

Cho hỗn hợp qua dung dịch brom dư
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
Khí thoát ra là \(CH_4\)
\(CH_4+2O_2\rightarrow^{t^o}CO_2+2H_2O\)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
Ta có:
\(n_{CaCO_3}=\frac{40}{100}=0,4mol=n_{CO_2}=n_{CH_4}\)
\(\rightarrow V_{CH_4}=0,4.22,4=8,96l\)
\(\rightarrow\%V_{CH_4}=\frac{8,96}{13,56}=66\%\rightarrow\%V_{C_2H_4}=34\%\)

nBr2 = 0,125 mol
Khi đốt cháy nA = 0,25 mol
mNaOH ban đầu = 36g => nNaOH = 0,9 mol
Gọi x, y lần lượt là số mol của CO2 và H2O
mdd = 180 + 44x + 18y
Vì NaOH dư do đó chỉ tạo muối trung hòa
CO2 +2NaOH → Na2CO3 + H2O
x 2x
nNaOH dư = 0,9 – 2x
có 2 , 75 % = 40 ( 0 , 9 - 2 x ) 180 + 44 x + 18 y . 100 % (1)
=> 81,21x + 0,495y = 31,05n
2,8 lít khí A tác dụng với 0,125 mol Br2
=> 5,6 lít khí A tác dụng với 0,25 mol Br2
Gọi số mol khí của CH4, C2H4 và C2H2 lần lượt là a; b; c
Ta có a + b + c = 0,25 mol
Và b + 2c = 0,25
=> a = c
=> khi đốt cháy hỗn hợp A cho nCO2 = nH2O
Thay vào (1) => x = y = 0,38 mol
Bảo toàn C, H khi đốt cháy ta có
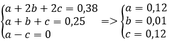
=> %VCH4 = %VC2H2 = 48%
%VC2H4 = 4%

a) mtăng = mC2H4
=> \(n_{C_2H_4}=\dfrac{5,6}{28}=0,2\left(mol\right)\)
=> \(\%V_{C_2H_4}=\dfrac{0,2.22,4}{13,44}.100\%=33,33\%\)
\(\%V_{CH_4}=100\%-33,33\%=66,67\%\)
b) \(n_{CH_4}=\dfrac{13,44.66,67\%}{22,4}=0,4\left(mol\right)\)
PTHH: CH4 + 2O2 --to--> CO2 + 2H2O
0,4--------------->0,4
C2H4 + 3O2 --to--> 2CO2 + 2H2O
0,2----------------->0,4
Ca(OH)2 + CO2 --> CaCO3 + H2O
0,8----->0,8
=> mCaCO3 = 0,8.100 = 80 (g)
a.\(m_{tăng}=m_{C_2H_4}=5,6g\)
\(n_{hh}=\dfrac{13,44}{22,4}=0,6mol\)
\(n_{C_2H_4}=\dfrac{5,6}{28}=0,2mol\)
\(\%V_{C_2H_4}=\dfrac{0,2}{0,6}.100=33,33\%\)
\(\%V_{CH_4}=100\%-33,33\%=66,67\%\)
b.\(C_2H_4+3O_2\rightarrow\left(t^o\right)2CO_2+2H_2O\)
0,2 0,4 ( mol )
\(CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\)
0,4 0,4 ( mol )
\(n_{CO_2}=0,4+0,4=0,8mol\)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
0,8 0,8 ( mol )
\(m_{CaCO_3}=0,8.100=80g\)

nhh = 5.6/22.4 = 0.25 (mol)
nBr2 = 0.5*0.2 = 0.1 (mol)
C2H4 + Br2 => C2H4Br2
0.1_____0.1
nCH4 = 0.25 - 0.1 = 0.15 (mol)
VC2H4 = 0.1*22.4 = 2.24 (l)
VCH4 = 0.15*22.4 = 3.36 (l)
mCH4 = 0.15*16 = 2.4 (g)
mC2H4 = 0.1*28 = 2.8 (g)
%mCH4 = 2.4/(2.4 + 2.8) * 100% = 46.15%
%mC2H4 = 100 - 46.15 = 53.85%
Chúc bạn học tốt !!!

\(n_{hhkhí}=\dfrac{7,84}{22,4}=0,35\left(mol\right)\\ m_{tăng}=m_{C_2H_4}=4,2\left(g\right)\\ n_{C_2H_4}=\dfrac{4,2}{28}=0,15\left(mol\right)\\ n_{CH_4}=0,35-0,15=0,2\left(mol\right)\\ \left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{0,15}{0,35}=42,85\%\\\%V_{CH_4}=100\%-42,85\%=57,15\%\end{matrix}\right.\)
PTHH:
C2H4 + 3O2 --to--> 2CO2 + 2H2O
0,15 ------------------> 0,3
CH4 + O2 --to--> CO2 + 2H2O
0,2 -----------------> 0,2
Ca(OH)2 + CO2 ---> CaCO3 + H2O
0,5 -------> 0,5
\(m_{CaCO_3}=0,5.100=50\left(g\right)\)

\(n_{O_2}=\dfrac{8}{32}=0.25\left(mol\right)\)
\(CH_4+2O_2\underrightarrow{t^0}CO_2+2H_2O\)
\(0.125....0.25....0.125\)
\(m_{CH_4}=0.125\cdot16=2\left(g\right)\)
\(V_{CO_2}=0.125\cdot22.4=2.8\left(l\right)\)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
\(............0.125.....0.125\)
\(m_{CaCO_3}=0.125\cdot100=12.5\left(g\right)\)
Bạn chia nhỏ câu hỏi ra
bài 5
nBr2 = 0,025 mol
C2H4 + Br2 → C2H4Br2
0,025 <--0,025
⇒ VC2H4 = 0,56 (l)
⇒ %C2H4 = 0,56.100%\5,6= 10%
⇒ %CH4 = (5,6−0,56).100%\5,6= 90%
câu 12
vì A là một hợp chất hữu cơ gồm 2 nguyên tố nên A được tạo bởi C và H
ta có nH=2nH2O=2*5.4\18=2*0.3=0.6 mol
=>mH=0.6*1=0.6g
ta có : mH+mC=mA => mC= mA-mH = 3-0.6=2.4 g
=> nC =2.4\12= 0.2 mol
Gọi CT của A là CxHy
lập tỉ lệ:
x : y= nC : nH= 0.2:0.6=1:3
vậy công thứ tổng quát của A là (CH3)n
Ta có khối lương mol của A =30g
=> M(CH3)n=30
<=> 15n=30
<=>n=2
vậy công thức phân tử của A là C2H6