Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



a) Gọi số mol của FeCO3: x (mol) ;
số mol của FeS2: y (mol)
4FeCO3 + O2 → Fe2O3 + 4CO2↑
x → 0,25x → x (mol)
4FeS2 +11O2 → 2Fe2O3 + 8SO2↑
y → 2,75y → 2y (mol)
∑ nO2 = 0,25x + 2,75y (mol)
Cùng điều kiện về nhiệt độ và áp suất nên tỉ lệ về thể tích = tỉ lệ về số mol
=> nN2 = 4nO2 = 4(0,25x + 2,75y)
=> nN2 = x + 11y (mol)
Vậy hỗn hợp Y gồm:

Khối lượng Fe có trong Z là:

Vì H = 80% => nFe2O3 (trong X) = 0,12. 100% : 80% = 0,15 (mol)
nFe2O3 dư (trong Z) = 0,15 – 0,12 = 0,03 (mol)
Khối lượng tạp chất trong Z = 27,96 – mFe – mFe2O3 dư = 27,96 – 0,24.56 – 0,03.160 = 9,72 (g)
Bảo toàn nguyên tố Fe => nFeCO3 + nFeS2 = 2nFe2O3(trong X)
=> x + y = 0,3 (2)
Từ (1) và (2) => x = 0,18 và y = 0,12 (mol)
Áp dụng công thức PV = nRT ( với n = nCO2 + nSO2 + nN2 = 0,18 + 2. 0,12 + 0,18 +11.0,12 = 1,92)
=> P.10 = 1,92.0,082. (136,5 +273)
=> P = 6,447 ( atm) ≈ 6,5 (atm)
Ta có: mA = mFeCO3 + mFeS2 + mtạp chất = 0,18.116 + 0,12.120 + 9,72 = 45 (g)
![]()
b) hỗn hợp Y gồm:

Cho hỗn hợp Y qua O2 ( xúc tác V2O5 ) có phản ứng sau:

Khối lượng dd sau: mdd sau = mSO3 + mH2O = 0,24. 80 + 592,8 = 612 (g)


Dung dịch Ca(OH)2 không hấp thụ khí CO nên 6,72 lít khí thoát ra chính là khí CO dư.


3. CuO +H2SO4 -->CuSO4 +H2O
nCuO=64/80=0,8(mol)
theo PTHH :nCuO =nH2SO4=nCuSO4=0,8(mol)
=>mddH2SO4 20%=0,8.98.100/20=392(g)
mCuSO4=0,8.160=128(g)
mdd sau phản ứng =64 +392=456(g)
mH2O=456 -128=328(g)
giả sử có a g CuSO4.5H2O tách ra
trong 250g CuSO4 tách ra có 160g CuSO4 và 90g H2O tách ra
=> trong a g CuSO4.5H2O tách ra có : 160a/250 g CuSO4 và 90a/250 g H2O tách ra
=>mCuSO4(còn lại)=128 -160a/250 (g)
mH2O (còn lại)=328 -90a/250 (g)
=>\(\dfrac{128-\dfrac{160a}{250}}{328-\dfrac{90a}{250}}.100=25\)
=>a=83,63(g)

(a)- Khi cho E tác dụng với NaHCO3 sinh ra V lít khí (CO2) và muối natri của X => X là axit
- Ta thấy thể tích khí sinh ra khi cho E tác dụng với Na (khí H2) lớn hơn 0,5 lần thể tích khí khi cho E tác dụng với NaHCO3 (khí CO2) => Y là ancol
Vậy E gồm axit X, ancol Y và este Z (tạo bởi X, Y)
Giả sử V lít tương ứng với 1 (mol) khí
+ nCO2 = n-COOH = 1 (mol)
+ nH2 = 0,5n-COOH + 0,5n-OH => 0,75 = 0,5.1 + 0,5n-OH => n-OH = 0,5 (mol)
+ n hỗn hợp = 2nH2 = 1,5 mol => nX = nY = nZ = 1,5:3 = 0,5 mol
Số chức của axit X là: 1 : 0,5 = 2
Số chức của ancol Y là: 0,5 : 0,5 = 1
=> Este Z có 2 chức
* Đốt cháy muối natri của X:
Muối natri của X có dạng RO4Na2
Gọi số mol muối của X là x (mol)
BTNT Na: nNa2CO3 = n muối = x (mol)
BTNT O: 4n muối + 2nO2 = 2nCO2 + nH2O + 2nNa2CO3
=> 4x + 2nO2 = 0,03.2 + 0,02 + 3x => nO2 = 0,04 – 0,5x (mol)
BTKL: m muối + mO2 = mCO2 + mH2O + mNa2CO3
=> 1,62 + 32(0,04 - 0,5x) = 0,03.44 + 0,02.18 + 106x
=> x = 0,01 mol
=> M muối = 162 => R + 16.4 + 23.2 = 162 => R = 28 => CTPT của X là C4H6O4
* Đun nóng Y với H2SO4 đặc thu được Y1 có tỉ khối so với Y là 34/43 => phản ứng tách nước tạo anken
=> MY1 = MY – 18
=> dY1/Y = (MY-18)/MY = 34/43 => MY = 86 (C5H10O)
Mà khi đun Y1 với KMnO4/H2SO4 thu được Y2 duy nhất, không có khí thoát ra, Y2 có cấu tạo mạch thẳng và là điaxit nên Y1 có cấu tạo mạch vòng, chứa 1 liên kết đôi.
- Cấu tạo Y1:
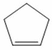
- Cấu tạo Y2: HOOC-(CH2)3-COOH
- Cấu tạo Y: 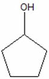
- Cấu tạo X:
HOOC-CH2-CH2-COOH hoặc HOOC-CH(CH3)-COOH
- Cấu tạo Z:
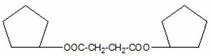
Hoặc
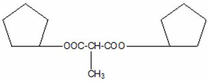
(b)Giả sử số mol mỗi chất trong ½ hỗn hợp G:
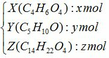
- Khối lượng của ½ hỗn hợp G:
118x + 86y + 254z = 7,8 (1)
- Đốt cháy phần 1 cần nO2 = 9,408 : 22,4 = 0,42 mol:
C4H6O4 + 3,5 O2 → 4CO2 + 3H2O
x 3,5x
C5H10O + 7O2 → 5CO2 + 5H2O
y 7y
C14H22O4 + 17,5O2 → 14CO2 + 11H2O
z 17,5z
Ta có: nO2 = 0,42 => 3,5x + 7y + 17,5z = 0,42 (2)
- Phần 2 tác dụng vừa đủ với nNaOH = 0,04.2 = 0,08 mol:
C2H4(COOH)2 + 2NaOH → C2H4(COONa)2 + 2H2O
x 2x x
C2H4(COOC5H9)2 + 2NaOH → C2H4(COONa)2 + 2C5H9OH
z 2z z 2z
nNaOH = 2nX + 2nZ => 2a + 2c = 0,08 (3)
Từ (1) (2) (3) ta có hệ phương trình:
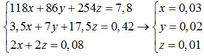
Sau phản ứng thu được:
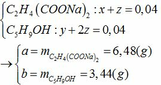

a)
2Al + 6HCl → 2AlCl3 + 3H2↑
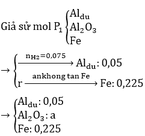
Pt: 2Al + 6H2SO4 → Al2(SO4)3 + 3SO2↑ + 6H2O
2Fe + 6H2SO4 → Fe2(SO4)3 + 3SO2↑ + 6H2O
Al2O3 + 3H2SO4 → Al2(SO4)3 + 3H2O
Giả sử P2 = kP1
=> a=0.1
=> m = 128,8g
b)
2yAl + 3FexOy → yAl2O3 + 3xFe
0,1 0,225
=> 0,225y = 0,3x => 3y = 4x
=> Fe3O4

m rắn giảm = mO (oxit) => nO (oxit) = (1,6 – 1,408) : 16 = 0,012mol
Dễ thấy n = nO (oxit) = 0,012mol
=> nH2 ban đầu = 0,012 : 80% = 0,015
=> nFe = nH2= 0,015 → x = 0,015
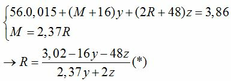
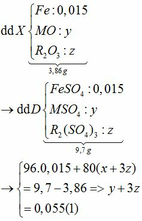
Ta có: CO + O(Oxit) → CO2
Vì: m(Rắn giảm) = mO(Oxit) → nO(Oxit) = (3,86 – 3,46) : 16 = 0,025
TH1: cả 2 oxit đều bị khử bởi CO
→ nO(Oxit) = y + 3z = 0,025 kết hợp với (1) loại
TH2: chỉ có MO bị khử bởi CO
→ nO(Oxit) = nMO = 0,025 → y = 0,025 kết hợp với (1) => z = 0,01
Kết hợp với (*) => M = 64 (Cu)
TH3: chỉ có R2O3 bị khử bởi CO
→ nO(Oxit) = 3.nR2O3 → z = 0,025/3 kết hợp với (1) => y = 0,03
Kết hợp với (*) y => M lẻ => loại
Vậy %m các chất trong X là: 21,76%; 51,81%; 26,43%

a.
BTKL ta có mX = mY => nX . MX = nY . mY
MX / My = nY / mY =0.75
Đặt nX = 1 mol => nY = 0,75 mol => nH2 phản ứng = 1 – 0,75 = 0,25mol
* TH hidrocacbon là anken: n anken = n H2 = 0,25 mol => n H2 trong X = 0,75 => M = (6,75 – 0,75 . 2)/0,25 = 21 (loại) * TH là ankin: => n akin = 0,25/2 = 0,125 => n H2 trong X = 0,875 mol => M = (6,75 – 0,875 . 2)/0,125 = 40 =>C3H4
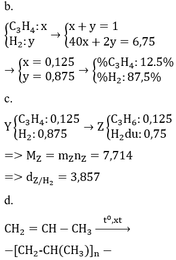


1) muối axit là NaHCO3
CO2 + NaOH → NaHCO3
nCO2 = 4,48/22,4 = 0,2 mol => nNaOH = 0,2 mol ,mNaOH =0,2.40 = 8 gam
C% =\(\dfrac{m_{ct}}{m_{dd}}\).100 => mdd NaOH = \(\dfrac{8.100}{25}\) = 32gam
2) Ag không bị oxi hóa bởi oxi ở nhiệt độ cao,đồng thì có nên hỗn hợp chất rắn A thu được gồm CuO và Ag
2Cu + O2 --> 2CuO
Cho A + HCl dư thì Ag cũng không phản ứng
CuO + HCl --> CuCl2 + H2O
=> Chất rắn B còn lại là Ag
1) muối axit là NaHCO3
CO2 + NaOH → NaHCO3
nCO2 = 4,48/22,4 = 0,2 mol => nNaOH = 0,2 mol ,mNaOH =0,2.40 = 8 gam
C% =mctmddmctmdd.100 => mdd NaOH = 8.100258.10025 = 32gam
2) Ag không bị oxi hóa bởi oxi ở nhiệt độ cao,đồng thì có nên hỗn hợp chất rắn A thu được gồm CuO và Ag
2Cu + O2 --> 2CuO
Cho A + HCl dư thì Ag cũng không phản ứng
CuO + HCl --> CuCl2 + H2O
=> Chất rắn B còn lại là Ag
Câu 1: Cho lần lượt cùng khối lượng các kim loại Al, Mg, Fe, Zn vào các ống nghiệm chứa dung dịch HCl dư. Nhận xét nào sau đây là đúng? ( Các khí thoát ra ở cùng điều kiện).
A. Nhôm tạo ra thể tích khí thoát ra lớn nhất.
B. Mg tạo ra thể tích khí lớn nhất.
C. Zn tạo ra thể tích khí nhỏ nhất.
D. Fe tạo ra thể tích khí nhỏ nhất.
E. Các kim loại cùng tạo ra thể tích khí như nhau.
Câu 2: Dẫn luồng khí H2 dư qua hỗn hợp có CuO, MgO, Al2O3 nung nóng. Sau phản ứng thu được chất rắn có chứa:
A. Một đơn chất và hai hợp chất.
B. Hai đơn chất và một hợp chất.
C. Ba đơn chất.
D. Ba hợp chất.
E. Hai đơn chất và hai hợp chất.
Câu 15: Cho các phản ứng: Na với O2, SO2 với O2; Fe và Cl2; Cu và O2; P và O2. Số các phản ứng tạo ra sản phẩm có khả năng tác dụng với nước là:
A. 2
B. 3
C.4
D.5
E.1
Câu 16: Chất khí A có màu vằng lục, mùi hắc, độc, tuy nhiên với một lượng nhỏ lại được dùng khử trùng nước hoạt. A là:
A. Cl2
B. Br2
C. I2
D. F2
Câu 17: Khi sục khí Cl2 vào dung dịch NaOH thu được:
A. Dung dịch nước clo
B. Dung dịch nước Gia-ven
C. Dung dịch clorua vôi
D. Dung dịch thuốc tím
Câu 18: Than hoạt tính có vai trò quan trọng như làm trắng đường, chế tạo mặt lọ phòng độc,.. nhờ vào tính hấp thụ. Nguyên tố tạo nên than hoạt tính là:
A. F
B. Cl
C. Si
D. S
E. C
Câu 19: Những hoạt động nào của con người không nên làm?
A. Thu gom rác thải để đúng nơi quy định
B. Trồng nhiều cây xanh
C. Để cây xanh trong phòng ngủ vào buổi tối đóng kín cửa.
D. Đun than tổ trong phòng kín
Câu 20: Ở điều kiện thích hợp, khí clo phản ứng được với những chất nào sau đây?
A. O2, NaCl
B. H2, Fe
C. Mg, NaOH
D. Cu, KCl
Mấy câu kia làm sau nhé!
âu 1: Cho lần lượt cùng khối lượng các kim loại Al, Mg, Fe, Zn vào các ống nghiệm chứa dung dịch HCl dư. Nhận xét nào sau đây là đúng? ( Các khí thoát ra ở cùng điều kiện).
A. Nhôm tạo ra thể tích khí thoát ra lớn nhất.
B. Mg tạo ra thể tích khí lớn nhất.
C. Zn tạo ra thể tích khí nhỏ nhất.
D. Fe tạo ra thể tích khí nhỏ nhất.
E. Các kim loại cùng tạo ra thể tích khí như nhau.
Câu 2: Dẫn luồng khí H2 dư qua hỗn hợp có CuO, MgO, Al2O3 nung nóng. Sau phản ứng thu được chất rắn có chứa:
A. Một đơn chất và hai hợp chất.
B. Hai đơn chất và một hợp chất.
C. Ba đơn chất.
D. Ba hợp chất.
E. Hai đơn chất và hai hợp chất.
Câu 3: Cho 15 gam hỗn hợp kim loại Al, Fe, Cu phản ứng với oxi thu được 18,2 gam hỗn hợp X gồm các oxit. Hòa tan hết X bằng dung dịch HCl dư thu được dung dịch Y. Nhận xét đúng về phản ứng trên là:
A. Có 2,24 lít oxi phản ứng ( ở đktc).
B. Có 0,2 mol HCl phản ứng.
C. Có 0,4 mol HCl phản ứng.
D. Có 4,48 lít khí oxi phản ứng ( ở đktc).
E. Dung dịch sản phẩm chỉ có muối.
Câu 4: Dẫn khí H2 dư qua hỗn hợp X có chứa MgO, CuO, FeO, Al2O3 nung nóng thu được chất rắn Y. Cho Y vào dung dịch HCl dư thu được dung dịch Z. Nhận xét nào sau đây là đúng?
A. Y tan hết trong dung dịch HCl.
B. Y có chwuas 2 kim loại
C. Z có chứa 3 chất tan.
D. Y có chứa 3 kim loại
E. Z có chứa 4 chất tan.
Câu 5: Nung nóng m gam magiê với 2,24 lít oxi( ở đktc) thu được chất rắn X. Cho X vào bình chứa dung dịch HCl dư thu được dung dịch Y và thoát ra 3,36 lít khí. Nhận xét nào sau đây là đúng.
A. Có 0,7 mol HCl phản ứng.
B. Khối lượng magiê ban đầu là 8,4 gam.
C. Khối lượng của X là 10 gam
D. Khối lượng magiê ban đầu là 3,6 gam.
E. Khối lượng magiê ban đầu là 4,8 gam.
Câu 6: Một lọ cồn cần được làm khan để chuẩn bị cho thí nghiệm este hóa. Người ta đã thêm từ từ CuSO4 vào lọ chứa đến khi CuSO4 không đổi màu thì dừng lại thấy đã dùng hết 8 gam muối. Biết khi hút nước tạo ra muối CuSO4.5H2O. Nhận xét nào sau đây là đúng?
A. Ban đầu xuất hiện chất rắn màu xanh
B. Trong lọ cồn có chứa 4,5 gam nước.
C. CuSO4 hút nước chuyển sang màu vàng
D. Trong lọ cồn có chứa 0,9 gam nước
E. Trong lọ có chứa 9 gam nước.
Câu 7: Hòa tan hết hỗn hợp X gồm 8,4 gam Fe và 2,4 gam Mg vào dung dịch HCl dư thấy thoát ra V lít khí ( ở đktc). Giá trị của V là:
A. 3,36
B. 2,24
C. 5,6
D. 7,28
Câu 8: Cho 4,8 gam Mg vào cốc chauws dung dịch HCl 2M và H2SO4 1M thấy tan hết và thoát ra khí hiđrô. Thể tích khí thoát ra ở đktc là:
A. 4,48 lít.
B. 2,24 lít
C. 8,96 lít
D. 6,72 lít
Câu 9: Nung nóng 6 gam bột nhôm với khí oxi thu được 10,8 gam chất rắn. Nhận xét nào sau đây là đúng?
A. Chất rắn thu được có chứa 5,4 gam Al.
B. Khối lượng nhôm phản ứng là 6 gam
C. Thể tích oxi phản ứng là 3,36 lít ( ở đktc)
D. Thể tích oxi phản ứng là 6,72 lít.
Câu 10: Một bình điện phân nước sau khi điện phân thấy khối lượng nước gaimr 3,6 gam so với ban đầu. Tổng thể tích khí thoát ra ở đktc từu cả hai điện cực là:
A. 6,72 lít
B. 3,36 lít
C. 10,08 lít
D. 13,44 lít
Câu 11: Hấp thụ hết V lít khí SO3 ( ở đktc) vào cốc thủy tinh có chứa m gam nwuosc thấy thu được 100 gam dung dịch axit có nồng độ 19,6%. Nhận xét nào sau đây là đúng?
A. Giá trị của V là 4,48; giá trị của m là 80,4
B. Giá trị của V là 2,24; giá trị của m là 84
C. Giá trị của V là 4,48; giá trị của m là 84
D. Giá trị của V là 2,24; giá trị của m là 80,4
Câu 12: Trong một phòng thí nghiệm dẫn 3,36 lít khí H2(đktc) qua ống nghiệm chứa 10 gam bột CuO nung nóng thu được 6,4 gam đồng. Nhận xét nào sau đây không đúng?
A. Hiệu suất phản ứng của thí nghiệm là 66,67%
B. Hiệu suất phản ứng của thí nghiệm là 80%
C. Khối lượng chất rắn sau phản ứng là 8,4 gam
D. Thí nghiệm tạo ra 1,8 gam hơi nước.
Câu 13: Đốt cháy hoàn toàn hỗn hượp Al, Mg, Fe bằng một lượng oxi thu được 20 gam chất rắn X, hòa tan hết X cần vừa đủ 600 ml dung dịch H2SO4 nồng độ 1M. Khối lượng hỗn hợp kim loại ban đầu là:
A. 10,4 gam
B. 9,6 gam
C. 58,8 gam
D. 29,6 gam
Câu 14: Hòa tan hết mẩu natri nặng 4,6 gam vào cốc thủy tinh chứa 50gam nước. Khối lượng dung dịch thu được sau phản ứng là:
A. 54,6 gam
B. 54,4 gam
C. 8 gam
D. 58 gam
E. 54,2 gam
Câu 15: Cho các phản ứng: Na với O2, SO2 với O2; Fe và Cl2; Cu và O2; P và O2. Số các phản ứng tạo ra sản phẩm có khả năng tác dụng với nước là:
A. 2
B. 3
C.4
D.5
E.1
Câu 16: Chất khí A có màu vằng lục, mùi hắc, độc, tuy nhiên với một lượng nhỏ lại được dùng khử trùng nước hoạt. A là:
A. Cl2
B. Br2
C. I2
D. F2
Câu 17: Khi sục khí Cl2 vào dung dịch NaOH thu được:
A. Dung dịch nước clo
B. Dung dịch nước Gia-ven
C. Dung dịch clorua vôi
D. Dung dịch thuốc tím
Câu 18: Than hoạt tính có vai trò quan trọng như làm trắng đường, chế tạo mặt lọ phòng độc,.. nhờ vào tính hấp thụ. Nguyên tố tạo nên than hoạt tính là:
A. F
B. Cl
C. Si
D. S
E. C
Câu 19: Những hoạt động nào của con người không nên làm?
A. Thu gom rác thải để đúng nơi quy định
B. Trồng nhiều cây xanh
C. Để cây xanh trong phòng ngủ vào buổi tối đóng kín cửa.
D. Đun than tổ trong phòng kín
Câu 20: Ở điều kiện thích hợp, khí clo phản ứng được với những chất nào sau đây?
A. O2, NaCl
B. H2, Fe
C. Mg, NaOH
D. Cu, KCl