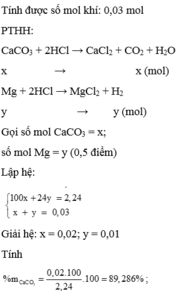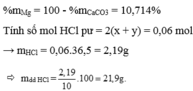Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a, PT: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
Ta có: \(n_{H_2}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\)
Theo PT: \(n_{Mg}=n_{H_2}=0,03\left(mol\right)\)
\(\Rightarrow m_{Mg}=0,03.24=0,72\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Mg}=\dfrac{0,72}{1,74}.100\%\approx41,38\%\\\%m_{AlCl_3}\approx58,62\%\end{matrix}\right.\)
b, Theo PT: \(n_{HCl}=2n_{H_2}=0,06\left(mol\right)\)
\(\Rightarrow m_{HCl}=0,06.36,5=2,19\left(g\right)\)
\(\Rightarrow C\%_{ddHCl}=\dfrac{2,19}{500}.100\%=0,438\%\)
Bạn tham khảo nhé!
a, nH2 = 0,03 ( mol )
=> nMg = nH2 = 0,03 ( mol )
=> mMg = 0,72 g
=> %Mg \(\approx\) 41,38 % .
=> % Al \(\approx\) 58,62 % .
b, Có : nH2 = 0,03 mol
=> nHCl = nHCltừ Al2O3 + nHCltừ Mg = 0,06 + 0,06 = 0,12 ( mol )
=> mHCl = 4,38 ( g )
Lại có : mdd = mhh + mddHCl = 501,74 ( g )
=> \(C\%=\dfrac{m_{HCl}}{m_{dd}}.100\%\approx0,87\%\)
( chắc đoạn trên là Al2O3 :vvvv )

\(a) n_{Fe_2O_3} = \dfrac{8}{160} = 0,05(mol)\\ Fe_2O_3 + 6HCl \to 2FeCl_3 + 3H_2O\\ n_{FeCl_3} = 2n_{Fe_2O_3} = 0,1(mol)\\ m_{FeCl_3} = 0,1.162,5 = 16,25(gam)\\ b) n_{HCl} = 6n_{Fe_2O_3} = 0,05.6 = 0,3(mol)\\ V_{dd\ HCl} = \dfrac{0,3}{0,5} = 0,6(lít)\\ c) C_{M_{FeCl_3}} = \dfrac{0,1}{0,5} = 0,2M\)

nH2=6,72/22,4=0,3 mol
Mg + 2HCl \(\rightarrow\) MgCl + H2
a a mol
Fe + 2HCl \(\rightarrow\) FeCl2 +H2
b b mol
ta có 24a + 56b =13,6
và a + b=0,3
=>a=0,1 mol , b=0,2 mol
=>mMg=0,2*24=2,4 g
=>%Mg=2,48100/13,6=17,65%
=>%Fe=100-17,65=82,35%
nMgCl2=nMg=0,1mol=>mMgCl2=0,1*95=9,5 g
nFeCl2=nFe=0,2 mol=>mFeCl2 = 0,2*127=25,4 g
nHCl=nMg+nFe=0,1+0,2=0,3mol
=>CMHCl=0,3/0,4=0,75M

\(Đặt:nMg=a\left(mol\right),n_{MgCO_3}=b\left(mol\right)\)
\(n_{khí}=\dfrac{6.72}{22.4}=0.3\left(mol\right)\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(a................a.......a\)
\(MgCO_3+2HCl\rightarrow MgCl_2+CO_2+H_2O\)
\(b....................b........b\)
\(m_X=24a+84b=13.2\left(g\right)\left(1\right)\)
\(n_{khí}=a+b=0.3\left(mol\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.2,b=0.1\)
\(m_{Mg}=0.2\cdot24=4.8\left(g\right),m_{MgCO_3}=0.1\cdot84=8.4\left(g\right)\)
\(m_{ddB}=13.2+200-0.2\cdot2-0.1\cdot44=208.4\left(g\right)\)
\(m_{MgCl_2}=0.3\cdot95=28.5\left(g\right)\)
\(C\%MgCl_2=\dfrac{28.5}{208.4}\cdot100\%=13.67\%\)

\(n_{SO_2}=\dfrac{12,32}{22,4}=0,55mol\)
\(2Fe+6H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+6H_2O+3SO_2\uparrow\)
x 3x 0,5x 3x 1,5x
\(2Ag+2H_2SO_4\rightarrow2H_2O+SO_2\uparrow+Ag_2SO_4\)
y y y 0,5y 0,5y
\(\Rightarrow\left\{{}\begin{matrix}1,5x+0,5y=0,55\\56x+108y=38,4\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,3\\y=0,2\end{matrix}\right.\)
a)\(\%m_{Fe}=\dfrac{0,3\cdot56}{38,4}\cdot100\%=43,75\%\)
\(\%m_{Ag}=100\%-43,75\%=56,25\%\)
b)\(m_{muối}=m_{Fe_2\left(SO_4\right)_3}+m_{Ag_2SO_4}\)
\(\Rightarrow muối=0,5\cdot0,3\cdot400+0,5\cdot0,2\cdot312=91,2g\)
c)Cho hỗn hợp trên tác dụng \(H_2SO_4\) loãng chỉ có Fe tác dụng.
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
0,3 0,3 0,3
\(C_{M_{H_2SO_4}}=\dfrac{0,3}{0,2}=1,5M\)
\(V_{H_2}=0,3\cdot22,4=6,72l\)