Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(a,n_{H_2}=\dfrac{2,576}{22,4}=0,115\left(mol\right)\\ Đặt:n_{Mg}=a\left(mol\right);n_{Al}=b\left(mol\right)\left(a,b>0\right)\\ Mg+2HCl\rightarrow MgCl_2+H_2\\ 2Al+6HCl\rightarrow2AlCl_3+3H_2\\ \Rightarrow\left\{{}\begin{matrix}95a+133,5b=10,475\\a+1,5b=0,115\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,04\\b=0,05\end{matrix}\right.\\ \%m_{Mg}=\dfrac{0,04.24}{0,04.24+0,05.27}.100\approx41,558\%\Rightarrow\%m_{Al}\approx58,442\%\\ b,n_{HCl}=2.n_{H_2}=2.0,115=0,23\left(mol\right)\\ \Rightarrow x=C\%_{ddHCl}=\dfrac{0,23.36,5}{100}.100=8,395\%\)

\(2Al+6HCl->2AlCl_3+3H_2\\ Fe+2HCl->FeCl_2+H_2\\ n_{Al}=a;n_{Fe}=b\\ 27a+56b=8,3\\ 1,5a+b=\dfrac{5,6}{22,4}=0,25\\ a=b=0,1\\ m_{Al}=27\cdot0,1=2,7g\\ m_{Fe}=8,3-2,7=5,6g\\ a=\dfrac{3a+2b}{500}\cdot36,5=3,65\%\\ m_{ddsau}=508,3-0,25\cdot2=507,8g\\ C\%_{AlCl_3}=\dfrac{133,5a}{507,8}=2,63\%\\ C\%_{FeCl_2}=\dfrac{127b}{507,8}=2,50\%\)

\(19,1gam\) \(:\left\{{}\begin{matrix}Al\\Mg\\Zn\end{matrix}\right.\)\(\underrightarrow{+O_2}\)\(Y:25,5gam\)\(\underrightarrow{+HCl}\left\{{}\begin{matrix}AgCl_3\\MgCl_2\\ZnCl_2\end{matrix}\right.\) + H2 : 0,3 mol
H2O
Áp dụng định luật bảo toàn khối lượng:
\(mO_2=25,5-19,1=6,4gam\) \(\Rightarrow nO_2=0,2\left(mol\right)\)
BTNT O : nH2O = 0,4mol
\(\rightarrow nHCl^-\left(tdOxi\right)=0,8\left(mol\right)\)
\(nH_2=0,3\left(mol\right)\rightarrow nCl^-\left(tdKl\right)=0,6\left(mol\right)\)
\(m_{muối}=19,1+\left(0,8+0,6\right).35,5=68,8\left(g\right)\)

Đáp án A
Tương tự Câu 12, áp dụng định luật bảo toàn mol electron ta có
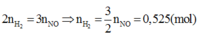
Vậy V= 11,76 (lít)

Đáp án A
Tương tự câu 12, áp dụng định luật bảo toàn mol electron ta có:
2 n H 2 = 3 n N O = > 3 2 n N O = 0 , 525 ( m o l )
Vậy V = 11,76 (lít)

Đáp án B
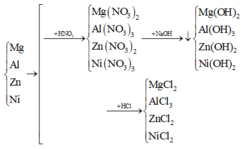
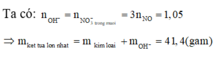
Khối lượng hỗn hợp mỗi phần là 23,55 gam.
Vì để thu được khối lượng kết tủa là lớn nhất nên không có sự hòa tan kết tủa bởi NaOH dư.

Đáp án B

Khối lượng hỗn hợp mỗi phần là 23,55 gam.
Vì để thu được khối lượng kết tủa là lớn nhất nên không có sự hòa tan kết tủa bởi NaOH dư.
Ta có:
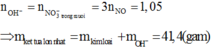



Bài 2:
Cu +HCl không pư
Mg +2HCl → MgCl2 + H2
x x x
2Al +6 HCl →2AlCl3 +3 H2
y y 3/2y
Vì Cu không pư ⇒mCu=2,54 (g)⇒mMg,Al=6,6 (g)
nH2= 0,32 (mol)
Đặt x=nMg , y=nAl
Theo PTHH ta có:
24x + 27y =6,6
x + 3/2y =0,32
⇔ x=0,14
y=0,12
mMgCl2=13,3 (g)
mAlCl3=12,78 (g)
⇒m=13,3 + 12,78 =26,08 (g)
Bài 3:mcrăn = mKLmKL + mOmO
2 H + O -> H2OH2O
mol 0.8 0.4
mcrắn = 40 + 0,4 .16 = 46,4 gam
Bài 4:
Fe+H2SO4=FeSO4+H2
nH2=1,792/22,4=0,08mol
=>nFe=0,08mol
Khi cho 0,08mol Fe td với HNO3:
Quá trình nhường e: Fe=Fe+3 +3e
=> n e nhường=0,24mol
Theo ĐLBTe, ta có n e cho=n e nhận.
Quá trình nhận e: N+5 +3e=>N+2
=> nN+2=0,24/3=0,08mol
=>nNO=0,08mol =>V NO=0,08.22,4=1,792l
Bổ sung câu 1 : Cách 2
Ta có:
\(n_{H2}=\frac{8,52}{22,4}=0,38\left(mol\right)\)
\(2n_{Mg}+27n_{Al}=7,68\left(1\right)\)
Bảo toàn e:
\(2n_{Mg}+3n_{Al}=2n_{H2}=0,76\left(2\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{Mg}=0,14\left(mol\right)\\n_{Al}=0,16\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\%m_{Al}=\frac{0,16.27}{7,68}.100\%=56,25\%\)