
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(a.C_3H_8+5O_2\underrightarrow{^{to}}3CO_2+4H_2O\)
Đó anh viết PT cho em , em tự tính nha, đề không cho số liệu mà.


A: Fe
B: Fe2(SO4)3
C : Fe(OH)3
D: Fe2O3
X: H2SO4 đặc nóng
Y: NaOH
Z : CO
PTHH:
2Fe + 6H2SO4 → Fe2(SO4)3 + 3SO2 + 6H2O
Fe2(SO4)3 + 6NaOH → 2Fe(OH)3 + 3Na2SO4
2Fe(OH)3 ------to-------> Fe2O3 + 3H2O
Fe2O3 + 3CO --------> 2Fe + 3CO2

a) K không tác dụng với NaOH nhưng tác dụng với nước trong dd NaOH.
2K + 2 H2O -> 2 KOH + H2
b) Ca tác dụng nước trong dung dịch Na2CO3, sau đó tạo dd Ca(OH)2 tạo kết tủa với Na2CO3 ra CaCO3.
Ca + 2 H2O -> Ca(OH)2 + H2
Ca(OH)2 + Na2CO3 -> CaCO3 + 2 NaOH
c) Ba + 2 H2O -> Ba(OH)2 + H2
Ba(OH)2 + NaHSO4 -> BaSO4 + NaOH + H2O
d) Na + H2O -> NaOH + 1/2 H2
3 NaOH + AlCl3 -> 3 NaCl + Al(OH)3
e) Ba + 2 H2O -> Ba(OH)2 + H2
Ba(OH)2 + 2 NH4NO3 -> Ba(NO3)2 + 2 NH3 + 2 H2O
f) Na + H2O -> NaOH + 1/2 H2
NaOH + Al + H2O -> NaAlO2 + 3/2 H2
a) K không tác dụng với NaOH nhưng tác dụng với nước trong dd NaOH.
2K + 2 H2O -> 2 KOH + H2
b) Ca tác dụng nước trong dung dịch Na2CO3, sau đó tạo dd Ca(OH)2 tạo kết tủa với Na2CO3 ra CaCO3.
Ca + 2 H2O -> Ca(OH)2 + H2
Ca(OH)2 + Na2CO3 -> CaCO3 + 2 NaOH
c) Ba + 2 H2O -> Ba(OH)2 + H2
Ba(OH)2 + NaHSO4 -> BaSO4 + NaOH + H2O
d) Na + H2O -> NaOH + 1/2 H2
3 NaOH + AlCl3 -> 3 NaCl + Al(OH)3
e) Ba + 2 H2O -> Ba(OH)2 + H2
Ba(OH)2 + 2 NH4NO3 -> Ba(NO3)2 + 2 NH3 + 2 H2O
f) Na + H2O -> NaOH + 1/2 H2
NaOH + Al + H2O -> NaAlO2 + 3/2 H2

Ta có: \(\left\{{}\begin{matrix}n_{Fe_2O_3}=\dfrac{40\cdot60\%}{160}=0,15\left(mol\right)\\n_{CuO}=\dfrac{40\cdot40\%}{80}=0,2\left(mol\right)\end{matrix}\right.\)
PTHH: \(Fe_2O_3+3H_2\xrightarrow[]{t^o}2Fe+3H_2O\)
0,15____0,45___0,3____0,45 (mol)
\(CuO+H_2\xrightarrow[]{t^o}Cu+H_2O\)
0,2___0,2___0,2___0,2 (mol)
Ta có: \(\left\{{}\begin{matrix}m_{Fe}=0,3\cdot56=16,8\left(g\right)\\m_{Cu}=0,2\cdot64=12,8\left(g\right)\\V_{H_2}=\left(0,2+0,45\right)\cdot22,4=14,56\left(l\right)\end{matrix}\right.\)

Bài 1:
\(a,m_{NaOH}=0,2.40=8(g)\\ b,m_{H_2O}=1,5.18=27(g)\)
Bài 2:
\(a,V_{O_2}=0,3.22,4=6,72(l)\\ b,V_{Cl_2}=2.22,4=44,8(l)\)
Bài 3:
\(a,n_{Cu}=\dfrac{6,4}{64}=0,1(mol)\\ b,n_{H_2}=\dfrac{4,48}{22,4}=0,2(mol)\)

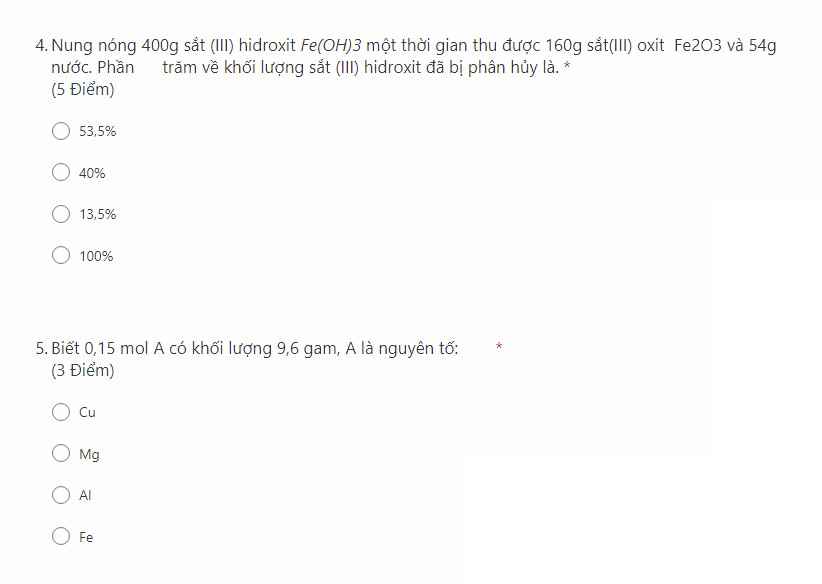
\(4,2Fe(OH)_3\xrightarrow{t^o}Fe_2O_3+3H_2O\\ \Rightarrow m_{Fe(OH)_3}=m_{Fe_2O_3}+m_{H_2O}=214(g)\\ \Rightarrow \%_{phân hủy}=\dfrac{214}{400}.100\%=53,5\%\\ \Rightarrow A\\ 5,M_A=\dfrac{9,6}{0,15}=64(g/mol)\\ \Rightarrow A:Cu\\ \Rightarrow A\)

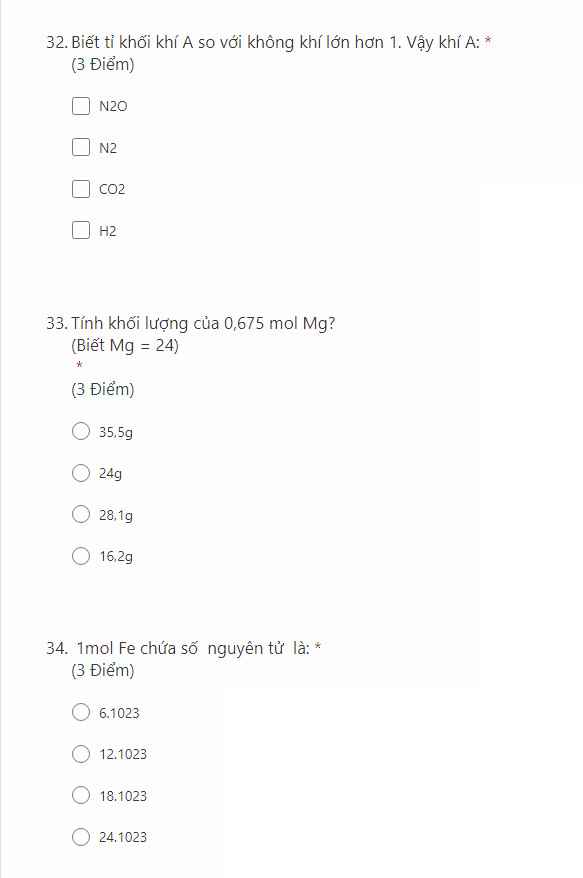
32: A, C
\(n_{N_2O/kk}=\dfrac{44}{29}=1,517>1\)
\(m_{CO_2/kk}=\dfrac{44}{29}=1,517>1\)
33: D
\(m_{Mg}=0,675.24=16,2\left(g\right)\)
34: A

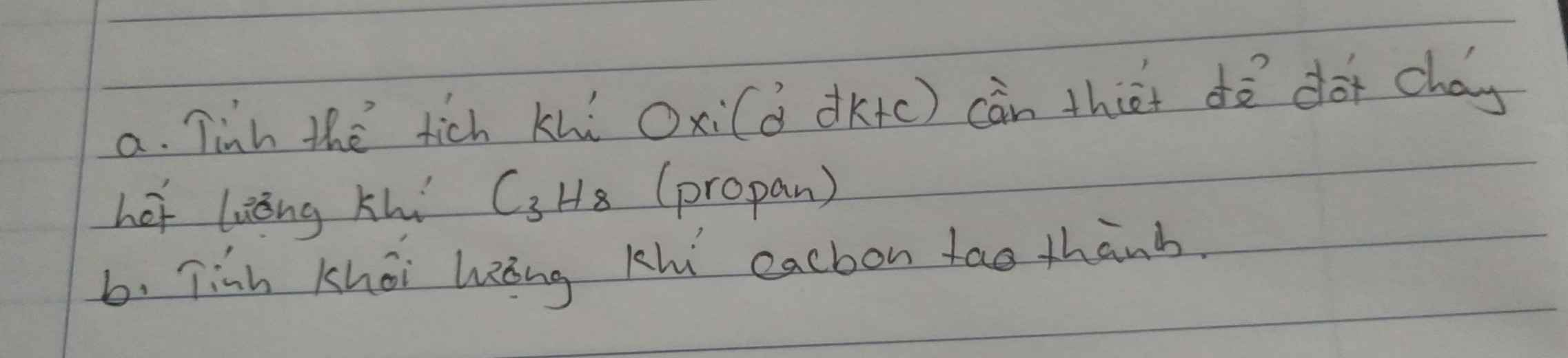
 A-Ai cứu mình với...bài nhiều quá...mình không làm nổi...Mấy bạn giúp mình với...
A-Ai cứu mình với...bài nhiều quá...mình không làm nổi...Mấy bạn giúp mình với...





\(a,PTHH:4Al+3O_2\underrightarrow{t^o}2Al_2O_3\\ b,n_{Al}=\dfrac{2,7}{27}=0,1\left(mol\right)\\ Theo.pt:n_{Al_2O_3}=\dfrac{1}{2}n_{Al}=\dfrac{1}{2}.0,1=0,05\left(mol\right)\\ m_{Al_2O_3}=0,05.102=5,1\left(g\right)\\ c,THeo.pt:n_{O_2}=\dfrac{3}{4}n_{Al}=\dfrac{3}{4}.0,1=0,075\left(mol\right)\\ V_{kk}=0,075.22,4.5=8,4\left(l\right)\)