Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Phương pháp hóa học :
+ Cho chất rắn vào dung dịch axit HCl, H2SO4 loãng dư
+ Chất rắn sau phản ứng là Cu do Cu không phản ứng với HCl, H2SO4 loãng
=> Cân, tìm được khối lượng Cu
=> Tính được % khối lượng Cu
=> 100 - % khối lượng Cu = % khối lượng Fe
Phương pháp vật lí :
+ Dùng nam chất hút sắt ra khỏi hỗn hợp
+ Cân, tìm được khối lượng Fe
=> Tính được % khối lượng Fe
=> 100 - % khối lượng Fe = % khối lượng Cu
PP HH):Cho hỗn hợp bột kim loại tác dụng với HCl dư (hoặc H2SO4 loãng dư), thì chỉ có bột sắt Fe tác dụng theo phương trình: Fe + 2HCl ----> FeCl2 + H2.
Còn bột đồng Cu sẽ kết tủa dưới đáy ống nghiệm. Gạn lấy kết tủa, ta được Cu. Cân bột đồng Cu, tính toán phần trăm khối lượng của Cu, suy ra phần trăm khối lượng của Fe.
PPVL) Cho nam châm lại gần hỗn hợp bột kim loại, chỉ có bột sắt Fe bị nam châm hút ra khỏi hỗn hợp. Phần bột kim loại không bị nam châm hút chính là bột đồng Cu. Cân lấy Cu, tính toán phần trăm khối lượng của Cu, suy ra phần trăm khối lượng của Fe.

Cho năm châm qua hỗn hợp kim loại, bột kim loại Iron bị năm châm hút còn lại bột kim loại Copper.
Cân bột Iron lên rồi lấy khối lượng bột Iron chia cho khối lượng hỗn hợp kim loại rồi nhân cho 100% ta được phầm trăm theo khối lượng của Iron trong hỗn hợp ban đầu.
Lấy 100% trừ cho phầm trăm theo khối lượng của Iron trong hỗn hợp ban đầu ta thu được phầm trăm theo khối lượng của Copper trong hỗn hợp ban đầu.

a) Cho hỗn hợp bột kim loại tác dụng với HCl dư (hoặc H2SO4 loãng dư), thì chỉ có bột sắt Fe tác dụng theo phương trình: Fe + 2HCl ----> FeCl2 + H2.
bẹn tham khảo

\(a) \\ Fe + H_2SO_4 \to FeSO_4 + H_2\\ Fe_2O_3 + 3H_2SO_4 \to Fe_2(SO_4)_3 + 3H_2O\\ b) \text{Theo PTHH} : \\ n_{Fe} = n_{H_2} = \dfrac{2,24}{22,4} = 0,1(mol)\\ \%m_{Fe} = \dfrac{0,1.56}{8} .100\% = 70\%\\ \%m_{Fe_2O_3} = 100\% -70\% = 30\%\)
\(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ PTHH:Fe+H_2SO_4\rightarrow FeSO_4+H_2\\ \left(mol\right).....0,1...........................\leftarrow0,1\\ m_{Fe}=0,1.56=5,6\left(g\right)\\ m_{Fe_2O_3}=\Sigma m_{hh}-m_{Fe}=8-5,6=2,4\left(g\right)\\ PTHH:Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\\ \left\{{}\begin{matrix}\%m_{Fe}=\dfrac{5,6}{8}.100\%=70\%\\\%m_{Fe_2O_3}=\dfrac{2,4}{8}.100\%=30\%\end{matrix}\right.\)

1)
Gọi số mol KMnO4, KClO3 là a, b (mol)
=> 158a + 122,5b = 308,2 (1)
PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
a-------------------------------->0,5a
2KClO3 --to--> 2KCl + 3O2
b------------------>1,5b
=> mO2 = (0,5a + 1,5b).32 = 16a + 48b (g)
mD = 308,2 - 16a - 48b(g)
\(m_{Mn}=\dfrac{\left(308,2-16a-48b\right).10,69}{100}=32,94658-1,7104a-5,1312b\left(g\right)\)
=> \(n_{Mn}=\dfrac{32,94658-1,7104a-5,1312b}{55}=0,6-\dfrac{1069}{34375}a-\dfrac{3207}{34375}\left(mol\right)\)
Mà \(n_{Mn}=n_{KMnO_4}=a\left(mol\right)\)
=> \(\dfrac{35444}{34375}a+\dfrac{3207}{34375}b=0,6\) (2)
(1)(2) => a = 0,4 (mol); b = 2 (mol)
=> \(\left\{{}\begin{matrix}\%m_{KMnO_4}=\dfrac{0,4.158}{308,2}.100\%=20,506\%\\\%m_{KClO_3}=\dfrac{2.122,5}{308,2}.100\%=79,494\%\end{matrix}\right.\)
2)
Giả sử nung 100 (g) đá vôi
=> \(m_{CaCO_3\left(bđ\right)}=\dfrac{80.100}{100}=80\left(g\right)\)
\(m_{rắn.sau.pư}=\dfrac{100.73,6}{100}=73,6\left(g\right)\)
=> mCO2 = 100 - 73,6 = 26,4 (g)
\(n_{CO_2}=\dfrac{26,4}{44}=0,6\left(mol\right)\)
PTHH: CaCO3 --to--> CaO + CO2
0,6<----------------0,6
=> mCaCO3(pư) = 0,6.100 = 60 (g)
\(H\%=\dfrac{60}{80}.100\%=75\%\)

Đặt x và y là số mol O 3 và O 2 có trong 1 mol hỗn hợp khí
Hỗn hợp khí A : (48x + 32y)/(x+y) = 19,2 x 2 = 38,4
→ 3x = 2y → 40% O 3 và 60% O 2
Đặt x và y là số mol H 2 và CO có trong 1 mol hỗn hợp khí
Hỗn hợp khí B : (2x + 28y)/(x+y) = 3,6 x 2 = 7,2
→ x = 4y → 80% H 2 và 20% CO

Nung cả hỗn hợp với $Cl_2$ rồi hòa vào nước lọc chất rắn là ta sẽ đưa bài toán trên về 2 bài toàn nhỏ:
Bài toán 1: Tách Al; Fe; Cu ra khỏi hỗn hợp dung dịch $AlCl_3;CuCl_2;FeCl_3$
Bài toán 2: Tách $Al_2O_3;Fe_2O_3;CuO$ ra khỏi hỗn hợp
Đưa về 2 bài này là nó lại ez rồi nhỉ :3
P/s: Thuc ra minh luoi lam vl nen thoi minh chỉ ra hướng vậy thoi he :3

a)
Dựa vào màu sắc:
+ NO: Chất khí không màu
+ NO2: Chất khí màu nâu
b)
Gọi số mol NO2, O2 là a, b (mol)
\(M=\dfrac{46a+32b}{a+b}=17,75.2=35,5\left(g/mol\right)\)
=> 10,5a = 3,5b
=> 3a = b
\(\left\{{}\begin{matrix}\%V_{NO_2}=\dfrac{a}{a+b}.100\%=\dfrac{a}{a+3a}.100\%=25\%\\\%V_{O_2}=100\%-25\%=75\%\end{matrix}\right.\)

Thành phần theo khối lượng:
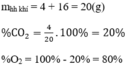
Thành phần phần trăm theo thể tích:


a.Cân khối lượng hỗn hợp X
Dùng nam châm hút sắt ra khỏi hỗn hợp
Cân sắt, sau đó tính \(\%m_{Fe}=\dfrac{m_{Fe}}{m_X}.100\)
Còn lại \(\%m_{Na_2O}=100-\%m_{Fe}\)
b. Cân khối lượng hỗn hợp X
Cho hỗn hợp X vào nước dư
Na2O tan hết trong nước, Fe không tan
Lọc lấy Fe, cân thu được khối lượng Fe. Sau đó tính \(\%m_{Fe}=\dfrac{m_{Fe}}{m_X}.100\)
Còn lại \(\%m_{Na_2O}=100-\%m_{Fe}\)