Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Phương trình hóa học của phản ứng:
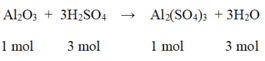
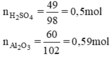
So sánh tỉ lệ 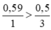 → Vậy Al2O3 dư
→ Vậy Al2O3 dư
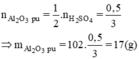
mAl2O3 (dư) = 60 - 17 = 43(g)

Phương trình phản ứng hóa học:
Al2O3 + 3H2SO4 → Al2(SO4) + 3H2O
102 g 3. 98 = 294 g
Theo phương trình phản ứng ta thấy, khối lượng axit sunfuric nguyên chất tiêu thụ lớn gấp hơn hai lần khối lượng oxit. Vì vậy, 49 gam H2SO4 nguyên chất sẽ tác dụng với lượng nhôm (III) oxi nhỏ hơn 60gam
Vật chất Al2O3 sẽ còn dư và axit sunfuric phản ứng hết.
102 g Al2O3 → 294 g H2SO4
X g Al2O3 → 49g H2SO4
Lượng chất Al2O3 còn dư là: 60 – x = 60 - = 43 g
Trần Thu Hà copy từ trang hoc khác đó cô @Cẩm Vân Nguyễn Thị

PTHH:Al2O3+3H2SO4\(\underrightarrow{ }\)Al2(SO4)3+3H2O
Theo PTHH:294 gam H2SO4 cần 102 gam Al2O3
Vậy:49 gam H2SO4 cần 17 gam Al2O3
Sau phản ứng, Al2O3 thừa:60-17=43(gam)

a) Pt : Al2O3 + 3H2SO4 → Al2(SO4)3 + 3H2O
1 3 1 3
0,03 0,1 0,03
b) Số mol của axit sunfuric
nH2SO4 = \(\dfrac{m_{H2SO4}}{M_{H2SO4}}=\dfrac{9,8}{98}=0,1\left(mol\right)\)
Số mol của nhôm sunfat
nAl2(SO4)3 = \(\dfrac{0,1.1}{3}=0,03\left(mol\right)\)
Khối lượng của nhôm sunfat
mAl2(SO4)3 = nAl2(SO4)3 . MAl2(SO4)3
= 0,03 . 342
= 10,26 (g)
c) Số mol của nhôm oxit
nAl2O3 = \(\dfrac{0,1.1}{3}=0,03\left(mol\right)\)
Khối lượng của nhôm oxit
mAl2O3 = nAl2O3 . MAl2O3
= 0,03 . 102
= 3,06 (g)
Chúc bạn học tốt

Khối lượng của kim loại có trong oxit kim loại:
MKL = 112 g
Khối lượng nguyên tố oxi: mO = 160 – 112 = 48g
Đặt công thức hóa học của oxit kim loại là MxOy, ta có:
MKL. x = 112 => nếu x = 2 thì M = 56. Vậy M là Fe
16y = 48 => y = 3
Vậy CTHH: Fe2O3, đó là sắt (III) oxit
Gọi Công thức hóa học của oxit đó là : MxOy
Ta có : khối lượng của M trong 1 mol là : 160 . 70 : 100 = 112(g)
=> khối lượng của Oxi trong 1 mol là : 160 - 112 = 48(g)
=> số nguyên tử Oxi có trong 1 phân tử Oxit là : 48 : 16 = 3 (nguyên tử)
=>y = 3 => M có hóa trị là III
Ta có : III . x = 3 . II
=> x = 2
=> MxOy = M2O3
=> Mkim loại M là 112 : 2 = 56 (g/mol)
=> M = Fe
Vậy tên Oxit đó là : Fe2O3

Đặt công thức của oxit kim loại là MxOy
%mO = 100% - 70% = 30%
⇒ mO = 12y = 160.30% = 48
⇒ y = 3
mM = 160.70% = 112g = M.x (với M là phân tử khối của kim loại M)
Áp dụng quy tắc hóa trị ta có:
a.x = 2.3 = 6 (với a là hóa trị của M; a = 1; 2; 3)
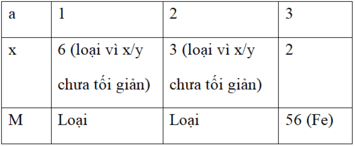
⇒ M là kim loại Sắt.
Vậy công thức hóa học của oxit kim loại là Fe2O3 (Sắt (III) oxit).

TL
1/ nAl = 5,4 : 27 = 0,2(mol)
4Al + 3O2 ---> 2Al2O3
0,2 ----> 0,1 (mol)
=> mAl2O3 = 0,1 x ( 27 x 2 + 16 x 3 ) = 0,2 x 102 = 20.4 (g)
2/ nAl2O3 = 30,6 : 102 = 0,3 (mol)
4Al + 3O2 ---> 2Al2O3
0,6 <---- 0,3 (mol)
=> mAl = 0,6 x 27 = 16,2 (g)
3/ B1 : Viết phương trình
B2 : Tính số mol các chất
B3 : Dựa vào phương trình hóa học tính được số mol chất cần tìm
B4 : Tính khối lượng.
Áp dụng: 1. C
2. B
3. B
Khi nào rảnh vào kênh H-EDITOR xem vid nha!!! Thanks!
Bài 1:
Gọi CTHH của oxit là \(A_xO_y\) ( x,y là những số nguyên dương đơn giản )
Vì \(M_{A_xO_y}=160\left(g/mol\right)\)
\(\Rightarrow x.M_A+16y=160\left(g/mol\right)\)
\(\%m_A=70\%\Rightarrow\dfrac{x.M_A}{160}.100\%=70\%\)
\(\Rightarrow x.M_A=112\)
Ta có bảng thử các giá trị của x:
⇒ x = 2 ; MA = 56 ⇒ Kim loại là Fe
\(y=\dfrac{160-112}{16}=3\)
Vậy CTHH : \(Fe_2O_3\)
Bài 2:
\(n_{H_2SO_4}=\dfrac{49}{98}=0,5\left(mol\right)\)
\(n_{Al_2O_3}=\dfrac{60}{102}=0,59\left(mol\right)\)
PTHH: Al2O3 + 3H2SO4 → Al2(SO4)3 + 3H2O
Tỉ lệ : \(\dfrac{0,59}{1}>\dfrac{0,5}{3}\)
→ Nhôm oxit dư, tính theo H2SO4
Theo PTHH : \(n_{Al_2O_3}=\dfrac{1}{3}.n_{H_2SO_4}=\dfrac{1}{3}.0,5=\dfrac{1}{6}\left(mol\right)\)
\(\Rightarrow m_{Al_2O_3p/ư}=\dfrac{1}{6}.102=17\left(g\right)\)
\(\Rightarrow m_{Al_2O_3dư}=60-17=43\left(g\right)\)
Theo PTHH: \(n_{Al_2\left(SO_4\right)_3}=\dfrac{1}{3}.n_{H_2SO_4}=\dfrac{1}{3}.0,5=\dfrac{1}{6}\left(mol\right)\)
\(\Rightarrow m_{AL_2\left(SO_4\right)_3}=\dfrac{1}{6}.342=57\left(g\right)\)