Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Các phương trình phản ứng :
M tác dụng với O2: 4 M + 2 n O 2 → t 0 2 M n O n
Chất rắn sau phản ứng tác dụng với dung dịch HCl thu được khí H2, chứng tỏ chất rắn sau có M dư nên O2 hết - chất rắn sau gồm M dư và M2On :
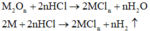
Tính toán:
Số mol H2 thu được là: n H 2 = 13 , 44 22 , 4 = 0 , 6 m o l
Sơ đồ phản ứng:
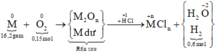
Các quá trình nhường, nhận electron cho cả quá trình:
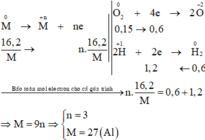

Ta có: \(n_{SO_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
\(n_S=\dfrac{4,8}{32}=0,15\left(mol\right)\)
Coi hh chất rắn gồm M và O.
⇒ nO = 0,15.2 = 0,3 (mol)
Ta có: \(n_M=\dfrac{16,2}{M_M}\left(mol\right)\)
BT e, có: n.nM = 2nO + 2nSO2 + 6nS
\(\Rightarrow\dfrac{16,2n}{M_M}=1,8\Rightarrow M_M=9n\left(g/mol\right)\)
Với n = 3 thì MM = 27 (g/mol) là thỏa mãn.
Vậy: M là Al.

Đáp án C.
Kim loại không phản ứng với H2SO4 loãng là Cu.
Gọi nCu = x, nMg = y, nAl = z
Ta có:
64x + 24y + 27z = 33,2 (1)
Bảo toàn e:
2nMg + 3nAl = 2nH2
=> 2y + 3z = 2.1 (2)
2nCu = 2nSO2 => x = 0.2 (mol) (3)
Từ 1, 2, 3 => x = 0,2; y = z = 0,4 (mol)
mCu = 0,2.64 = 12,8 (g)
mMg = 0,4.24 = 9,6 (g)
mAl = 10,8 (g)

Gọi n là hóa trị cao nhất của L, m là hóa trị thấp nhất, x là số mol pứ
n có thể = m hoặc n>m
\(n_{H_2}=\dfrac{1,344}{22,4}=0,06\left(mol\right)\)
Cho L tác dụng với Cl2:
\(L+\dfrac{n}{2}Cl_2\underrightarrow{t^o}LCl_n\)
x x
Vì \(LCl_n\) không tác dụng với HCl nên chất rắn X gồm L dư và \(LCl_n\)
\(2L+2mHCl\rightarrow2LCl_m+mH_2\)
\(\dfrac{0,12}{m}\) 0,06
Ta có:
\(n_{L.pứ}=x=0,0775-\dfrac{0,12}{m}=nLCl_n\)
=> \(L.\dfrac{0,12}{m}+\left(0,0775-\dfrac{0,12}{m}\right).\left(L+35,5n\right)=3,0125\)
Với n = m = 2
=> L = 24
Vậy kim loại L là Mg.
☕T.Lam✿

Câu 1 :
n Mg = 4,8/24 =0,2(mol)
n H2 = 3,36/22,4 = 0,15(mol)
Y gồm 0,2 mol Mg và O
Bảo toàn electron :
2n Mg = 2n O + 2n H2
<=> n O = 0,2 - 0,15 = 0,05(mol)
\(2H^+ + O^{2-} \to H_2O\\ 2H^+ + 2e \to H_2\)
Ta có :
n H+ = 2n O + 2n H2 = 0,15.2 + 0,05.2 = 0,4(mol)
=> n H2SO4 = 1/2 nH+ = 0,2(mol)
=> V dd H2SO4 = 0,2/1 = 0,2(lít)
Câu 2 :
Oleum : H2SO4.nSO3
n NaOH = 0,2.0,15 = 0,03(mol)
2NaOH + H2SO4 $\to$ Na2SO4 + 2H2O
n H2SO4 = 1/2 n NaOH = 0,015(mol)
=> trong 200 ml dung dịch X chứa 0,015.2 = 0,03(mol) H2SO4
H2SO4.nSO3 + nH2O $\to$ (n + 1)H2SO4
Theo PTHH :
\(n_{oleum} = \dfrac{n_{H_2SO_4}}{n + 1}\\ \Rightarrow 0,015 = \dfrac{0,03}{n + 1}\\ \Rightarrow n = 1\)
Vậy oleum cần tìm là H2SO4.SO3







\(n_{O_2}=\dfrac{1}{2}\cdot n_{KMnO_4}1=\dfrac{1}{2}\cdot0.1=0.05\left(mol\right)\)
\(n_{H_2}=\dfrac{1.792}{22.4}=0.08\left(mol\right)\)
\(\Rightarrow n_{M\left(dư\right)}=\dfrac{0.08\cdot2}{n}=\dfrac{0.16}{n}\left(mol\right)\)
\(n_{M\left(pư\right)}=\dfrac{0.05\cdot4}{n}=\dfrac{0.2}{n}\left(mol\right)\)
\(m_M=\left(\dfrac{0.16}{n}+\dfrac{0.2}{n}\right)\cdot M=11.7\left(g\right)\)
\(\Leftrightarrow0.36M=11.7n\)
\(\Leftrightarrow M=32.5n\)
\(BL:n=2\Rightarrow M=65\)
\(M:Zn\)
\(\)
* Nhường e:
\(M^0\rightarrow M^{+n}+ne\)
\(n_M\) \(n_M.n\)
* Nhận e:
\(O_2+4e\rightarrow2O^{-2}\)
\(0,05\) \(0,2\)
\(2H^++2e\rightarrow H_2\)
\(0,16\) \(0,08\)
Suy ra cái bảo toàn như trên :D