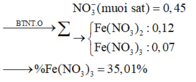Câu 1. Nồng độ mol của dung dịch có chứa 24,48 gam CaSO 4 trong 400ml dung dịch là:
A. 0,25M B. 0,15M C. 0,45M D. 1,25M
Câu 2. Đem cô cạn 200ml dung dịch FeSO 4 0,5M thì khối lượng muối khan thu được là:
A. 10 gam B. 15,2 gam C. 14 gam D. 13,2 gam
Câu 3. Hòa tan 50 gam KNO 3 vào 200 gam nước thu được dung dịch có nồng độ là:
A. 15% B. 20% C. 25% D. 28%
Câu 4. Khối lượng của NaOH có trong 200ml dung dịch NaOH 0,5M là:
A. 2,0 gam B. 4,0 gam C. 8,0 gam D. 16,0 gam
Câu 5. Cho 13 gam kẽm vào dung dịch HCl thì thể tích khí H 2 thoát ra (đkc) là:
A. 2,479 lít B. 4,486 lít C. 9,916 lít D. 4,958 lít
Câu 6. Trộn 200 ml dung dịch NaOH 2M với 300 ml dung dịch H 2 SO 4 1M thu được dung dịch X. Khối
lượng muối trong dung dịch X là.
A. 14,2 gam. B. 28,4 gam. C. 21,3 gam. D. 42,6 gam.
Câu 7. Cho 40 gam CaCO 3 vào dung dịch HCl dư, kết thúc phản ứng thu được bao nhiêu lít khí CO 2 ở
điều kiện chuẩn?
A. 9,942 lít B. 6,724 lít C. 9,916 lít D. 4,958 lít
Câu 8. Cho 4,8 g Mg tác dụng với 9,916 lít khí Cl 2 (đkc). Biết hiệu suất phản ứng là 100%. Hỏi sau phản
ứng chất nào còn dư?
A. Cl 2 B. Mg C. Không có chất dư. D. Cả 2 chất.
Câu 9. Biết rằng khi cho 8,4 gam Mg tác dụng với dung dịch HCl thì thu được 23,275 g MgCl 2 . Hiệu suất
phản ứng là:
A. 65% B. 70% C. 75% D. 80%
Câu 10. Cho a gam Cu tác dụng với oxygen thu được 10,8 gam CuO. Hiệu suất phản ứng là 90%. Giá trị
của a là:
A. 8,64 gam. B. 5,4 gam. C. 7,64 gam. D. 9,6 gam. làm hộ e với
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(C_{M_{HCl}}=a\left(M\right),C_{M_{H_2SO_4}}=b\left(M\right)\)
\(n_{HCl}=a\left(mol\right),n_{H_2SO_4}=b\left(mol\right)\)
\(n_{NaOH}=0.4\cdot0.5=0.2\left(mol\right)\)
\(NaOH+HCl\rightarrow NaCl+H_2O\)
\(a..........a.........a\)
\(2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\)
\(2b............b..........b\)
\(n_{NaOH}=a+2b=0.2\left(mol\right)\left(1\right)\)
\(m_{muối}=58.5a+142b=12.95\left(g\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.1,b=0.05\)
\(\left[H^+\right]=0.1+0.05\cdot2=0.2\left(M\right)\)
\(\left[Cl^-\right]=0.1\left(M\right)\)
\(\left[SO_4^{2-}\right]=0.05\left(M\right)\)
\(b.\)
\(pH=-log\left(0.2\right)=0.7\)

Ta có: n FeSO 4 = 0,2 x 0,5 = 0,1 (mol)
→ m FeSO 4 = 0,1 x 152 = 15,2 (gam)
Chọn B

Ta có:
n FeSO 4 = 0 , 2 x 0 , 5 = 0 , 1 ( mol )
→ m FeSO 4 = 0 , 1 x 152 = 15 , 2 ( gam )

a,Gọi nHCl là a, nH2SO4 là b
mddNaOH = 400×1,2 = 480(g)
mNaOH = (480×5)/100 = 24 (g)
nNaOH = 24/40 = 0,6(mol)
HCl + NaOH-> NaCl + H2O (1)
a -> a (mol)
H2SO4 + 2NaOH-> Na2SO4 +
b -> 2b (mol)
2H2O (2)
Ta có : a + 2b= 0,6
Mà a:b = 1 => a=b, thay a vào phương trình trên ta được
a + 2a = 0,6 <=> 3a = 0,6
=> a = b = 0,6/3 = 0,2 (mol)
CMHCl = 0,2/0,1 = 2M
CMH2SO4 = 0,2/0,1 = 2M
b, Theo (1) và (2) ta có :
nNaCl = nHCl = 0,2 (mol)
nNa2SO4 = nH2SO4 = 0,2 (mol)
Tổng khối lượng muối thu được sau khi cô cạn là:
m= mNaCl + mNa2SO4 = 0,2×58,5 + 0,2×142= 40,1(g)

Chọn A
Gọi nồng độ mol ban đầu của HCl và H 2 S O 4 lần lượt là x và y (M)



Đáp án A
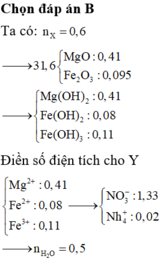
nNH4+ = 0,1 , nK+ = 0,02 , nSO42- = 0,05
Bảo toàn điện tích ⇒ nCl- = 0,1 + 0,02 – 0,05.2 = 0,02
⇒ mchất rắn = mNH4+ + mK+ + mSO42- + mCl- = 8,09g.